Clear Sky Science · pt
Palmitoilação de B7H3 induzida por ácido palmítico promove fuga imune
Por que esta pesquisa importa para pacientes com câncer
A maioria das pessoas já ouviu que novos medicamentos de imunoterapia podem ajudar o sistema imunológico a atacar o câncer, mas muitos pacientes com câncer colorretal comum (do intestino) obtêm pouco benefício. Este estudo revela um truque bioquímico oculto que tumores colorretais usam para se proteger de ataques imunológicos e aponta para um novo tipo de fármaco — um pequeno peptídeo — que poderia tornar a imunoterapia mais eficaz para esses pacientes.
Um obstáculo na imunoterapia atual do câncer intestinal
O câncer colorretal é um dos tipos de câncer mais comuns no mundo. Medicamentos de imunoterapia que liberam os “freios” do sistema imune, como inibidores de PD-1 e PD-L1, transformaram o tratamento de uma minoria de pacientes cujos tumores apresentam muitas mutações no DNA (os chamados tumores MSI-H). Infelizmente, a maioria dos cânceres colorretais é microsatellite-stable (MSS) e responde mal a esses tratamentos. Os autores se concentraram em outra molécula de freio chamada B7H3, que se encontra na superfície das células tumorais e reduz a atividade de células imunes assassinas, especialmente células T CD8+. Eles descobriram que a proteína B7H3 está fortemente elevada em tumores MSS e associada a pior sobrevida, mesmo que o gene subjacente B7H3 não esteja mais ativo. Essa discrepância levantou uma questão importante: o que mantém a proteína B7H3 tão abundante nas células tumorais?
Como uma gordura comum ajuda os tumores a se esconderem
A equipe suspeitou que o metabolismo tumoral pudesse estar estabilizando a B7H3. Ao comparar a atividade gênica e os perfis de pequenas moléculas de tumores colorretais MSS e MSI-H, eles descobriram que muitas vias relacionadas a lipídios diferem, com um ácido graxo em particular se destacando: o ácido palmítico. Quando expuseram células de câncer de cólon a vários produtos de quebra de gorduras em laboratório, apenas o ácido palmítico causou um aumento claro nos níveis da proteína B7H3. Experimentos adicionais mostraram o porquê: o ácido palmítico alimenta um processo de modificação química chamado palmitoilação, no qual uma cadeia gordurosa é ligada a posições específicas nas proteínas. Essa modificação, realizada por uma enzima chamada ZDHHC24 em uma única cisteína dentro da B7H3, tornou a B7H3 mais estável e mais abundante na superfície das células tumorais.
Bloqueando a rota de descarte de um freio imune
As células normalmente removem proteínas indesejadas ou danificadas por mecanismos semelhantes à reciclagem e à coleta de lixo. Os pesquisadores mostraram que a B7H3 é principalmente degradada por uma via celular de “autocataplasia” chamada autofagia, que usa uma proteína receptora chamada SQSTM1/p62 para marcar o material a ser destruído. Quando a B7H3 foi palmitoilada, ela se ligou mal a esse receptor e escapou da degradação autofágica, levando a níveis persistentemente altos do freio imune. Quando o sítio de palmitoilação foi mutado para que não pudesse mais receber a etiqueta gordurosa, ou quando a enzima ZDHHC24 foi deletada, a B7H3 foi direcionada com mais eficiência para os “sacos de lixo” celulares e degradada. Em camundongos, tumores sem a B7H3 palmitoilada cresceram mais lentamente, não alteraram sua taxa intrínseca de crescimento em animais imunodeficientes e apresentaram muito mais células T CD8+ e atividade de morte tumoral mais forte. Isso demonstrou que a modificação age principalmente desarmando a imunidade, e não alterando a velocidade de divisão das células cancerígenas.
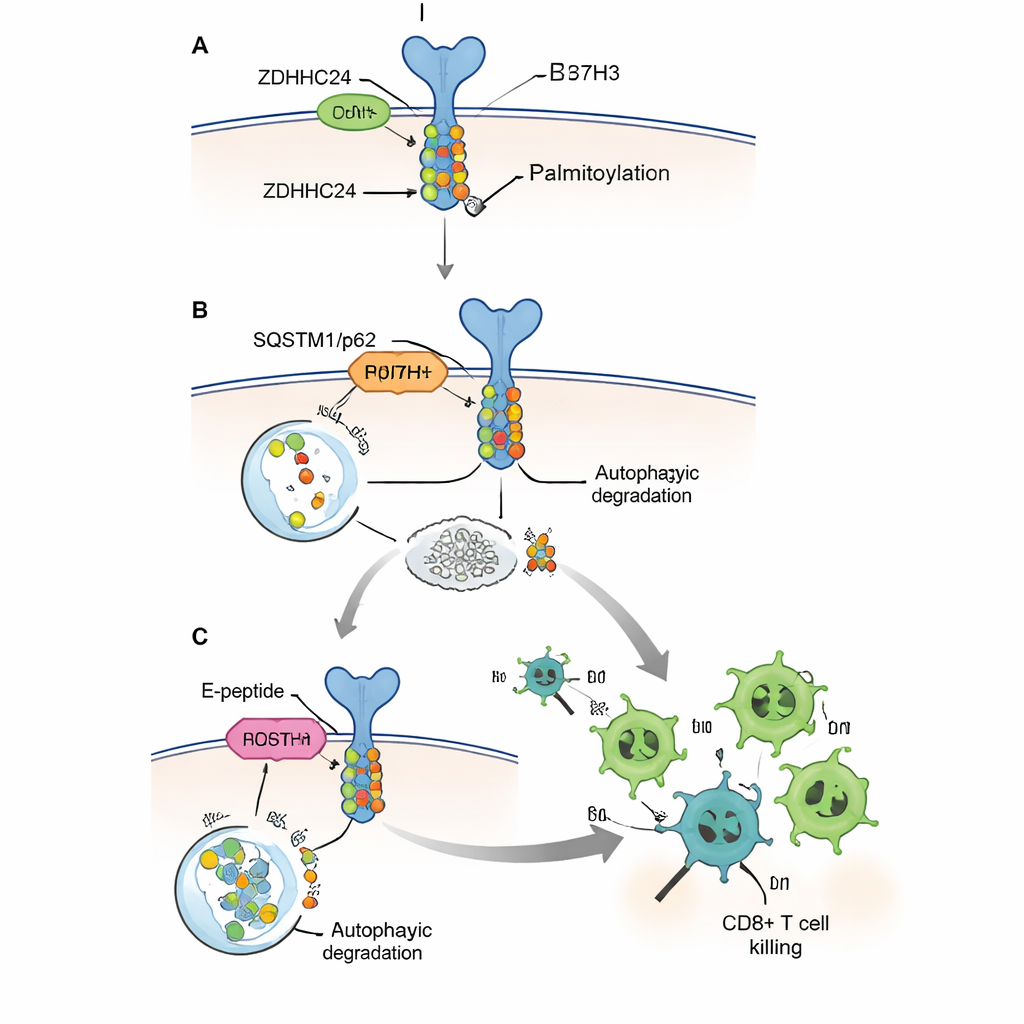
Reduzindo o escudo e potencializando as células T
Como eliminar completamente ZDHHC24 ou B7H3 por abordagens genéticas não é um tratamento prático em pacientes, os autores desenharam um peptídeo curto e penetrante que chamam de peptídeo E. Ele imita um pequeno trecho da proteína B7H3 que normalmente se liga à ZDHHC24, atuando como um engodo que impede a enzima de modificar as moléculas reais de B7H3. Em células em cultura, o peptídeo E reduziu a palmitoilação e os níveis de proteína B7H3, restaurou seu reconhecimento pela maquinaria da autofagia e permitiu que células T CD8+ humanas matassem as células tumorais com mais eficiência. Em vários modelos de camundongo, incluindo um camundongo humanizado portador de células imunes humanas e tumores colorretais humanos, injeções do peptídeo E reduziram tumores, aumentaram o número de células T CD8+ no interior deles e elevaram a produção de moléculas assassinas-chave, como granzima B e interferon-gama.
Um novo parceiro para a imunoterapia existente
Por fim, os pesquisadores perguntaram se essa estratégia poderia funcionar em conjunto com o bloqueio padrão de PD-1. Em modelos murinos de câncer colorretal, tanto o peptídeo E isoladamente quanto o anticorpo anti-PD-1 isoladamente ofereceram algum controle tumoral. Mas quando combinados, os dois tratamentos produziram supressão tumoral muito mais forte e duradoura, em alguns casos fazendo os tumores desaparecerem e mais do que dobrando a sobrevida média em comparação com controles. Isso sugere que desativar o escudo B7H3 cortando seu “âncora” gordurosa pode complementar os medicamentos checkpoint já existentes que têm como alvo a via PD-1.
O que isso significa para tratamentos futuros do câncer
Em termos simples, este estudo mostra que uma gordura dietética comum, o ácido palmítico, pode ser sequestrada por tumores colorretais para blindar quimicamente uma proteína que bloqueia a imunidade (B7H3) e ajudar o câncer a se esconder. Ao bloquear essa única ligação química, os autores foram capazes de remover a blindagem, permitir que os sistemas de descarte da célula removam a B7H3 e reabrir o acesso para que células T CD8+ ataquem. Embora o peptídeo E em si seja uma ferramenta experimental em estágio inicial, o trabalho identifica a palmitoilação de B7H3 — e sua enzima ZDHHC24 — como alvos promissores para fármacos. Se agentes similares mostrarem-se seguros e eficazes em humanos, eles podem um dia transformar mais cânceres colorretais de tumores “frios” que ignoram a imunoterapia em tumores “quentes” que o sistema imune consegue reconhecer e destruir.
Citação: Rao, Z., Huang, C., Wu, Q. et al. Palmitic acid-triggered B7H3 palmitoylation promotes immune escape. Nat Commun 17, 1810 (2026). https://doi.org/10.1038/s41467-026-68525-x
Palavras-chave: imunoterapia do câncer colorretal, checkpoint B7H3, metabolismo do ácido palmítico, palmitoilação de proteínas, imunidade tumoral por células T CD8