Clear Sky Science · pt
Macrófagos de peixe-zebra convertem sinais físicos de ferimentos em rápida permeabilização vascular
Como um Peixe Minúsculo Nos Ensina Sobre o Inchaço de Feridas
Quando você ralha o joelho, a área logo fica vermelha, inchada e com vazamento de fluidos. Essa mudança rápida nos vasos sanguíneos vizinhos é crucial para combater infecções e iniciar a reparação, mas exatamente como o corpo percebe o dano e reage em questão de segundos tem sido difícil de observar em tempo real. Usando larvas de peixe-zebra translúcidas e imageamento ao vivo avançado, este estudo revela como células imunes especializadas envoltas nos vasos sanguíneos convertem o choque físico de uma ferida em um vazamento quase instantâneo dos vasos, oferecendo novos insights sobre inflamação, cicatrização e até lesão pulmonar humana.
Observando Como a Lesão Se Espalha pelo Corpo
Os pesquisadores trabalharam com peixes-zebra jovens, cujos corpos transparentes permitem aos cientistas assistir células e vasos sanguíneos em ação ao microscópio. Eles cortaram a ponta da nadadeira caudal e preencheram a circulação com um corante fluorescente que permanece dentro de vasos saudáveis. Quando os peixes feridos foram colocados de volta em água doce normal, o súbito influxo de água nos tecidos criou um “choque osmótico” ao redor da ferida. Em minutos, os vasos próximos dilataram e começaram a vazar o corante fluorescente para o tecido circundante, imitando o inchaço e o exsudato que ocorrem em feridas humanas. Ao transferir os peixes entre água normal e soluções salinas ou açucaradas especialmente balanceadas, a equipe demonstrou que essa permeabilização vascular rápida depende fortemente de mudanças osmóticas, e não apenas do simples rompimento do tecido.
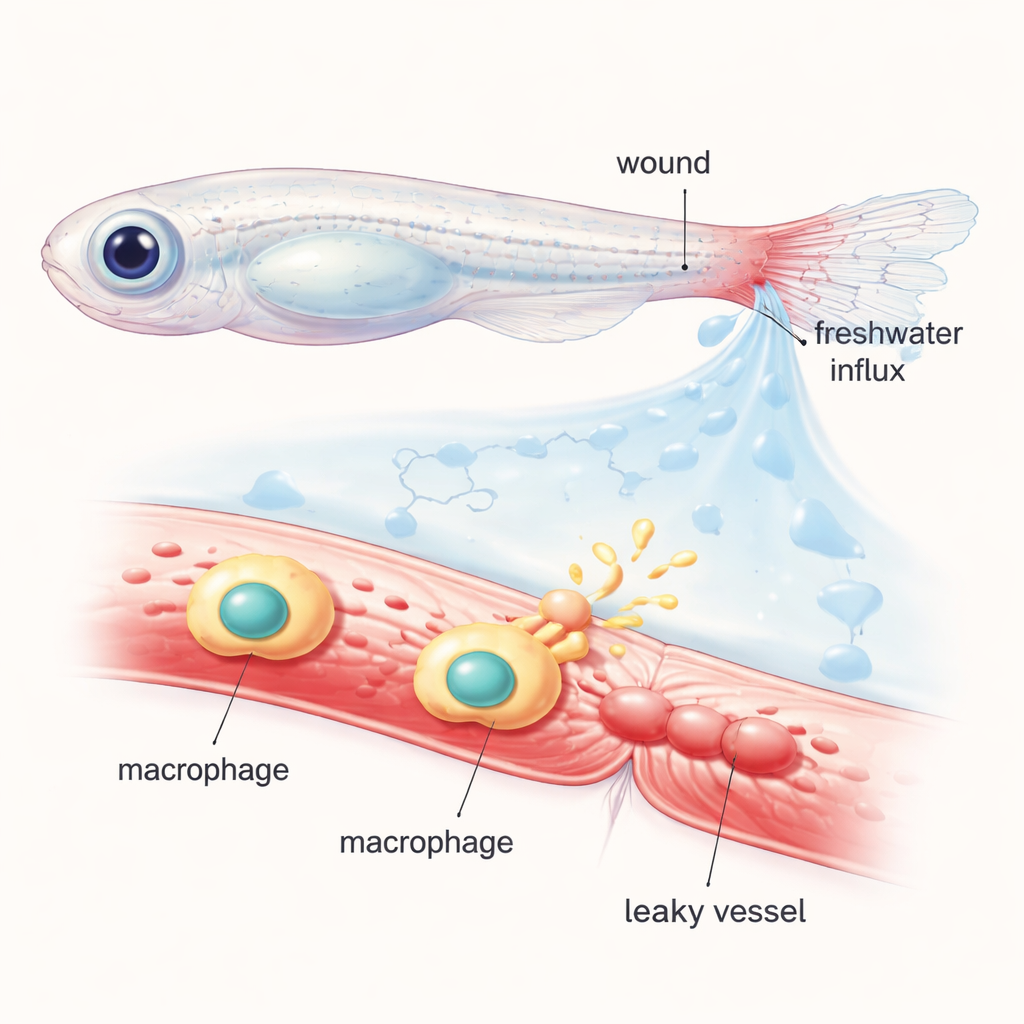
Rastreando os Mensageiros Químicos por Trás do Vazamento
Para descobrir quais moléculas convertem o choque físico em sinal de vazamento, os cientistas examinaram uma família de compostos gordurosos chamados eicosanoides, originados do ácido araquidônico. Esses lipídios são bem conhecidos por seus papéis na inflamação e no fluxo sanguíneo. Usando mutantes genéticos e fármacos, eles desativaram seletivamente enzimas individuais na via dos eicosanoides. Bloquear uma enzima-chave chamada Alox5a (5-lipoxigenase) ou sua parceira Lta4h reduziu fortemente a quantidade de corante que escapou dos vasos após o choque osmótico, sem impedir o fechamento da ferida em si. Em contraste, interferir com outras enzimas relacionadas teve pouco efeito. Isso apontou para um ramo específico da via lipídica como o principal motor da resposta rápida de vazamento, atuando quase como uma válvula química que pode ser aberta ou fechada sob demanda.
O Papel Surpreendente das Células Imunes que Abraçam os Vasos
O sangue contém diferentes tipos de células imunes e, em larvas de peixe-zebra, neutrófilos e macrófagos são os protagonistas. A equipe usou um truque genético inteligente para destruir seletivamente neutrófilos ou macrófagos antes de causar a ferida. Remover neutrófilos teve pouco impacto no vazamento vascular. Mas quando os macrófagos foram eliminados, a resposta de vazamento caiu cerca de metade, refletindo o efeito de bloquear a via lipídica Alox5a–Lta4h. Importante, essas manipulações não impediram que a ferida fechasse rapidamente, mostrando que o recrutamento de leucócitos e o vazamento vascular podem ser controlados de modo relativamente independente. Isso revelou os macrófagos perivasculares — macrófagos posicionados firmemente ao longo do exterior dos vasos — como tradutores-chave entre o dano físico e o comportamento vascular.
Do Estiramento Nuclear ao Sinal Químico
Como esses macrófagos perivasculares detectam uma ferida que pode estar a certa distância? A resposta está na forma como seus núcleos respondem ao estresse mecânico. Quando o choque osmótico da ferida se espalha pelo tecido próximo, a entrada de água causa um leve inchaço celular e deformação nuclear. Os pesquisadores marcaram uma enzima mecanossensível chamada cPla2 com um marcador fluorescente e a expressaram especificamente em macrófagos. Após a ferida em água doce normal, a cPla2 mudou rapidamente para a superfície interna da membrana nuclear em macrófagos, movendo-se em uma onda que varreu o tecido a cerca de 50 micrômetros por segundo, compatível com a propagação dos sais dissolvidos. Essa translocação dependia de condições hipotônicas e foi muito mais fraca em soluções isotônicas. Macrófagos próximos aos vasos sanguíneos apresentaram pulsos especialmente nítidos e reversíveis de ligação nuclear de cPla2, os quais liberam ácido araquidônico para conversão em lipídios que induzem o vazamento.
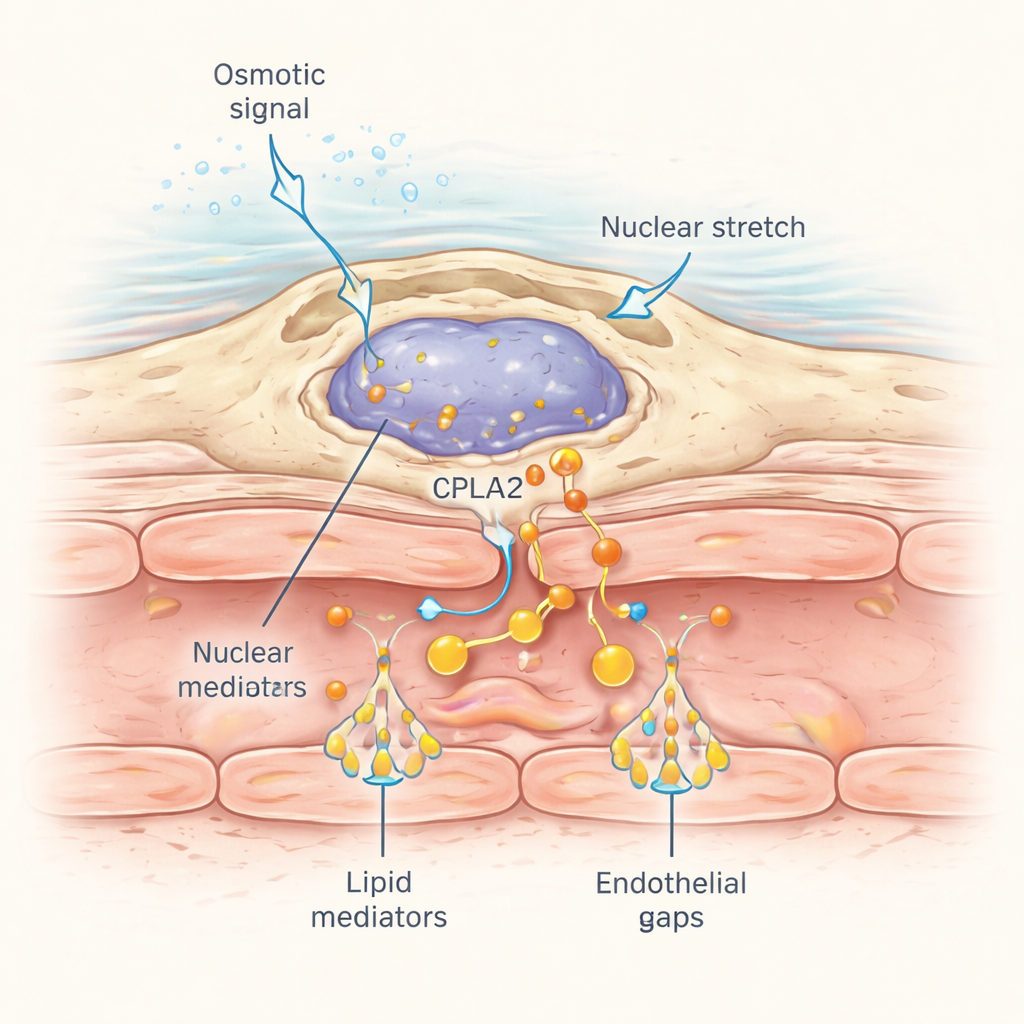
Por Que Isso Importa Além dos Peixes
Em termos simples, este estudo mostra que certos macrófagos atuam como sentinelas físicas: eles percebem o estiramento dos tecidos e das membranas nucleares causado por mudanças osmóticas numa ferida, ativam a cPla2 na superfície nuclear e rapidamente produzem mensageiros lipídicos que dizem aos vasos sanguíneos próximos para “abrir os portões” e permitir que fluido e fatores imunes entrem em massa. Embora os peixes-zebra vivam em água doce e enfrentem desafios osmóticos únicos, vias mecanossensíveis semelhantes provavelmente operam em tecidos humanos expostos a pressões e fluxos variáveis, como os pulmões durante a ventilação mecânica. Entender como o estiramento nuclear e os sinais lipídicos controlam a permeabilidade vascular em tempo real pode, a longo prazo, orientar tratamentos que ajustem a inflamação — seja atenuando vazamentos prejudiciais em condições como lesão pulmonar aguda, seja reforçando respostas úteis para acelerar a reparação tecidual.
Citação: Gelashvili, Z., Shen, Z., Ma, Y. et al. Zebrafish macrophages convert physical wound signals into rapid vascular permeabilization. Nat Commun 17, 1807 (2026). https://doi.org/10.1038/s41467-026-68520-2
Palavras-chave: cicatrização de feridas, vasos sanguíneos, macrófagos, inflamação, peixe-zebra