Clear Sky Science · pt
Células líquidas ultrafinas para cryo-EM cronometrada em microsegundos
Observando proteínas em ação em tempo real
Muitas das máquinas que mantêm nossas células vivas são formadas por proteínas, e frequentemente sabemos como essas proteínas parecem quando congeladas em posição. Mas o que realmente queremos ver é como elas se movem enquanto desempenham suas funções. Este estudo apresenta uma nova forma de observar esses movimentos em escalas de tempo incrivelmente curtas — milionésimos de segundo — sem sacrificar o nível de detalhe que a microscopia eletrônica criogênica (cryo-EM) moderna pode fornecer.
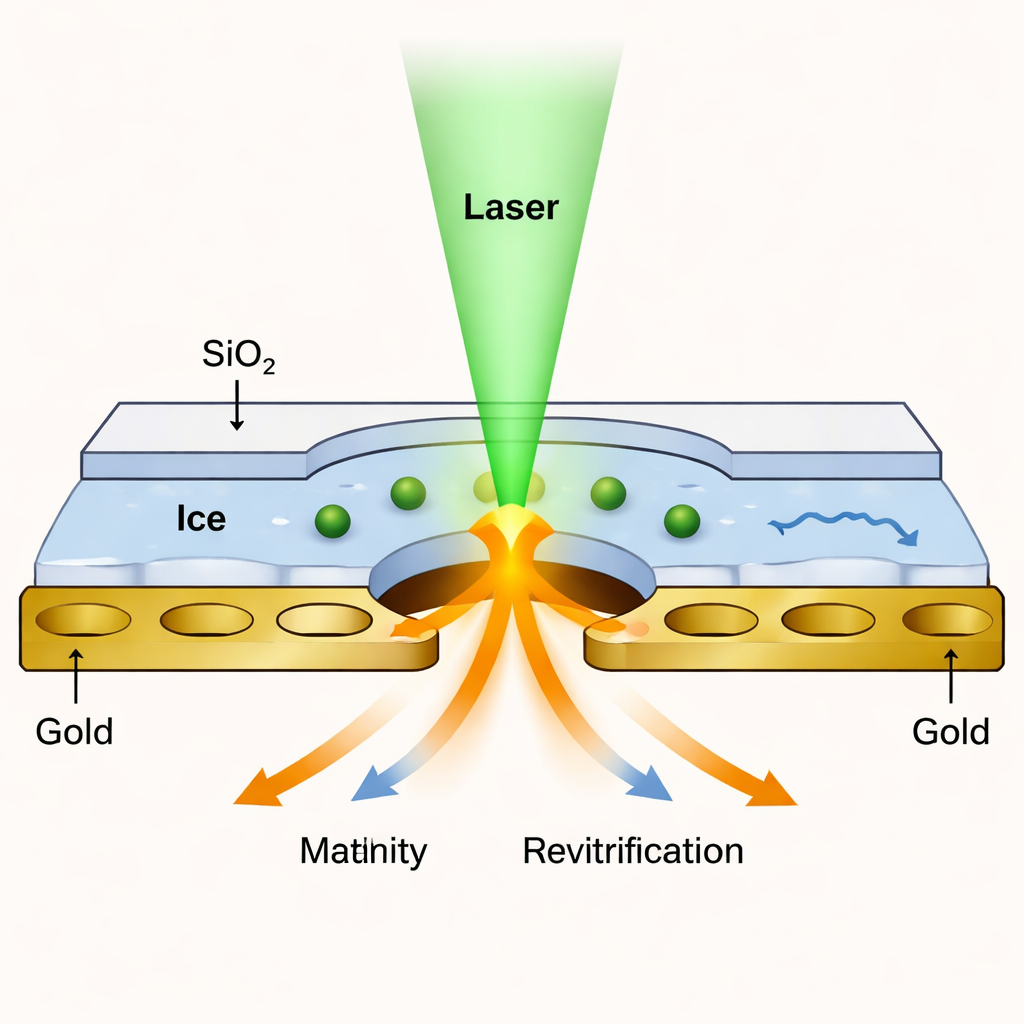
Uma nova janela para o mundo microscópico
A cryo-EM revolucionou a biologia estrutural ao imagear proteínas congeladas por congelamento rápido com resolução quase atômica. No entanto, os métodos tradicionais mostram apenas imagens estáticas. Para capturar movimento, pesquisadores desenvolveram a “cryo-EM cronometrada em microsegundos”, em que um laser funde brevemente uma amostra congelada para que as proteínas possam se mover, e então a amostra é rapidamente recongelada para aprisioná-las em novas posições. O problema tem sido que o filme líquido minúsculo criado pelo laser tende a se romper após algumas dezenas de microsegundos, limitando por quanto tempo as proteínas podem ser observadas. O novo trabalho resolve esse gargalo ao encapsular a amostra em uma célula líquida ultrafina, mantendo-a estável tempo suficiente para observar movimentos mais lentos e complexos.
Construindo uma célula líquida ultrafina
A equipe criou uma espécie de sanduíche nanoscópico: a solução de proteína é congelada em uma grade padrão de ouro perfurada, e então ambos os lados são revestidos com camadas de dióxido de silício com apenas cerca de 1,4 nanômetro de espessura — apenas alguns átomos. Essas camadas vítreas atuam como tampas transparentes que impedem a evaporação do líquido quando o laser funde o gelo. Pulsos curtos de laser aquecem a amostra selada a uma temperatura controlada e em seguida permitem que ela recongele em poucos microsegundos. Como as membranas são tão finas, ainda deixam passar elétrons suficientes para que o microscópio produza imagens com praticamente a mesma resolução da cryo-EM convencional, até cerca de 1,7–1,8 ångströms para uma proteína teste chamada apoferritina.
Vistas mais nítidas e ângulos mais justos
Um desafio oculto na cryo-EM é que as proteínas tendem a aderir à interface ar–água na fina camada de gelo, alinhando-se em orientações similares e dificultando a reconstrução de uma vista 3D completa. Os revestimentos de dióxido de silício nessas células líquidas transformam a superfície de água–ar em água–sólido e a tornam mais amigável à água. Como resultado, as proteínas têm menos probabilidade de ficar presas em uma única pose. Quando os autores testaram uma grande máquina celular chamada subunidade ribossomal 50S, descobriram que a distribuição angular das partículas tornou-se quase perfeitamente uniforme, eliminando essencialmente o problema de longa data da “orientação preferencial”, ao mesmo tempo em que mantinha alta resolução nas reconstruções finais.
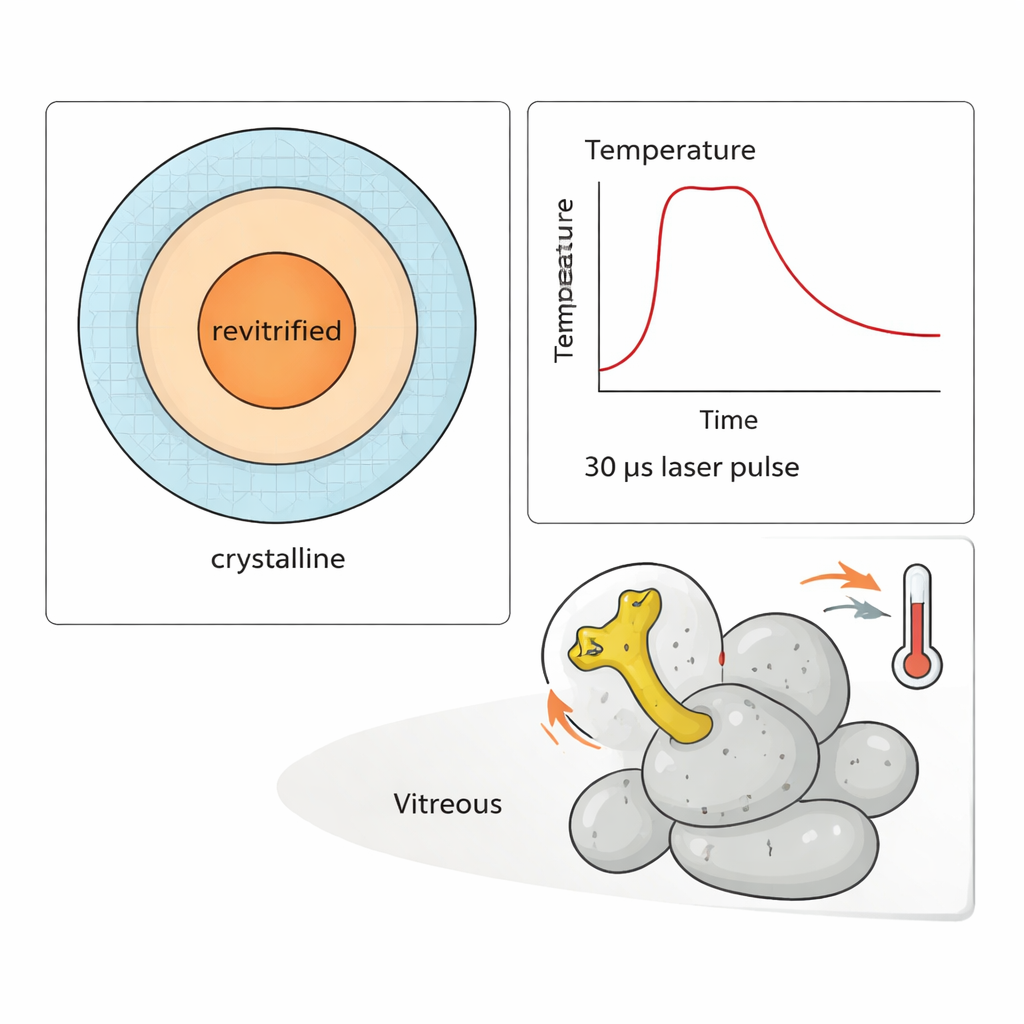
Marcando o tempo do movimento de uma alavanca molecular
Para demonstrar o poder do método, os pesquisadores realizaram um experimento de “salto de temperatura” na subunidade 50S. Um braço flexível nessa partícula, conhecido como haste L1, oscila como uma alavanca durante a síntese proteica. Ao fornecer trens de pulsos de laser de 30 microssegundos, eles puderam aquecer a amostra a diferentes temperaturas por até cerca de 300 microssegundos e então recongelá-la. Simulações e medições de quais regiões recongelaram como vidro permitiram estimar a temperatura de cada partícula observada. Analisando milhares de imagens, mostraram que a amplitude do movimento da haste L1 aumenta claramente com a temperatura — mas apenas após centenas de microssegundos. Em tempos iniciais, a distribuição de conformações ainda reflete o estado original em temperatura ambiente antes do congelamento.
Por que isso importa para a biologia futura
Para não especialistas, a mensagem principal é que esse desenho de célula líquida ultrafina estende dramaticamente por quanto tempo as proteínas podem ser observadas em movimento sem borrar os detalhes estruturais. Ele desloca a cryo-EM cronometrada em microsegundos de capturar apenas os eventos mais rápidos para sondar rearranjos mais lentos e biologicamente relevantes, como a resposta retardada da haste L1 a um pulso térmico. Com refinamentos adicionais, essa abordagem pode preencher a lacuna até a faixa de milissegundos e além, e também oferece novas maneiras de preparar amostras, reduzir artefatos de imagem e disparar reações diretamente na grade. Em termos práticos, isso significa que os cientistas estão mais próximos de produzir “filmes moleculares” que conectam as formas das proteínas ao que elas realmente fazem dentro de células vivas.
Citação: Curtis, W.A., Wenz, J., Krüger, C.R. et al. Ultrathin liquid cells for microsecond time-resolved cryo-EM. Nat Commun 17, 1799 (2026). https://doi.org/10.1038/s41467-026-68515-z
Palavras-chave: cryo-EM cronometrada, dinâmica de proteínas, microscopia eletrônica de célula líquida, haste L1 do ribossomo, membranas ultrafinas de dióxido de silício