Clear Sky Science · pt
Forças mecânicas da auto‑montagem peptídica intercelular impulsionam a formação de esferoides
Construindo Pequenos Tecidos no Laboratório
Cientistas correm para criar versões em miniatura de tecidos humanos que se comportem como os reais. Esses modelos vivos podem tornar os testes de medicamentos contra o câncer mais seguros e aproximar novos tratamentos para diabetes e outras doenças da realidade. Este estudo apresenta uma maneira engenhosa de induzir células a formar aglomerados tridimensionais realistas, completos com suas próprias redes primitivas “semelhantes a vasos” que melhoram a entrega de nutrientes e a função.
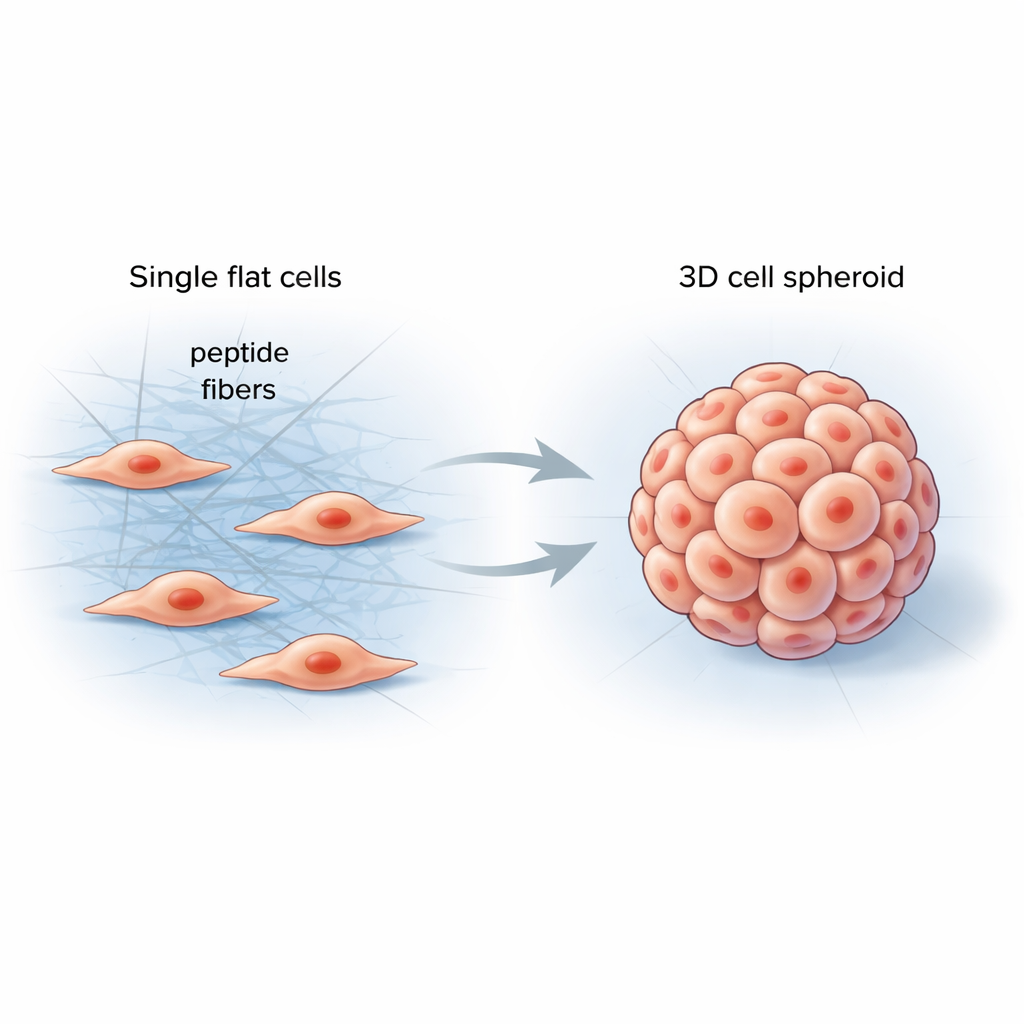
Ajudando as Células a Sentir o Ambiente
Dentro do nosso corpo, as células vivem em um ambiente macio, porém estruturado, chamado matriz extracelular — uma malha de proteínas que sustenta os tecidos e envia sinais mecânicos constantes às células. Materiais convencionais de laboratório têm dificuldade em imitar essa complexidade, frequentemente produzindo camadas celulares planas que se comportam de modo muito diferente de órgãos ou tumores reais. Os pesquisadores buscaram projetar um material simples e programável que se formasse diretamente entre as células, rigidizasse seu entorno de maneira controlada e as impulsionasse a assumir formas tridimensionais mais naturais.
Peptídeos Inteligentes que se Montam entre Células
A equipe criou fragmentos curtos de proteína, chamados peptídeos, que podem se ligar em fibras longas e finas quando encontram enzimas específicas na superfície celular. Quando esses peptídeos foram adicionados a células cancerígenas, permaneceram inativos a princípio, como uma solução clara. Após as próprias enzimas das células retirarem parte da molécula, os peptídeos se auto‑montaram rapidamente em uma rede fibrosa envolvendo e conectando as células vizinhas. Essa nova malha de fibras alterou as forças mecânicas locais, encorajando as células a se puxarem mutuamente, reorganizarem seu arcabouço interno e se agregarem em esferoides 3D arredondados em vez de se espalharem em uma lâmina.
De Aglomerados Celulares a Redes Semelhantes a Vasos
Para se aproximar ainda mais do tecido real, os cientistas introduziram em seguida células endoteliais humanas, o tipo que normalmente reveste vasos sanguíneos, junto com um segundo peptídeo carregando uma pequena “etiqueta de endereço” que atrai essas células. Juntos, os peptídeos original e modificado formaram um andaime de nanofibras compartilhado. As células endoteliais usaram esse andaime para brotar em extensões tubulares que envolveram e penetraram os esferoides, criando estruturas semelhantes a capilares. Quando a equipe fez fluir moléculas fluorescentes semelhantes a açúcares ao redor dessas estruturas, observaram penetração muito mais profunda no núcleo do esferoide em comparação com esferoides sem esses tubos internos, mostrando que o transporte de nutrientes e sinais foi significativamente melhorado.
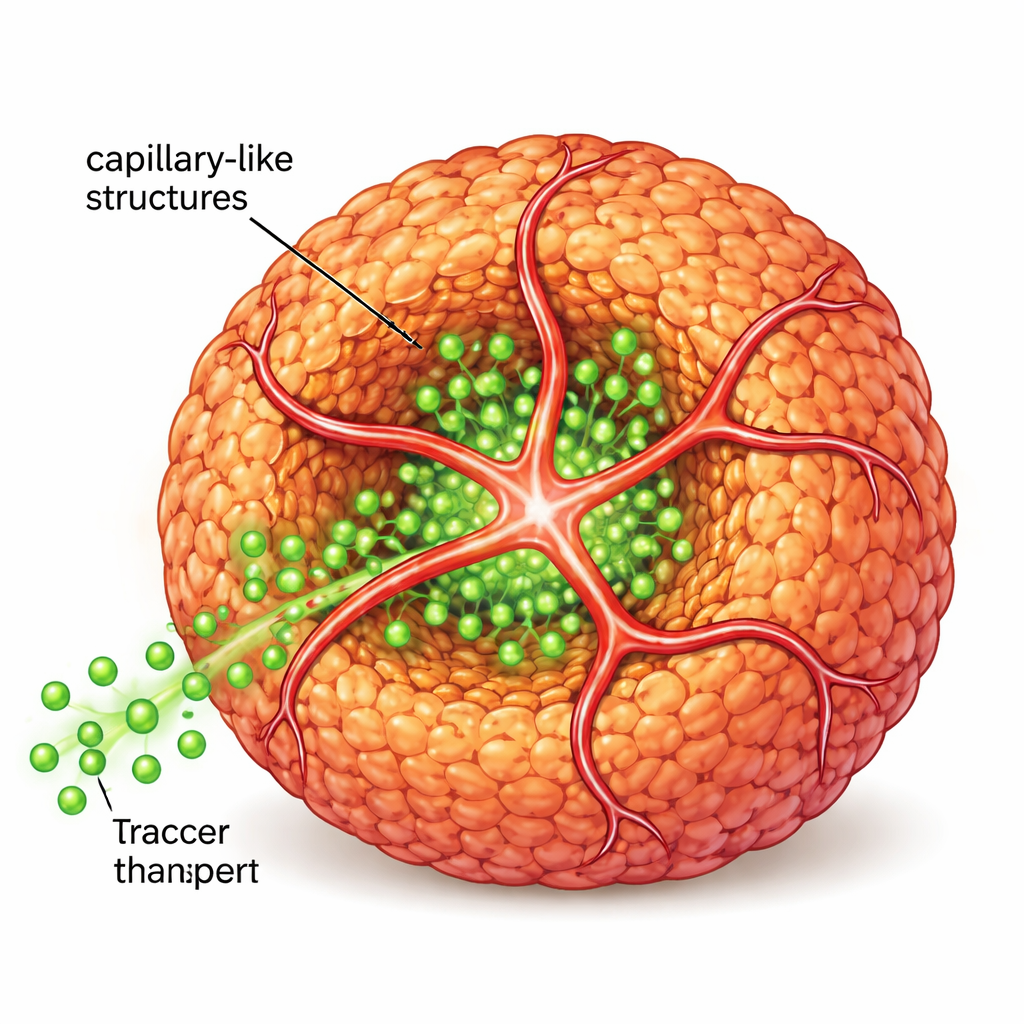
Mais Próximo de Tumores Reais e Ilhotas Funcionais
O perfil de atividade gênica revelou que esferoides tumorais com estruturas semelhantes a capilares se assemelhavam mais a amostras de glioblastoma de pacientes do que culturas tradicionais planas ou esferoides não vascularizados. Em camundongos, esferoides contendo essas redes vasculares primitivas cresceram para tumores maiores e mais vascularizados, indicando que o modelo in vitro captura características-chave do comportamento tumoral real. A mesma estratégia foi aplicada a células beta pancreáticas, que normalmente vivem em ilhotas altamente vascularizadas e secretam insulina em resposta à glicose. Quando esferoides de células beta foram equipados com estruturas semelhantes a capilares usando o sistema peptídico e células endoteliais, mostraram liberação de insulina muito mais forte e refinada, sugerindo uma ferramenta poderosa para pesquisa em diabetes e medicina regenerativa.
Por Que Isso Importa para Terapias Futuras
Ao permitir que peptídeos simples se auto‑montem entre células vivas, este trabalho oferece uma receita geral para construir tecidos em miniatura vascularizados que se sentem e funcionam mais como os do corpo. Os esferoides resultantes espelham melhor tumores de pacientes e ilhotas funcionais, tornando‑os valiosos para testar fármacos, estudar mecanismos de doença e projetar novas terapias baseadas em células. Para o público não especializado, a principal conclusão é que dar às células cultivadas em laboratório a “sensação correta” e pequenas redes semelhantes a vasos pode melhorar dramaticamente o quanto elas imitam tecidos humanos, acelerando potencialmente o caminho da pesquisa básica até tratamentos eficazes.
Citação: Lu, H., Li, Y., Yang, X. et al. Mechanical forces from intercellular peptide self-assembly drive spheroid formation. Nat Commun 17, 1801 (2026). https://doi.org/10.1038/s41467-026-68513-1
Palavras-chave: engenharia de tecidos, modelos de câncer, angiogênese, organoides, auto‑montagem de peptídeos