Clear Sky Science · pt
Jejum intermitente inibe glioma dirigido por Tp53 por meio da regulação metionina-m6A mediada pelo microbiota intestinal
Por que dar um descanso ao intestino pode desacelerar tumores cerebrais letais
O glioblastoma está entre os cânceres cerebrais mais agressivos, e os tratamentos atuais — cirurgia, radioterapia e quimioterapia — muitas vezes aumentam o tempo de sobrevida dos pacientes apenas modestamente. Este estudo investiga uma pergunta simples, porém de grande impacto para a vida cotidiana: será que a forma como comemos, especificamente o jejum intermitente, pode alterar nossas bactérias intestinais e a química sanguínea o suficiente para retardar de modo significativo certos tumores cerebrais?
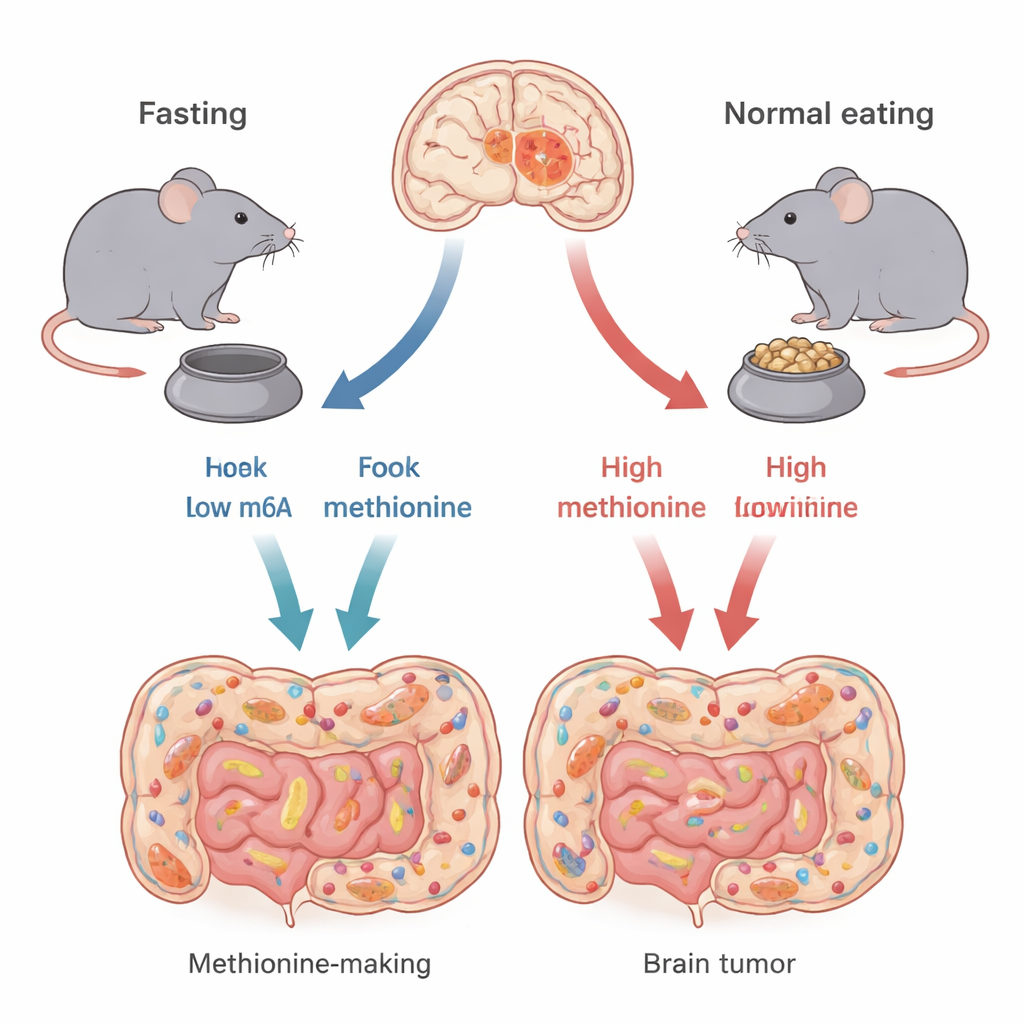
Diferentes tipos do “mesmo” câncer cerebral
Nem todos os glioblastomas são iguais. Os autores concentram-se em dois grandes tipos genéticos, definidos por alterações nos genes TP53 e CDKN2A. Esses genes ajudam a controlar como as células crescem ou morrem. Usando modelos de camundongos que reproduzem bem cada subtipo humano, os pesquisadores mostram que o jejum intermitente — 24 horas sem alimento seguidas de 24 horas com alimento — não beneficia todos os tumores cerebrais da mesma forma. Camundongos com tumores do tipo TP53 viveram mais e tiveram tumores menores quando jejuaram, enquanto camundongos com tumores do tipo CDKN2A mostraram pouco benefício. Isso sugere que a eficácia do jejum pode depender fortemente da configuração genética do tumor.
Do padrão alimentar às bactérias intestinais e à química cerebral
A equipe então investigou como o jejum produz seu efeito seletivo. Como a quantidade total de comida foi mantida igual entre os grupos, a diferença-chave foi o momento da alimentação. Esse timing remodelou de forma marcante o microbiota intestinal — a vasta comunidade de bactérias no intestino. Nos camundongos TP53 em jejum, certos grupos bacterianos que produzem de forma eficiente o aminoácido metionina, como cepas específicas de Alistipes e Prevotella, diminuíram em abundância. Como a metionina é um bloco de construção essencial que os animais devem obter da dieta ou de microrganismos intestinais, essa mudança microbiana resultou em menos metionina fluindo do intestino para o sangue e, por fim, para o cérebro.
Como um único nutriente afina sinais que impulsionam o câncer
A metionina não é apenas um nutriente; é também matéria-prima para a S-adenosilmetionina (SAM), o “doador de metil” universal da célula. A SAM alimenta um processo químico de marcação no RNA chamado m6A. Essas marcas ajudam a controlar a intensidade com que certos genes são expressos. No modelo tumoral TP53, o jejum reduziu os níveis de metionina e de SAM no sangue e nas regiões tumorais do cérebro. Utilizando várias camadas de tecnologias ômicas — sequenciamento de RNA padrão, perfilização de RNA em célula única e mapas espaciais tanto da atividade gênica quanto de metabólitos — os pesquisadores encontraram menos marcas m6A em RNAs ligados ao câncer sob jejum. Um alvo importante foi TGFB2, um gene da via de sinalização TGF‑β, conhecido por impulsionar o crescimento e a invasão tumoral. Com o jejum, a enzima METTL3 (que adiciona marcas m6A) e TGFB2 foram ambas reduzidas, e a sinalização TGF‑β enfraqueceu.
Provando causalidade com intervenções direcionadas
Para ir além da correlação, os cientistas realizaram experimentos de “resgate”. Bloquearam a METTL3 com um fármaco, ou transferiram bactérias intestinais de camundongos em jejum para camundongos alimentados normalmente, e observaram desaceleração do crescimento tumoral mesmo sem jejum — apoiando a ideia de que tanto o microbiota quanto a maquinaria m6A são peças-chave. Por outro lado, quando camundongos em jejum receberam metionina extra ou foram tratados com um fármaco que aumenta marcas m6A, seus tumores cresceram de modo semelhante aos de camundongos alimentados normalmente, e a vantagem de sobrevida desapareceu. Importante notar que a perturbação das bactérias intestinais com antibióticos de amplo espectro eliminou muitas das mudanças associadas ao jejum, reforçando que a comunidade intestinal é um elo central nessa cadeia de eventos.
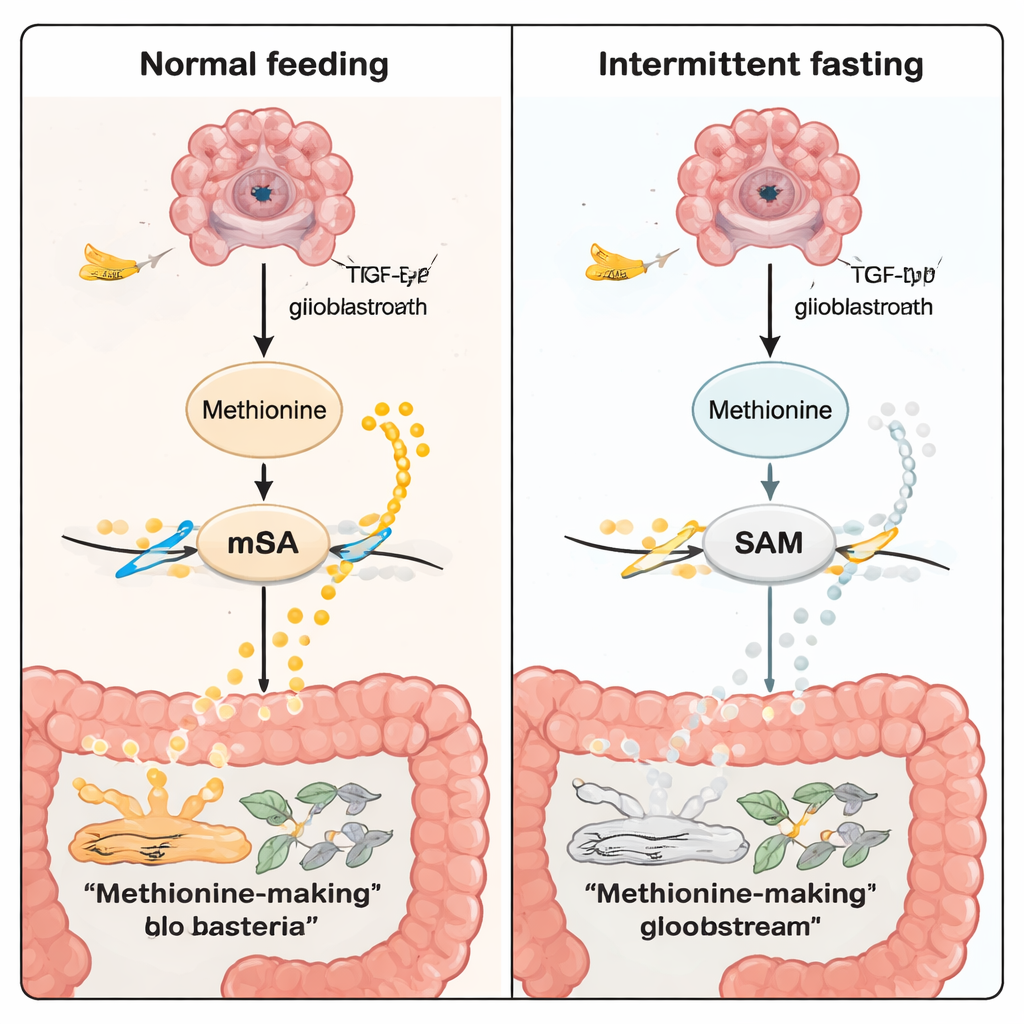
O que isso significa para pessoas e terapias futuras
Para o leitor leigo, a mensagem central é que nem todos os cânceres, ou mesmo todos os glioblastomas, responderão da mesma forma a uma estratégia dietética como o jejum intermitente. Em gliomas do tipo TP53, o jejum parece “conversar” com o cérebro por meio do intestino: remodela as bactérias intestinais, que por sua vez reduzem a produção de metionina, diminuem a marcação química do RNA e atenuam sinais de crescimento potentes dentro das células tumorais. Embora este trabalho tenha sido feito em camundongos e exija tradução clínica cuidadosa, aponta para um futuro em que padrões simples de estilo de vida, tratamentos baseados no microbiota intestinal e fármacos que miram a metionina ou as vias m6A possam ser adaptados ao subtipo genético do tumor de um paciente.
Citação: Lin, Y., Li, S., Xu, X. et al. Intermittent fasting inhibits Tp53-driven glioma through gut microbiota-mediated methionine-m6A regulation. Nat Commun 17, 1804 (2026). https://doi.org/10.1038/s41467-026-68512-2
Palavras-chave: jejum intermitente, glioblastoma, microbioma intestinal, metabolismo da metionina, modificação de RNA m6A