Clear Sky Science · pt
Oxidação simultânea de sulfeto e redução de sulfato para homeostase redox intracelular em condições altamente ácidas
Por que a limpeza de gases tóxicos precisa de micróbios inteligentes
Muitas indústrias liberam sulfeto de hidrogênio, um gás venenoso com odor de ovo podre que pode corroer equipamentos, contaminar o ar e prejudicar trabalhadores. Para eliminá‑lo, engenheiros dependem cada vez mais de micróbios que transformam o sulfeto em formas de enxofre mais seguras. Este artigo revela uma estratégia microbiana inesperada: um Mycobacterium recém‑identificado que executa simultaneamente duas vias químicas normalmente opostas para detoxificar o sulfeto rapidamente e, ao mesmo tempo, proteger-se de danos internos, mesmo em condições extremamente ácidas.
Uma disputa no ciclo do enxofre
Na natureza, o ciclo do enxofre é movido por duas reações opostas. Alguns micróbios oxidam o sulfeto (a forma mais reduzida e tóxica) a produtos menos nocivos, como enxofre elementar ou sulfato, obtendo energia no processo. Outros seguem o caminho inverso, reduzindo sulfato de volta a sulfeto para sintetizar componentes celulares essenciais, como aminoácidos contendo enxofre. Como essas reações se anulam, biólogos presumiram por muito tempo que uma única célula evitaria executar ambas ao mesmo tempo; isso pareceria desperdício, como aquecer e resfriar uma casa com as janelas abertas. 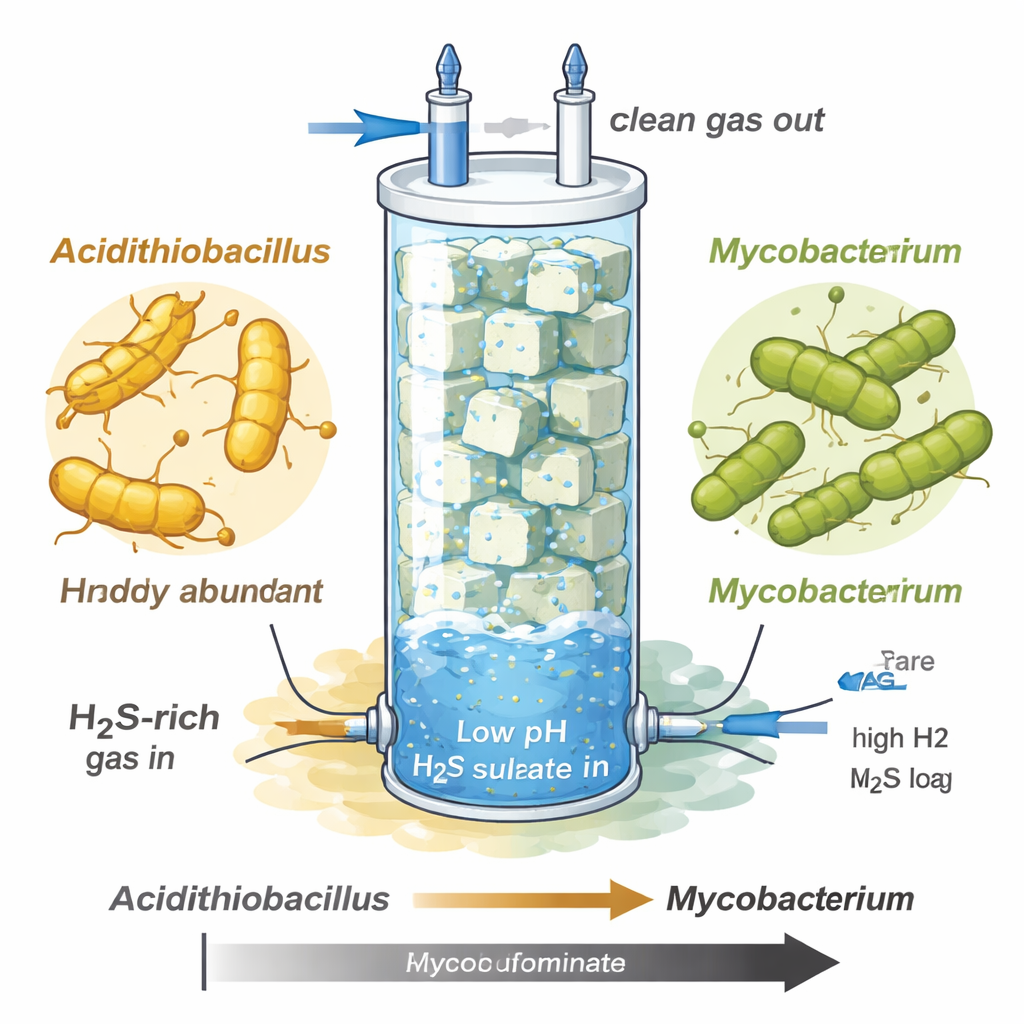
Encontrando uma sobrevivente em um reator extremo
Os pesquisadores estudaram um filtro biotrickling—uma coluna de vidro alta preenchida com cubos de espuma—projetado para remover sulfeto de hidrogênio de correntes gasosas semelhantes a biogás bruto ou gás natural. À medida que aumentaram a carga de sulfeto e mantiveram o sistema muito ácido (pH em torno de 1–1,5), a comunidade microbiana mudou dramaticamente. No início, um oxidante de sulfeto bem conhecido, chamado Acidithiobacillus, prosperava e convertia grande parte do sulfeto em sulfato, mas depois entrou em colapso sob o estresse extremo de sulfeto. Em seu lugar, uma espécie de Mycobacterium previamente não caracterizada, rotulada MAG‑M116, assumiu quase toda a comunidade, apesar de crescer mais lentamente na fase inicial, menos severa.
Um micróbio que quebra as regras usuais
Análises genéticas e em nível de proteínas mostraram que MAG‑M116 possui um arranjo metabólico incomum. Ele carrega uma enzima chave, sulfeto:quinona oxidorredutase, que oxida o sulfeto apenas até o enxofre elementar sólido, que se acumula como partículas minúsculas. Ao mesmo tempo, o micróbio possui um conjunto completo de genes para redução assimilatória de sulfato, a via que incorpora o sulfato na célula e o reduz para sintetizar aminoácidos como cisteína e metionina. Em condições de alto sulfeto, ambas as vias foram ativadas simultaneamente. A oxidação do sulfeto injetava elétrons na máquina energética da célula, enquanto a redução do sulfato absorvia parte desse fluxo eletrônico, vinculando as duas direções do ciclo do enxofre dentro de uma única célula.
Transformando um ciclo “desperdiçador” em uma válvula de segurança
Executar ambas as vias ao mesmo tempo poderia, em teoria, ser fútil—queimando energia sem ganho líquido. Mas a equipe mostra que, para MAG‑M116, isso atua como uma válvula de segurança para elétrons em excesso. Oxidar grandes quantidades de sulfeto libera uma onda de elétrons na cadeia respiratória da célula, que pode vazar e gerar espécies reativas de oxigênio (EROs)—moléculas nocivas que atacam DNA, proteínas e membranas. Ao reduzir ativamente o sulfato para aminoácidos, a célula desvia 10–14% desses elétrons para trabalho construtivo, reduzindo o acúmulo de um estado excessivamente reduzido, propenso a vazamentos. Experimentos comparando condições com e sem sulfato mostraram que a redução ativa de sulfato cortou a produção de EROs em até cerca de 60% e evitou o acúmulo de cofatores reduzidos que, de outra forma, alimentariam danos oxidativos. 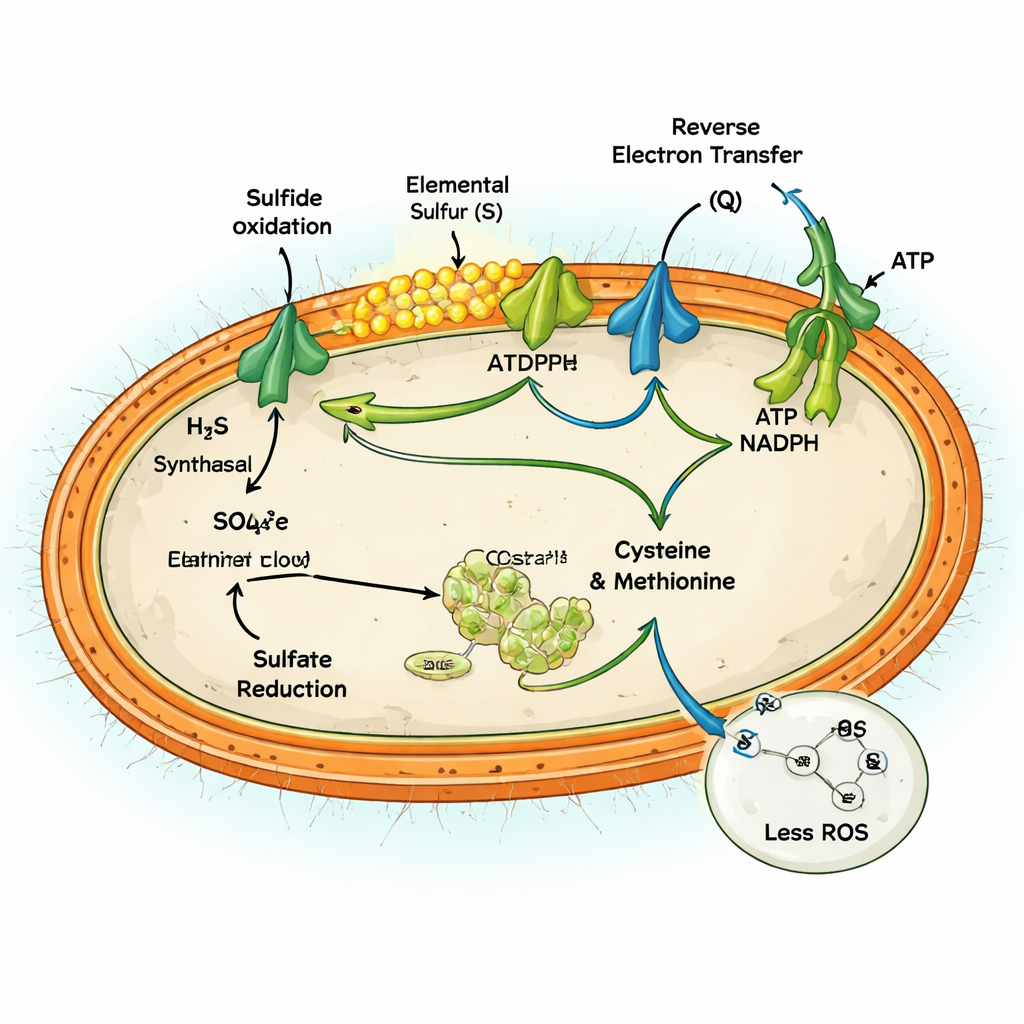
De gás tóxico a produtos úteis
Nas fases posteriores de operação do reator, quando MAG‑M116 dominava, quase todo o sulfeto de hidrogênio de entrada foi convertido em enxofre elementar sólido, em vez de sulfato. Ao mesmo tempo, os pesquisadores detectaram níveis crescentes de cisteína e metionina na fase líquida, sugerindo que o micróbio liberava aminoácidos ricos em enxofre em excesso para o ambiente. Essa combinação—enxofre elementar estável mais compostos orgânicos de enxofre valiosos—transforma um poluente perigoso em uma mistura de produtos recuperáveis com aplicações na agricultura, em materiais e em sistemas energéticos.
O que isso significa para saúde e tecnologia
Para um leitor não especializado, a mensagem principal é que este Mycobacterium resolveu um duplo problema: ele consegue limpar altos níveis de um gás tóxico enquanto mantém seu próprio equilíbrio químico interno. Faz isso executando reações de enxofre “push–pull” que normalmente seriam mantidas separadas, usando o ciclo supostamente desperdiçador como um amortecedor integrado para elétrons em excesso e radicais de oxigênio prejudiciais. Essa descoberta não só sugere novas maneiras de projetar biorreatores robustos e de baixo pH para remoção de sulfeto e sulfato, como também insinua que micróbios relacionados, incluindo espécies de Mycobacterium causadoras de doenças, podem usar truques semelhantes para sobreviver a ataques oxidativos dentro do corpo humano.
Citação: Jia, T., Peng, Y., Niu, L. et al. Simultaneous sulfide oxidation and sulfate reduction for intracellular redox homeostasis under highly acidic conditions. Nat Commun 17, 1797 (2026). https://doi.org/10.1038/s41467-026-68508-y
Palavras-chave: ciclo do enxofre, sulfeto de hidrogênio, Mycobacterium, homeostase redox, biodesulfurização