Clear Sky Science · pt
Uma célula artificial capaz de transdução de sinal mediada por ADRB2 para a regulação da glicogenólise
Ensinando Pequenas Bolhas a Falar
Imagine uma bolha de sabão microscópica que pode detectar um sinal similar a um hormônio no exterior e então “decidir” queimar combustível armazenado no interior, tal como uma célula humana real. Este estudo constrói exatamente esse tipo de célula artificial, mostrando como modelos celulares criados pelo homem podem receber uma mensagem química e convertê‑la em química controlada relacionada à energia. Esse trabalho nos aproxima de transportadores inteligentes de fármacos, tecidos fabricados em laboratório e formas de vida sintéticas simples que podem reagir ao seu ambiente.
Construindo uma Célula de Fora para Dentro
Células reais estão constantemente atentas ao ambiente por meio de receptores na sua membrana externa. Os autores propuseram reproduzir uma dessas vias naturais usando apenas componentes purificados e bolhas lipídicas simples, chamadas vesículas gigantes. Eles focaram em um receptor humano comum, o receptor β2‑adrenergico (ADRB2), que em nossos corpos ajuda a controlar a frequência cardíaca, a função pulmonar e o uso de combustível. Quando esse receptor encontra um fármaco como isoproterenol (ISO), ele normalmente desencadeia uma cadeia interna de eventos que produz uma molécula mensageira chamada cAMP, que por sua vez regula como as células degradam o glicogênio, a forma de reserva de glicose do corpo. Reproduzir toda essa sequência em uma célula artificial não havia sido alcançado antes.
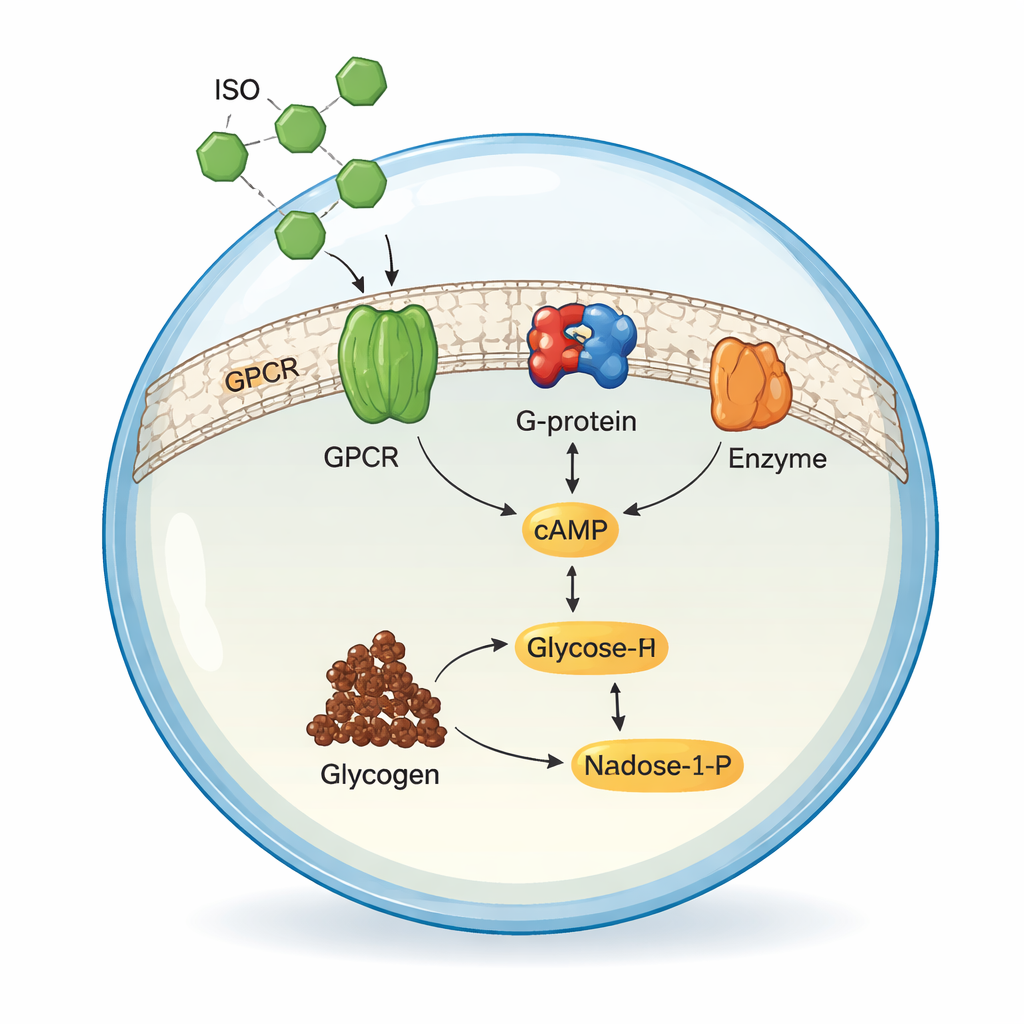
Recriando o Primeiro Repasse de Sinal
A equipe primeiro reconstruiu os estágios iniciais da via de sinalização em solução, fora de qualquer membrana. Eles produziram três proteínas humanas em células de inseto: ADRB2, sua subunidade parceira de proteína G (Gsα) e uma enzima chamada adenilato ciclase V (ADCY5), que sintetiza cAMP a partir de ATP. Quando misturaram essas partes com ISO sob condições cuidadosamente ajustadas, a ativação do receptor adrenérgico levou a ADCY5 a converter ATP em cAMP. Medindo cAMP por cromatografia líquida de alta performance, os pesquisadores otimizaram pH, temperatura e níveis de magnésio e descobriram que seu sistema reconstituído funcionava tão eficientemente quanto — ou melhor do que — muitas preparações anteriores, confirmando que a química central da sinalização estava em vigor.
Instalando Receptores Reais em Membranas Artificiais
Em seguida, os autores incorporaram as três proteínas nas membranas de vesículas unilamelares gigantes — bolhas lipídicas do tamanho de células que servem de chassi para células artificiais. Eles marcaram ADRB2 e ADCY5 com fluorescência para verificar que as proteínas se posicionavam na membrana, moviam‑se livremente e estavam presentes em grande número, com aproximadamente 1,8 milhão de receptores por vesícula. Tratamento enzimático mostrou que mais de 94% desses receptores estavam orientados corretamente, com seus sítios de ligação expostos para o exterior. Uma sonda fluorescente de GTP confirmou que a ligação de ISO na membrana realmente ativava proteínas G dentro das vesículas. Isso significava que, em princípio, as células artificiais podiam transmitir um sinal externo de ISO através de sua membrana exatamente como as células naturais.
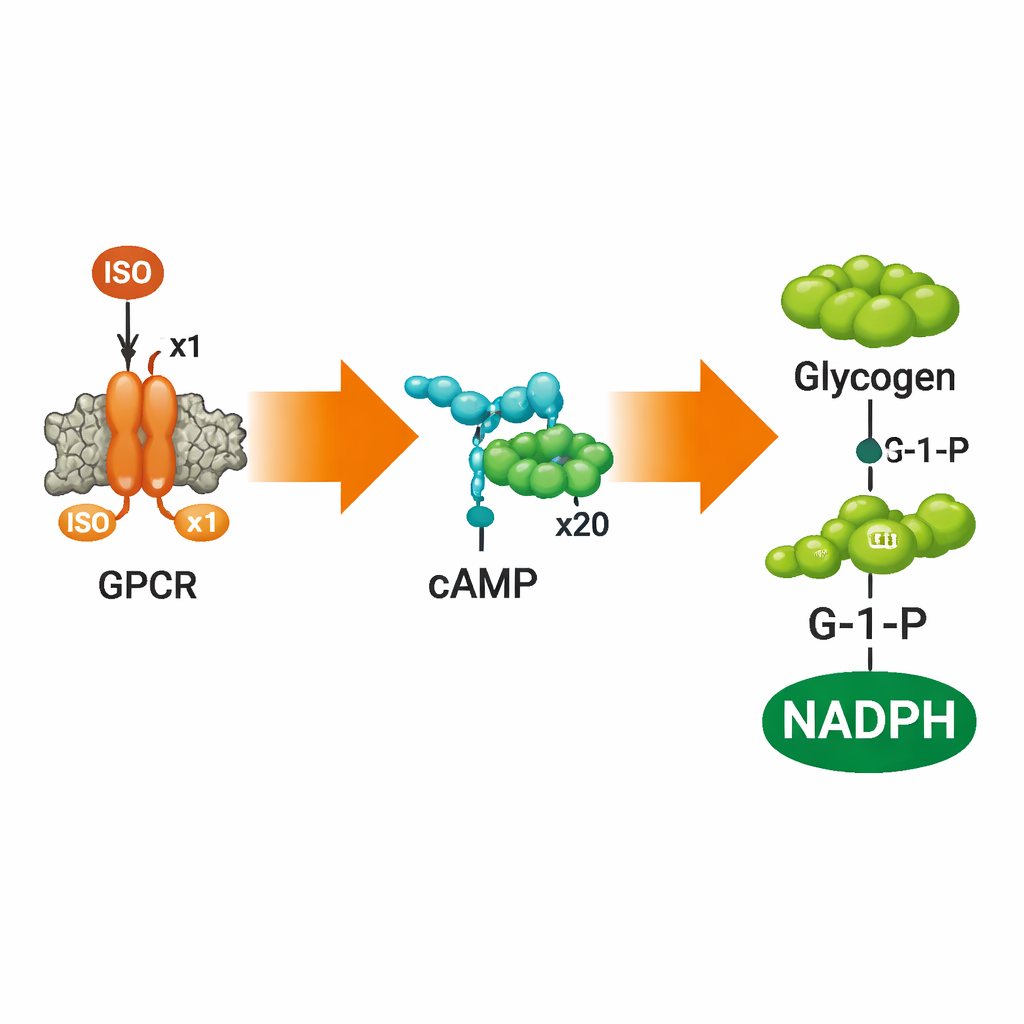
Convertendo Sinais em Quebra de Combustível
Para verificar se essas células sintéticas poderiam fazer algo útil com o sinal, a equipe adicionou um sensor de cAMP e depois uma via completa de degradação de glicogênio dentro das vesículas. Usando uma sonda de cAMP baseada em FRET, mostraram que a adição de ISO fora das vesículas fez com que os níveis de cAMP subissem no interior de forma dependente da dose e depois se estabilizassem conforme os receptores saturavam, espelhando o comportamento clássico de receptores acoplados à proteína G naturais. Fármacos que bloqueiam ou silenciam ADRB2 — alprenolol e carazolol — apagaram essa resposta exatamente como esperado. Quando os autores também encapsularam cinco enzimas que normalmente convertem glicogênio em glicose‑1‑fosfato (G‑1‑P) e então em NADPH, a estimulação por ISO levou à produção mensurável tanto de G‑1‑P quanto de NADPH dentro das células artificiais, monitorada por espectrometria de massa, cromatografia e fluorescência.
Ampliando um Sussurro em um Grito
Uma descoberta chave é o quão fortemente a resposta interna foi amplificada. Uma quantidade modesta de ISO fora das vesículas produziu aproximadamente 22 vezes mais moléculas de cAMP do que havia moléculas de ISO, e essa amplificação cresceu ainda mais ao longo da via. Quando o sinal conduziu a degradação do glicogênio e sua conversão em 6‑fosfogluconolactona acompanhada de NADPH, a amplificação total excedeu cem vezes. Esse impulso por etapas é uma característica de sinalização hormonal natural e mostra que o sistema artificial faz mais do que apenas detectar ISO — ele processa e amplifica a mensagem em uma resposta metabólica robusta.
Por Que Isso Importa para a Vida Sintética Futura
Para um não especialista, os detalhes técnicos se reduzem a uma ideia simples: os pesquisadores ensinaram uma célula mínima feita pelo homem a escutar e reagir como uma célula viva. Uma molécula externa de fármaco se ancora em um receptor humano realista, um sinal é passado através de uma membrana sintética e uma rede enzimática interna responde mobilizando energia química armazenada. Demonstrar essa cadeia completa — da ativação do receptor ao metabolismo controlado — em um sistema artificial simplificado é um passo importante rumo a células sintéticas autônomas que podem sentir, decidir e agir de maneiras úteis, como ajustar seu próprio suprimento de energia ou liberar terapias somente quando detectarem os sinais químicos corretos.
Citação: Liu, Y., Zhao, W., Zhao, Y. et al. An artificial cell capable of signal transduction mediated by ADRB2 for the regulation of glycogenolysis. Nat Commun 17, 1795 (2026). https://doi.org/10.1038/s41467-026-68503-3
Palavras-chave: células artificiais, transdução de sinal, GPCR, glicogenólise, biologia sintética