Clear Sky Science · pt
Liberação de fármacos controlada espaço-temporalmente via um sistema click-release utilizando mono-alquil-hidroxilamina e quimístria de ciclooctino
Ativando medicamentos potentes apenas onde são necessários
Muitos fármacos modernos são extremamente potentes, o que é vantajoso para combater o câncer ou aliviar a dor — mas arriscado para o resto do corpo. Este estudo descreve um “interruptor” químico que permite aos cientistas manter medicamentos em uma forma inativa e inofensiva e então ativá‑los somente em um local e momento escolhidos, como dentro de um tumor ou em uma pequena área que precise de anestesia local.
Um novo tipo de interruptor químico
Os pesquisadores se baseiam no conceito de “química click”, uma família de reações valorizada por ser rápida, precisa e compatível com ambientes biológicos. Reações click clássicas unem duas moléculas permanentemente. Aqui, a equipe inverte essa lógica: a reação click deles está diretamente ligada à quebra de uma ligação e ao liberamento de um fármaco ou molécula sinalizadora. Os protagonistas são uma molécula em anel chamada ciclooctino e um pequeno parceiro chamado mono‑alquil‑hidroxilamina. Quando esses dois se encontram, eles se unem rapidamente e então se rearranjam de modo que um “carga” ligada é liberada. Ao prender diferentes fármacos ou corantes fluorescentes como carga, a mesma reação básica pode ser reutilizada para várias finalidades. 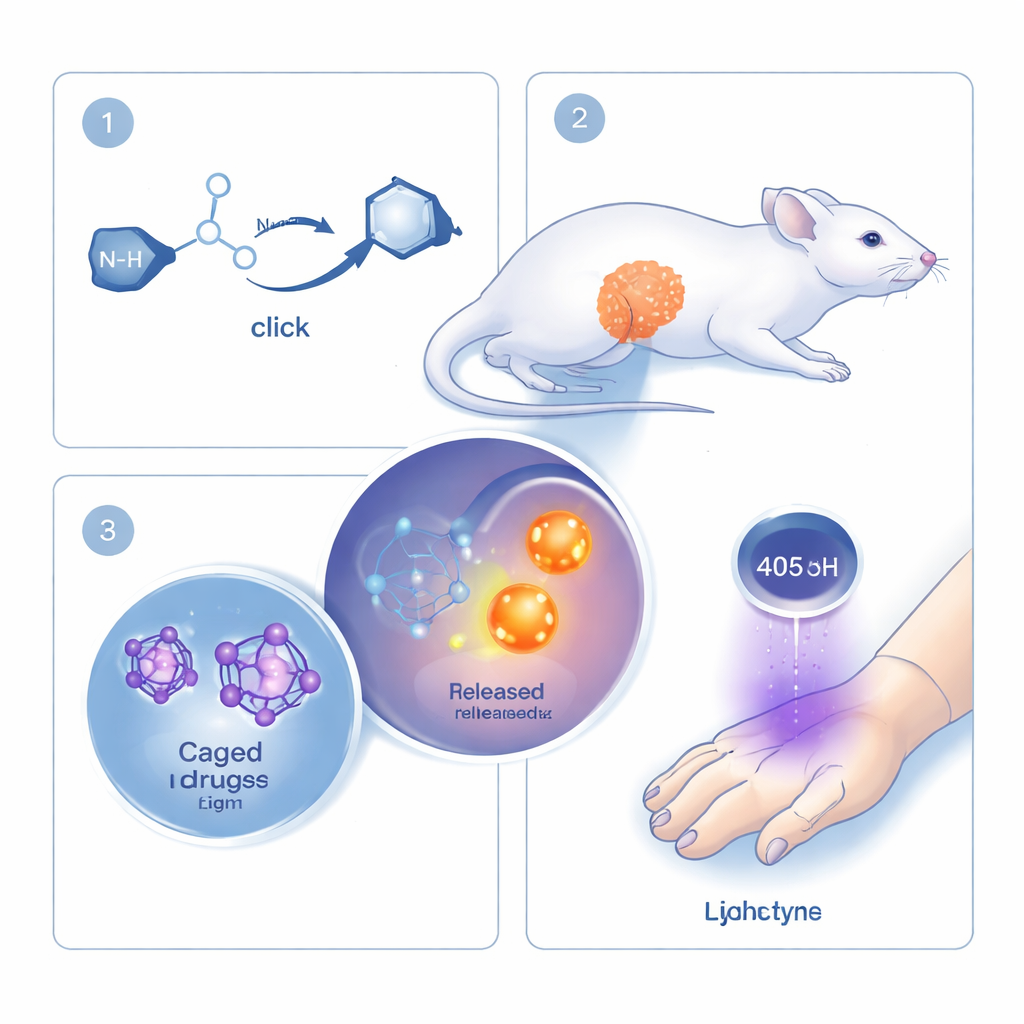
Liberação rápida e limpa dentro e fora das células
Para garantir que esse interruptor seria prático, a equipe mediu a rapidez da reação e o quão completamente ela libera a carga ligada. Eles descobriram que mono‑alquil‑hidroxilaminas cuidadosamente escolhidas reagem muito mais rápido do que hidroxilamina simples, atingindo conversão quase completa em minutos a horas, dependendo da estrutura. Importante, as etapas químicas que efetivamente liberam a carga são tão rápidas e seletivas que quase toda a molécula ligada é liberada, com pouquíssimos subprodutos. Os autores testaram uma variedade de cargas, incluindo corantes fluorescentes e até um íon fluoreto, e mostraram que o sistema pode quebrar vários tipos comuns de ligações usados em desenho de fármacos, como carbamatos e éteres.
Iluminando células e ativando fármacos contra o câncer sob demanda
Em seguida, os pesquisadores avançaram para células vivas. Primeiro esconderam corantes fluorescentes brilhantes atrás do interruptor químico e adicionaram essas sondas “encapsuladas” a células cancerígenas. Sozinhas, as sondas permaneceram escuras, indicando que as células não as ativaram acidentalmente. Quando o parceiro mono‑alquil‑hidroxilamina foi adicionado, os corantes foram liberados e as células se iluminaram em cores azul, verde ou próximo‑infravermelho, confirmando que a reação funciona de forma confiável em ambiente biológico. Aplicaram depois a mesma ideia ao doxorrubicina, um quimioterápico amplamente usado. Em sua forma encapsulada, o pró‑fármaco de doxorrubicina foi muito menos tóxico para as células. Mas quando o parceiro click estava presente, o fármaco ativo foi liberado eficientemente, restaurando sua capacidade de matar células cancerígenas quase com a mesma força da doxorrubicina livre.
Construindo gatilhos inteligentes para lugar e momento
Uma limitação de muitos sistemas click existentes é que as partes reativas estão sempre “ligadas”, dificultando o controle exato de onde e quando atuam. Para resolver isso, a equipe bloqueou temporariamente a reatividade da mono‑alquil‑hidroxilamina com pequenas tampas protetoras que só são removidas por gatilhos específicos. Eles criaram versões que respondem a altos níveis de glutationa (uma pequena molécula abundante em muitos tumores), a enzimas e a flashes de luz violeta. Em células e em camundongos com tumores, a versão responsiva à glutationa permaneceu silenciosa em condições normais, mas ligou‑se no ambiente quimicamente redutor do tumor, liberando corantes fluorescentes ou ativando o pró‑fármaco de doxorrubicina exatamente onde o câncer crescia. Camundongos tratados com a combinação pró‑fármaco mais gatilho mostraram maior encolhimento tumoral do que aqueles recebendo doxorrubicina padrão, enquanto experimentaram menor exposição ao fármaco em órgãos sensíveis como o coração.
Anestesia local controlada remotamente por luz
Para demonstrar o controle temporal, os autores desenvolveram uma segunda aplicação: anestesia local guiada por luz. Eles prenderam o anestésico tetracaína ao arcabouço de ciclooctino, tornando‑o inativo, e misturaram esse pró‑fármaco com uma versão foto‑sensível da hidroxilamina em um gel termo‑responsivo. Injetada na pata de um rato, a mistura não produziu efeito até que a pele fosse iluminada com luz de 405 nanômetros. A iluminação acionou a reação click‑release, liberando a tetracaína e produzindo entorpecimento comparável ao da injeção direta de tetracaína. Ao variar a duração e a intensidade da luz, os pesquisadores puderam ajustar quanto tempo durou o bloqueio nervoso, e foram capazes até de desencadear ondas repetidas de anestesia a partir de uma única injeção. 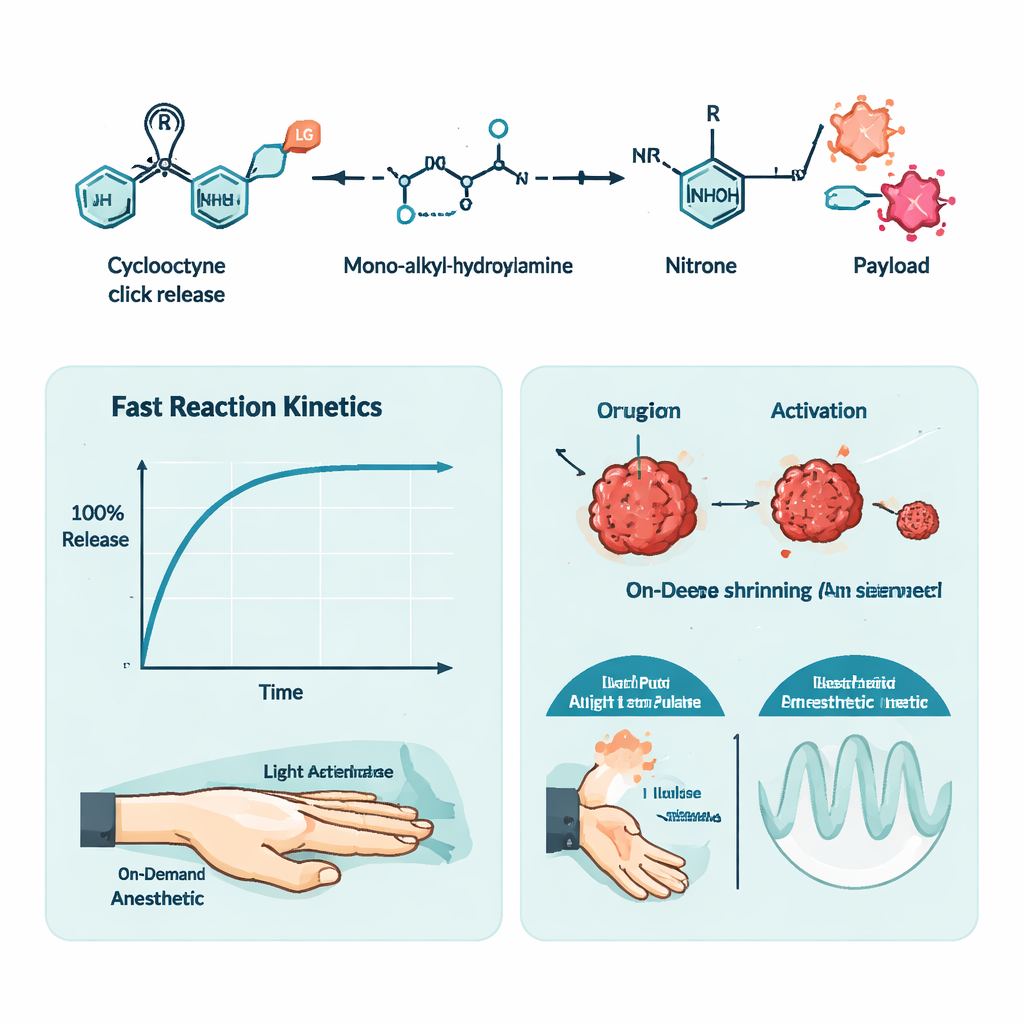
O que isso pode significar para tratamentos futuros
Para não especialistas, a mensagem principal é que este trabalho oferece um controle químico remoto flexível para medicamentos: os fármacos podem ser entregues em uma forma segura e silenciosa e então ativados apenas no local e momento corretos, usando sinais originados no próprio corpo ou de uma fonte de luz externa. Embora sejam necessários mais testes antes do uso clínico, a abordagem pode, no futuro, tornar tratamentos contra o câncer mais direcionados e menos tóxicos, permitir controle personalizável da dor após cirurgia e apoiar uma gama de outras terapias que se beneficiam de controle espaço‑temporal preciso.
Citação: Xu, X., Tong, X., Shi, Y. et al. Spatiotemporally controlled drug release via a click-release system utilizing mono-alkyl-hydroxylamine and cyclooctyne chemistry. Nat Commun 17, 1794 (2026). https://doi.org/10.1038/s41467-026-68502-4
Palavras-chave: química click, liberação direcionada de fármacos, pró-fármacos, microambiente tumoral, anestesia foto-controlada