Clear Sky Science · pt
Eletrossíntese seletiva de ureia a partir de nitrato e dióxido de carbono com baixo sobretensão
Transformando Resíduos em Fertilizante
A agricultura moderna depende fortemente do fertilizante ureia, mas sua produção convencional consome grande quantidade de combustíveis fósseis e libera muito dióxido de carbono. Este estudo explora uma rota mais limpa: usar eletricidade e materiais projetados para converter diretamente dióxido de carbono e nitrato — ambos poluentes comuns — em ureia sob condições brandas. Se escalado, esse processo poderia ajudar a alimentar a população ao mesmo tempo em que reduz as emissões de gases de efeito estufa e aproveita melhor correntes de resíduos.
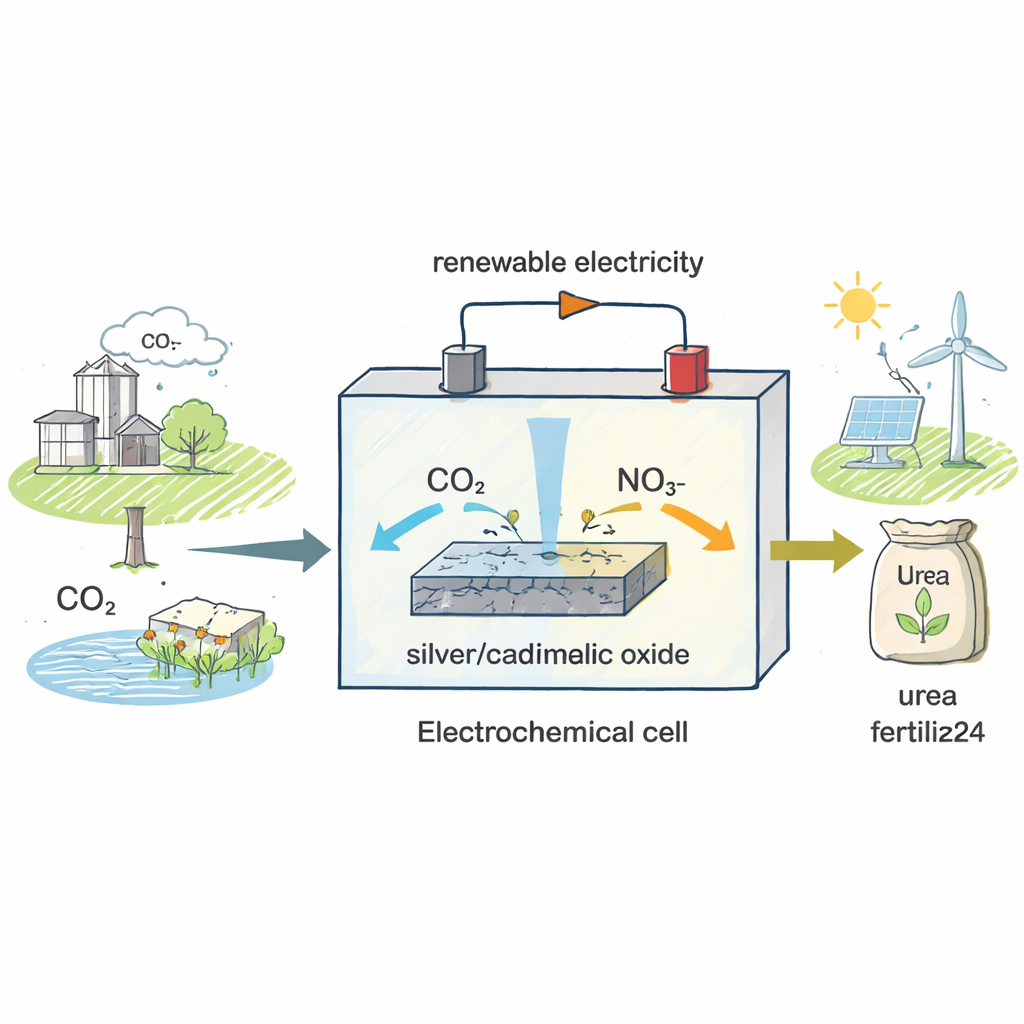
Uma Nova Forma de Produzir um Fertilizante Antigo
As fábricas de ureia atuais operam em altas temperaturas e pressões e dependem de amônia produzida a partir do gás nitrogênio, etapa que por si só consome mais de 2% da energia global. Os autores buscaram contornar essa rota intensiva em energia. Em vez de partir do gás nitrogênio, eles usam nitrato, um composto nitrogenado presente em escoamentos agrícolas e águas residuais industriais, e o combinam com dióxido de carbono, o principal gás de efeito estufa. Ambas as substâncias são alimentadas em uma célula eletroquímica — um dispositivo onde a eletricidade impulsiona reações químicas — de modo que, com o catalisador adequado, podem ser costuradas em ureia à temperatura ambiente e tensões relativamente baixas.
Projetando uma Superfície Útil
O coração do dispositivo é um catalisador sólido feito de partículas minúsculas que combinam prata (Ag) com óxido de cádmio (CdO). Microscopia e técnicas de raios X mostram que essas partículas formam “heteroestruturas” íntimas, onde a prata metálica e o CdO se tocam na escala nanométrica e trocam elétrons. Essa interação eletrônica altera sutilmente como cada componente liga as moléculas entrantes. Em condições de operação, a porção de CdO se transforma em carbonato de cádmio (CdCO₃) que contém átomos de oxigênio ausentes, conhecidos como vacâncias de oxigênio. Esses locais vagos atuam como pequenos pontos de ancoragem que ajudam a capturar e ativar o dióxido de carbono, enquanto as regiões vizinhas de prata são especialmente eficientes em capturar espécies contendo nitrogênio derivadas do nitrato.
Produzindo Ureia com Eficiência e Seletividade
Quando dióxido de carbono e nitrato fluem através desse catalisador Ag/CdO em uma célula em escala de laboratório, o material os converte em ureia com uma “sobretensão” incomumente baixa, ou seja, a voltagem extra além do requisito termodinâmico ideal é pequena. Em uma célula em forma de H simples, a composição otimizada, chamada Ag₀.₀₇/CdO, atinge uma seletividade para ureia de cerca de 50% a apenas −0,10 volts em relação a uma referência padrão, produzindo pouca amônia ou monóxido de carbono como subprodutos. Em uma célula de fluxo mais avançada, onde gases e líquidos são supridos continuamente, o mesmo catalisador alcança uma alta taxa de produção de ureia de aproximadamente 112 milimoles por grama de catalisador por hora a −0,15 volts. Ao otimizar ainda mais o projeto do reator e as condições operacionais, a equipe eleva a taxa de produção de ureia para cerca de 427 milimoles por grama por hora em correntes mais altas, mantendo o desempenho por 1.000 horas de operação contínua — um indicador importante de estabilidade.
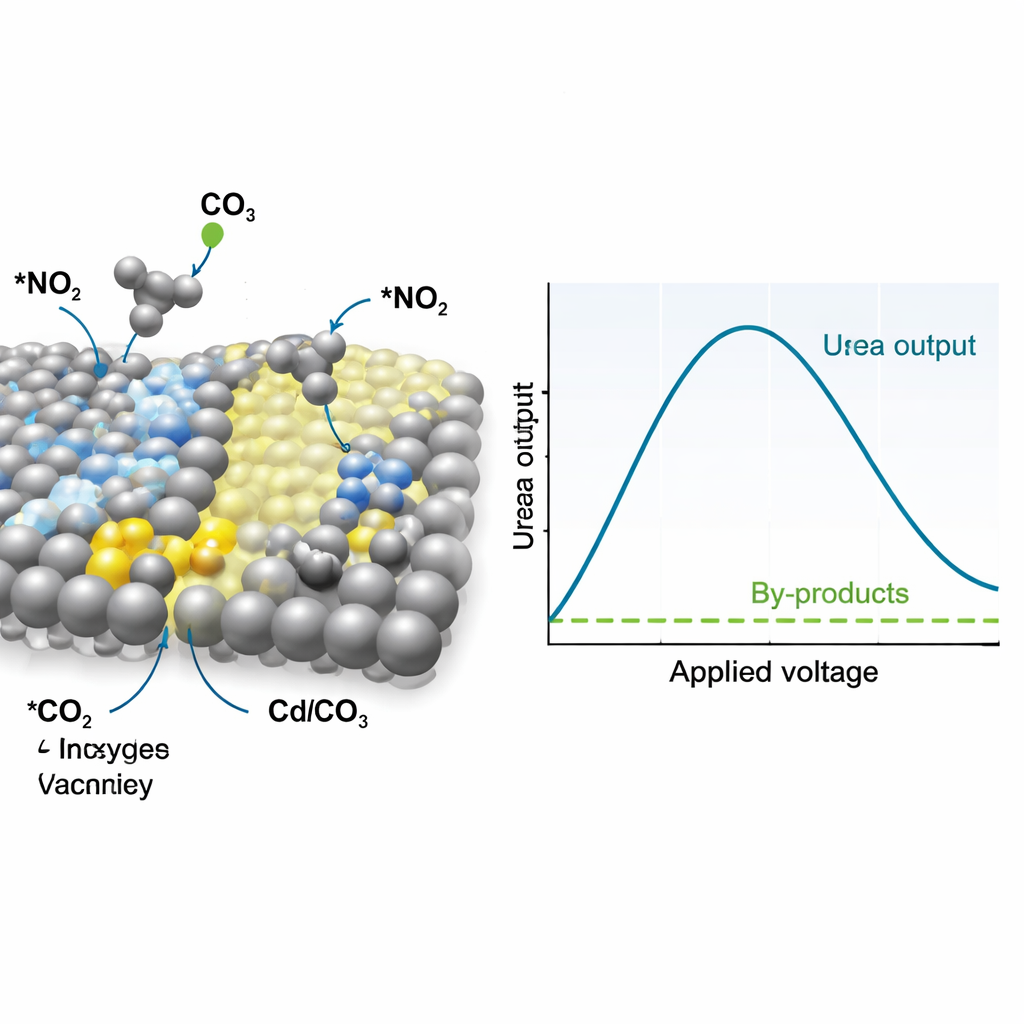
Como o Catalisador Direciona a Reação
Para entender por que esse material funciona tão bem, os pesquisadores acompanharam o catalisador e os intermediários de reação em tempo real usando espectroscopia Raman e infravermelha, junto com sondas avançadas de raios X. Essas medições indicam que os sítios de prata convertem preferencialmente o nitrato em um intermediário reativo frequentemente descrito como *NO₂, enquanto o CdCO₃ reconstruído com vacâncias de oxigênio liga o dióxido de carbono e o transforma em *CO, outro intermediário de curta duração. Sinais associados a ligações carbono–nitrogênio aparecem nas tensões de operação, mostrando que *NO₂ e *CO se acoplam cedo no processo para formar uma espécie semelhante à ureia, em vez de se desviarem para formar amônia ou monóxido de carbono separadamente. Simulações computacionais suportam essa imagem, revelando que a interface entre a prata e o CdCO₃ rico em vacâncias reduz a barreira de energia para essa etapa chave de acoplamento C–N e a torna mais favorável do que reações concorrentes.
O Que Isso Pode Significar para Fertilizantes e Clima
No conjunto, o trabalho demonstra que superfícies de catalisadores cuidadosamente projetadas podem guiar moléculas simples de resíduos, como dióxido de carbono e nitrato, ao longo de uma via energeticamente eficiente para ureia, sob condições brandas e com longa durabilidade. Para um público não especializado, a conclusão principal é que a equipe construiu uma espécie de “filtro eletrônico” que prefere unir carbono e nitrogênio em ureia em vez de deixá-los escapar como outros produtos. Embora a implantação em escala real exija enfrentar questões como custo dos materiais, engenharia do reator e o manejo seguro do cádmio, o estudo oferece um roteiro para a produção futura de fertilizantes que poderia ser alimentada por eletricidade renovável e alinhada com um ciclo de carbono e nitrogênio mais sustentável.
Citação: Liu, S., Wang, T., Liu, J. et al. Selective electrosynthesis of urea from nitrate and carbon dioxide with low overpotential. Nat Commun 17, 1787 (2026). https://doi.org/10.1038/s41467-026-68497-y
Palavras-chave: eletrossíntese de ureia, utilização de dióxido de carbono, redução de nitrato, projeto de eletrocatalisador, fertilizante verde