Clear Sky Science · pt
Alvo na cascata UFL1-AKT suprime a progressão do câncer de mama triplo negativo
Por que esta pesquisa importa
O câncer de mama triplo negativo (TNBC) é uma das formas mais letais de câncer de mama porque carece dos interruptores hormonais e de fator de crescimento que muitos medicamentos modernos visam. Pacientes frequentemente recebem apenas quimioterapia tradicional, que pode deixar de funcionar à medida que os tumores desenvolvem resistência. Este estudo revela um “motor” molecular até agora oculto que ajuda células de TNBC a crescer e a resistir à quimioterapia, e propõe um novo tipo de fármaco que bloqueia esse motor diretamente.
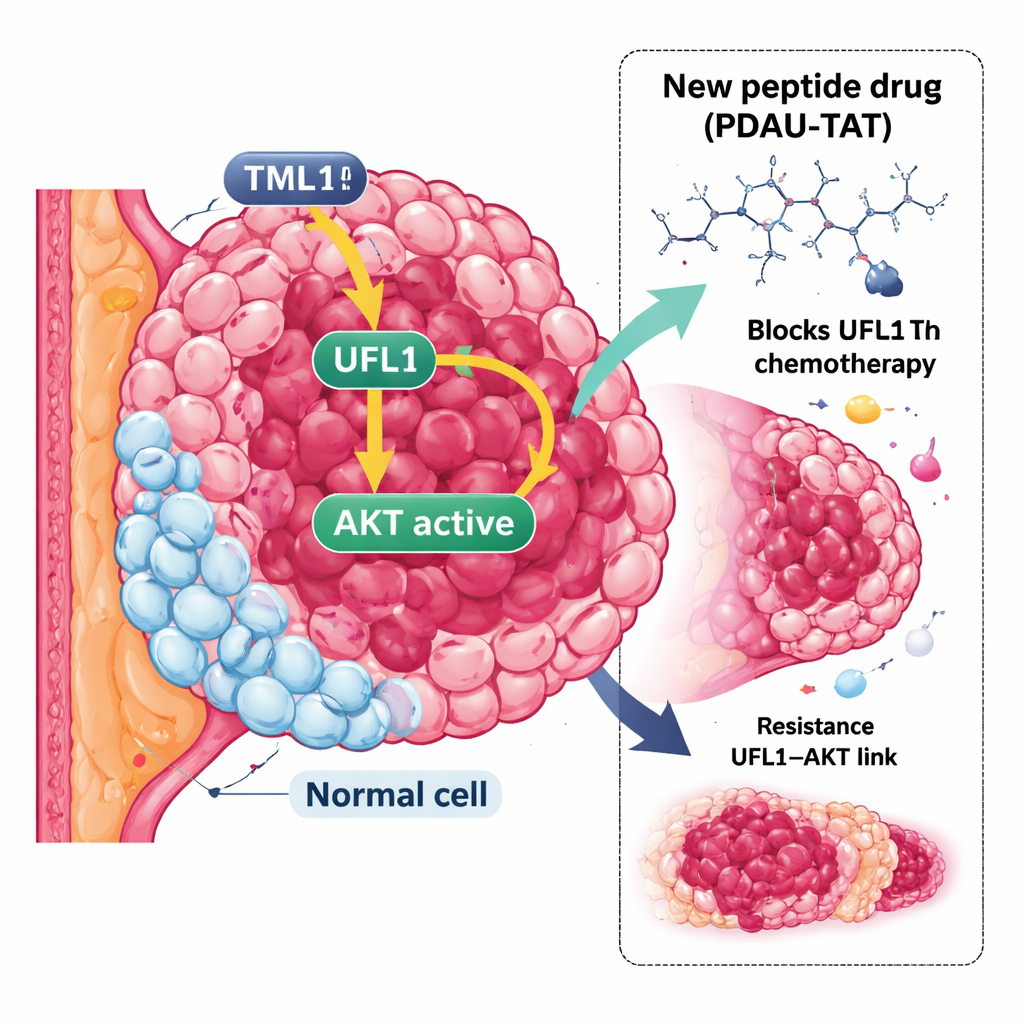
Uma forma persistente de câncer de mama
O TNBC é definido pela ausência de três marcadores comuns: o receptor de estrogênio, o receptor de progesterona e o receptor de crescimento HER2. Sem esses marcadores, muitas terapias alvo bem-sucedidas simplesmente não se aplicam. Fármacos padrão, como cisplatina e doxorrubicina, são usados em seu lugar, mas tumores de TNBC frequentemente desenvolvem resistência ou se adaptam rapidamente a esses tratamentos e têm maior propensão a se disseminar. Isso cria uma necessidade urgente de estratégias novas que vão além dos alvos habituais e procurem outras vulnerabilidades nos sistemas de controle do tumor.
Uma proteína pouco conhecida com grande impacto
Os pesquisadores se concentraram na UFL1, uma proteína que anexa uma pequena etiqueta chamada UFM1 a outras proteínas em um processo conhecido como UFMilação. Esse sistema de marcação foi descoberto recentemente, e seu papel no câncer tem sido incerto e às vezes até contraditório. Ao analisar dados de pacientes e amostras de tumores, a equipe mostrou que a UFL1 está marcadamente elevada no TNBC em comparação com o tecido mamário normal. Quando reduziram os níveis de UFL1 em linhagens celulares de TNBC e em modelos tumorais em camundongos, as células cancerosas se multiplicaram mais lentamente e ficaram muito mais sensíveis à quimioterapia, sugerindo que a UFL1 desempenha um papel promotor de tumor nesse contexto.
Conectando a UFL1 a um interruptor mestre de crescimento
Ao aprofundar, os cientistas descobriram que a UFL1 se liga diretamente à AKT, uma proteína central de sinalização que impulsiona o crescimento, a sobrevivência e o metabolismo celular e frequentemente está hiperativa em cânceres. No TNBC, a AKT é frequentemente superativa mesmo quando as mutações upstream usuais estão ausentes. A equipe constatou que a UFL1 marca quimicamente a AKT em três posições específicas, o que facilita sua ativação pelos parceiros ativadores, ao mesmo tempo que a protege de enzimas que normalmente a desligariam. Células sem UFL1 ou que expressavam uma forma modificada de AKT incapaz de receber essas marcações apresentaram atividade de AKT muito menor, crescimento mais lento e maior vulnerabilidade à quimioterapia tanto em culturas celulares quanto em modelos animais.
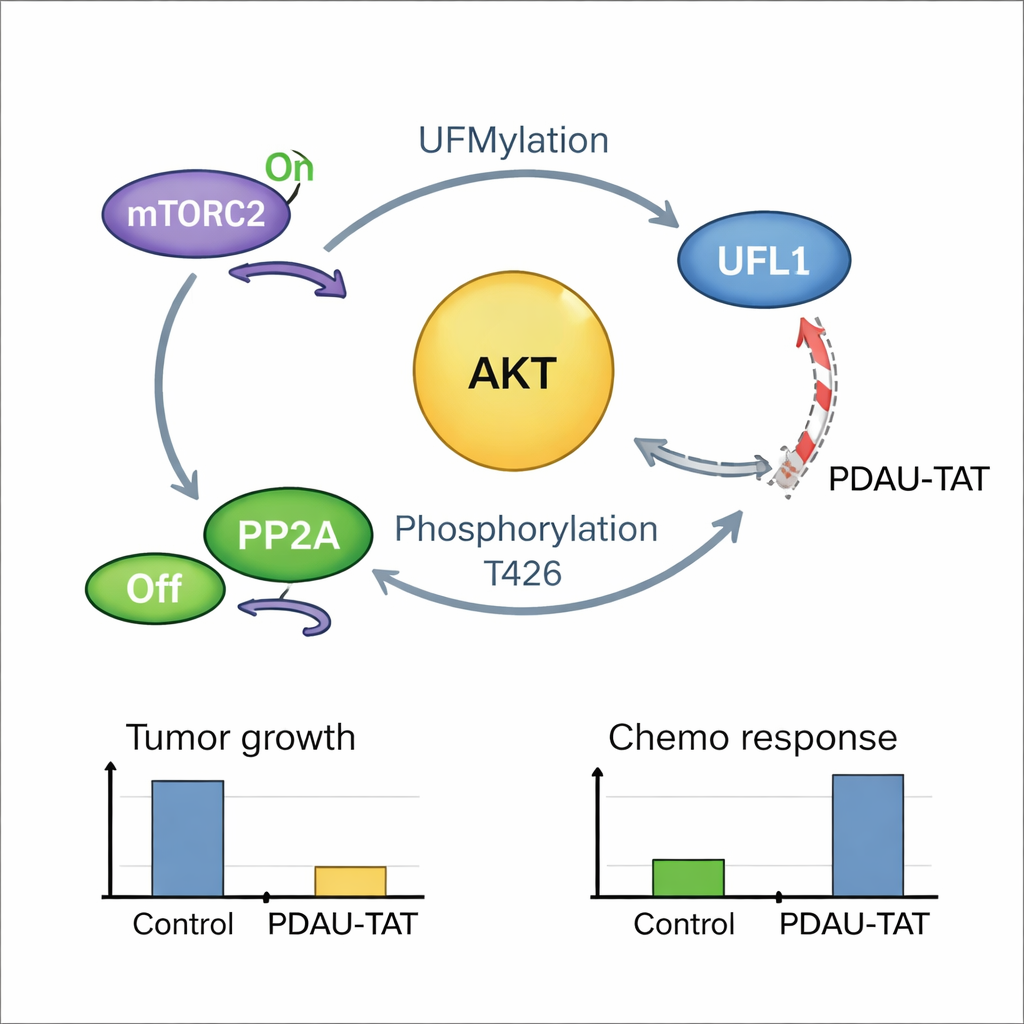
Um laço cancerígeno autorreforçador e uma forma de rompê‑lo
A história mostrou‑se ainda mais estreitamente ligada: uma vez ativada, a AKT retroalimenta e modifica a UFL1 em um sítio crucial, aumentando a atividade de marcação da UFL1 sobre a AKT e outros alvos. Isso cria um laço de feedback positivo em que a UFL1 ativa a AKT e a AKT ativa fortemente a UFL1. Amostras tumorais de pacientes mostraram que altos níveis de UFL1 modificada se correlacionam fortemente com altos níveis de AKT ativa, apoiando a existência desse laço na doença humana. Para explorar essa vulnerabilidade, a equipe desenhou um pequeno peptídeo penetrante em células, chamado PDAU‑TAT, que mimetiza uma pequena região da UFL1 e se encaixa entre a UFL1 e a AKT. Esse peptídeo interrompe a interação entre elas, reduz a ativação da AKT, retarda o crescimento tumoral e torna células de TNBC e tumores derivados de pacientes mais responsivos à quimioterapia, tudo sem dano aparente aos principais órgãos em camundongos.
O que isso pode significar para pacientes
Em termos simples, os pesquisadores descobriram um diagrama de fiação oculto dentro de células de TNBC: UFL1 e AKT estão presos em um ciclo de autoamplificação que mantém os sinais de crescimento na posição “ligada” e ajuda os tumores a resistir ao tratamento. Ao construir um pequeno peptídeo que se insere nesse ciclo e desconecta a UFL1 da AKT, eles mostram uma nova maneira plausível de enfraquecer tumores de TNBC enquanto preservam células normais, que tendem a ter níveis mais baixos de UFL1. Embora este trabalho ainda esteja em estágio pré‑clínico, ele aponta para uma nova classe de terapias direcionadas não aos receptores habituais, mas às conexões proteína–proteína que alimentam alguns dos cânceres de mama mais agressivos.
Citação: Yang, X., Wen, Y., Ma, X. et al. Targeting the UFL1-AKT cascade suppresses triple-negative breast cancer progression. Nat Commun 17, 613 (2026). https://doi.org/10.1038/s41467-026-68493-2
Palavras-chave: câncer de mama triplo negativo, sinalização AKT, UFMilação, UFL1, terapia peptídica contra o câncer