Clear Sky Science · pt
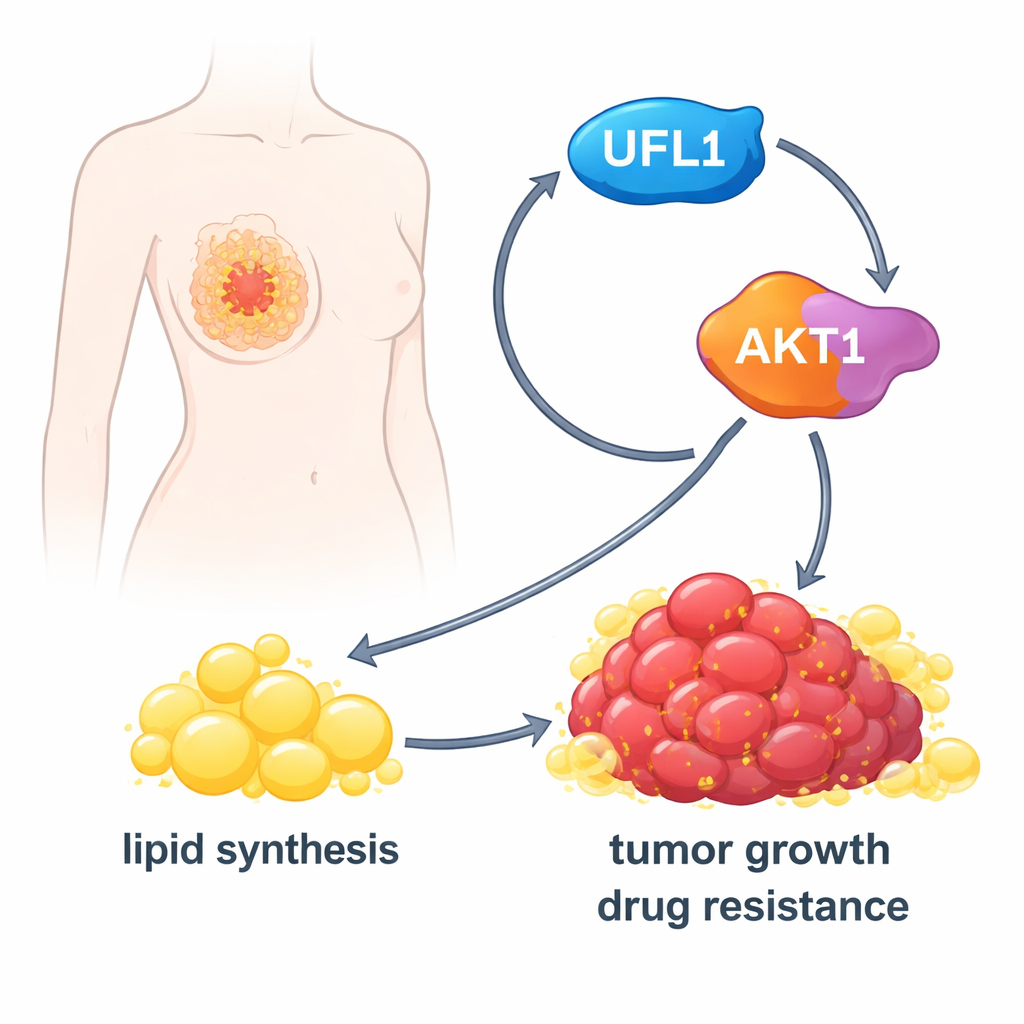
O ciclo de feedback positivo UFL1-AKT promove a progressão do câncer de mama ao aumentar a síntese lipídica
Por que as células cancerosas se importam tanto com gordura
As células de câncer de mama, como todas as células de crescimento rápido, precisam de um suprimento constante de blocos de construção para fabricar novas membranas e moléculas sinalizadoras. Gorduras, ou lipídios, são uma parte central desse suprimento. Este estudo revela como um sistema proteico pouco conhecido desloca as células cancerosas para um "modo de produção de gordura em excesso", ajudando os tumores a crescer e a escapar do tratamento. Entender essa linha de combustível oculta pode abrir novas vias para desacelerar ou privar os cânceres de mama.
Uma etiqueta proteica escondida com grandes consequências
Nossas células ajustam constantemente o comportamento de suas proteínas usando pequenas etiquetas químicas. Uma dessas etiquetas, chamada UFM1, é adicionada por uma enzima nomeada UFL1. A marcação por UFM1 (UFMilação) tem sido associada a reparo de DNA e respostas ao estresse, mas seu papel no câncer era incerto. Os autores mostram que a atividade de UFL1 é muito maior em tumores humanos de mama do que no tecido mamário normal, em todos os subtipos principais. Pacientes cujos tumores apresentam níveis mais altos de UFL1 tendem a ter pior sobrevida. Quando os pesquisadores reduziram UFL1 em células de câncer de mama ou em tumores de camundongos, o crescimento do câncer diminuiu, a divisão celular caiu e a morte celular aumentou, sugerindo que UFL1 se comporta como um fator que promove o câncer.
Como um centro de sinalização é convertido em modo de produção de gordura
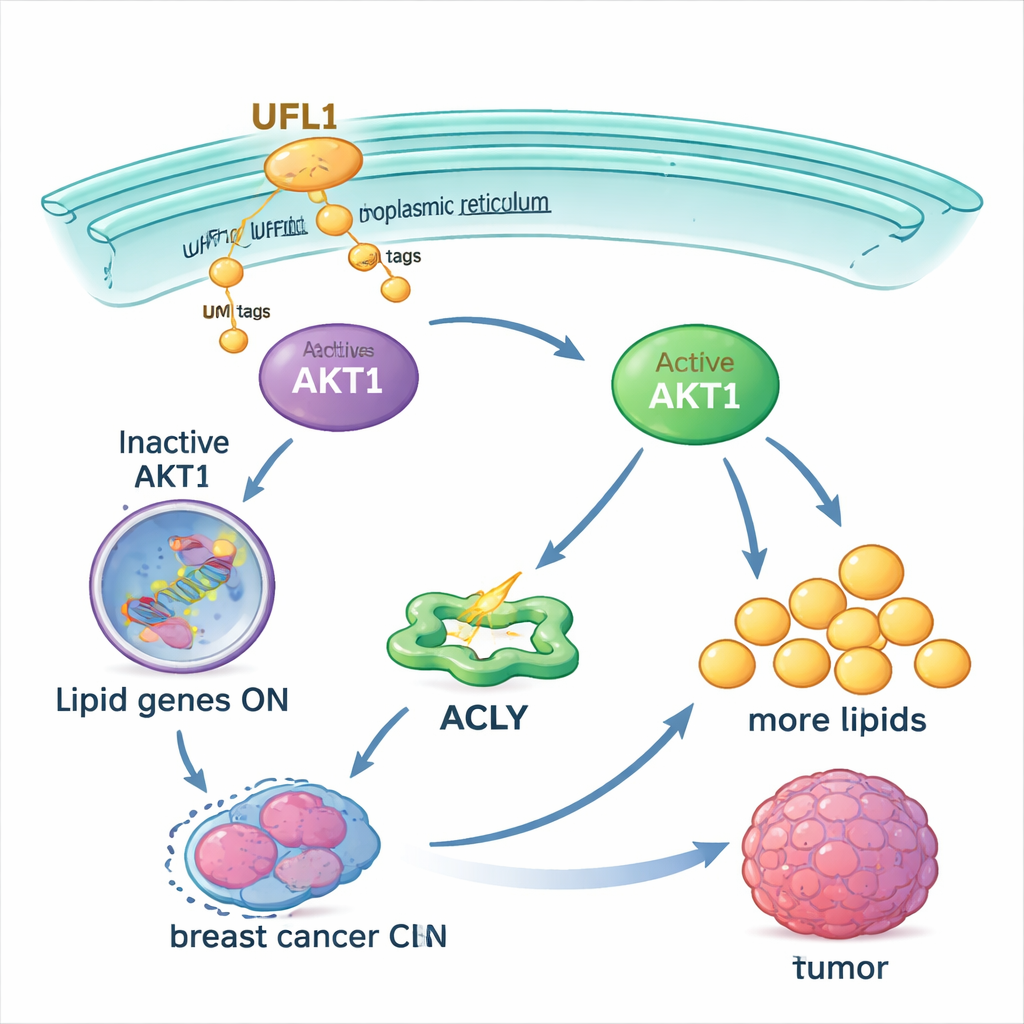
Para entender como UFL1 ajuda os tumores, a equipe procurou seus parceiros moleculares e encontrou uma proteína chave de controle de sinal chamada AKT1. AKT1 é um interruptor central que diz às células para crescer e produzir novos lipídios. O estudo mostra que UFL1 se liga fisicamente a AKT1 e o decora com etiquetas de UFM1 em vários pontos específicos. Essa marcação altera a conformação de AKT1, afrouxando um "freio" interno que normalmente o mantém inativo. Também ajuda AKT1 a se mover para um compartimento de membrana dentro da célula, o retículo endoplasmático, onde outras enzimas podem ativá‑lo totalmente adicionando grupos fosfato. Sem as etiquetas de UFM1 nesses locais, AKT1 é muito mais difícil de ativar.
Ligando a fábrica de gordura do câncer
Uma vez ativado, AKT1 impulsiona as células a aumentarem a produção de gordura. Ele eleva a atividade de uma enzima metabólica chave, ACLY, e aumenta os níveis de reguladores mestres como SREBP1 que ativam muitos genes de lipogênese. Em células de câncer de mama cultivadas em laboratório, UFL1 fez as células acumularem mais gotículas lipídicas, ácidos graxos livres e colesterol. A remoção de UFL1 reduziu fortemente essas reservas lipídicas, tanto em culturas quanto em tumores crescidos em camundongos. Fornecer ácidos graxos extras de fora da célula pôde em grande parte resgatar o crescimento de células cancerosas deficientes em UFL1, indicando que o efeito principal de UFL1 é garantir lipídios suficientes para sustentar a expansão tumoral.
Um ciclo autoamplificador que impulsiona o crescimento tumoral
Surpreendentemente, a relação entre UFL1 e AKT1 funciona nos dois sentidos. Os pesquisadores descobriram que, uma vez ativo, AKT1 por sua vez adiciona uma etiqueta fosfato em UFL1 em um sítio particular. Essa modificação aumenta ainda mais a capacidade de UFL1 de marcar AKT1 com UFM1, criando um laço de feedback positivo: UFL1 ativa AKT1, e AKT1 ativa UFL1. Mutar tanto os sítios de UFM1 em AKT1 quanto o sítio fosfato em UFL1 interrompe esse ciclo. Em camundongos, tumores que carregavam essas versões mutantes cresceram pouco, continham menos lipídios e mostraram mais células moribundas. Em amostras de pacientes com câncer de mama triplo‑negativo, níveis mais altos de UFL1 ativado e AKT1 ativado tendiam a aparecer juntos, destacando que esse ciclo opera em tumores reais.
Enfraquecendo o ciclo para ajudar os tratamentos a funcionarem
Como muitos ensaios clínicos já miram AKT, os autores testaram se bloquear a UFMilação poderia tornar esses tratamentos mais eficazes. Em células de câncer de mama, um inibidor de pequena molécula da UFMilação e um inibidor de AKT reduziram cada um a atividade de AKT1 e o acúmulo de lipídios, mas usados em combinação funcionaram muito melhor do que isoladamente. A combinação também retardou o crescimento tumoral e cortou o conteúdo lipídico em tumores de camundongos sem causar perda de peso perceptível nos animais. Bloquear a UFMilação tornou ainda as células cancerosas mais sensíveis a quimioterapias padrão, como cisplatina e etoposídeo, que frequentemente falham quando AKT está altamente ativo.
O que isso significa para os pacientes
Para um leitor leigo, o estudo mostra que certos cânceres de mama se conectam por um circuito auto‑reforçador que alimenta tanto seu crescimento quanto seu suprimento de gordura. UFL1 e AKT1 atuam juntos como dois pedais pressionados ao mesmo tempo: um marca, o outro sinaliza, e juntos dirigem a produção de lipídios e a expansão tumoral. Ao encontrar drogas que interfiram nesse ciclo — seja bloqueando a UFMilação, AKT1 ou a interação entre ambos — terapias futuras podem ser capazes de desacelerar o crescimento tumoral e tornar os tratamentos existentes mais eficazes, especialmente em tipos agressivos de câncer de mama.
Citação: Meng, F., Du, Y., Liang, J. et al. The UFL1-AKT positive feedback loop promotes breast cancer progression by enhancing lipid synthesis. Nat Commun 17, 614 (2026). https://doi.org/10.1038/s41467-026-68492-3
Palavras-chave: câncer de mama, metabolismo lipídico, sinalização AKT, UFMilação, terapia direcionada