Clear Sky Science · pt
Hidrogel de reservatório celular auto-montado in situ para manobrar radioimunoterapia em múltiplas etapas
Transformando a radiação em uma arma mais inteligente contra o câncer
A radioterapia é um dos tratamentos contra o câncer mais amplamente usados, mas os tumores frequentemente sobrevivem escondendo-se do sistema imunológico e crescendo em condições de baixo oxigênio (hipóxia) que atenuam o impacto da radiação. Este estudo descreve um “hidrogel inteligente” injetável que se forma diretamente dentro do tumor e funciona como uma pequena fábrica de fármacos e geradora de oxigênio. Ao fornecer tanto radiação quanto sinais imunostimuladores cuidadosamente temporizados ao tumor, o sistema busca transformar um câncer difícil de tratar em um alvo que as defesas do próprio corpo possam reconhecer e destruir.
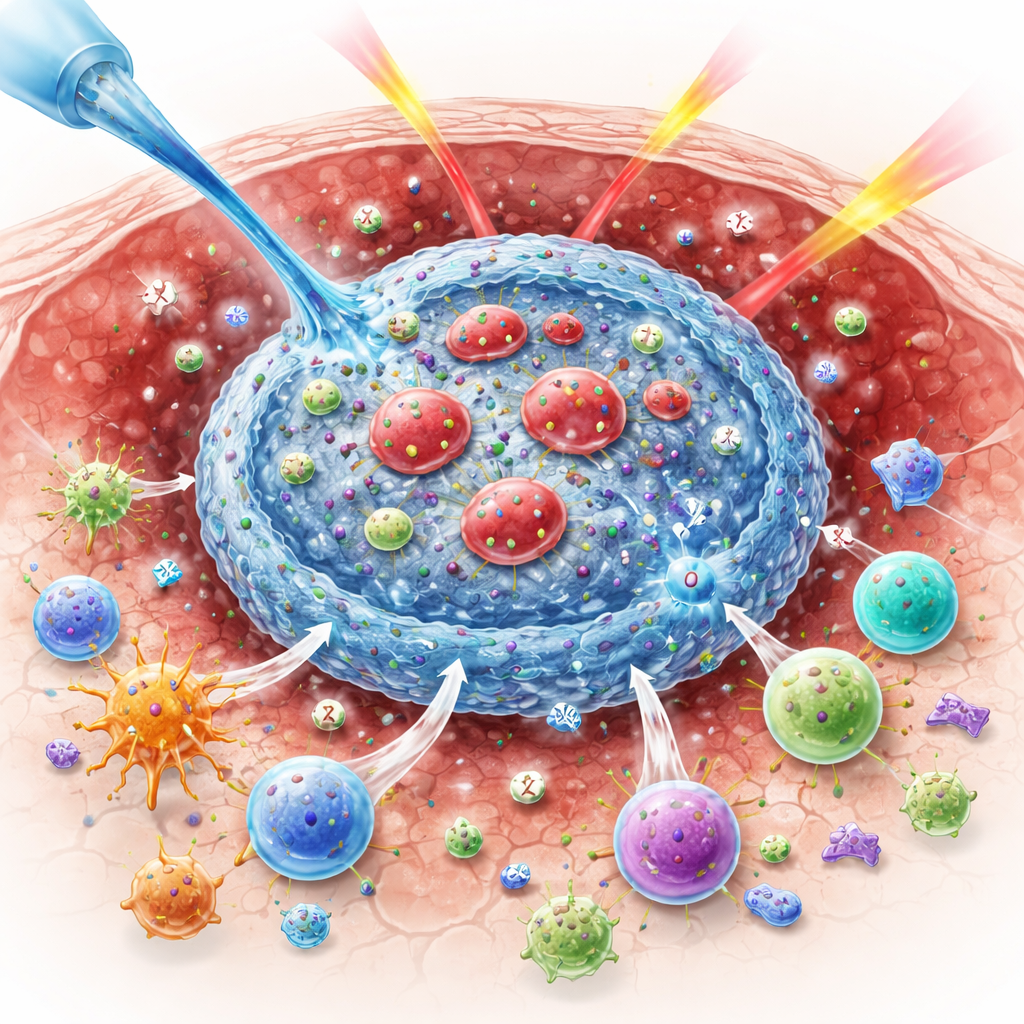
Por que o oxigênio importa para derrotar tumores
A radiação mata células cancerosas em parte gerando espécies de oxigênio altamente reativas que quebram o DNA. Quando os tumores são privados de oxigênio, essa química é menos eficaz, de modo que mais células cancerosas sobrevivem. Ao mesmo tempo, a radiação envia mensagens contraditórias ao sistema imunológico. Pode expor proteínas tumorais que marcam o câncer como perigoso, mas também pode aumentar “freios” nas células imunes, como a proteína de checkpoint CTLA-4, e favorecer células T reguladoras que suprimem o ataque. Esses efeitos opostos ajudam a explicar por que combinar radiação com drogas imunológicas nem sempre funcionou tão bem em pacientes quanto em camundongos.
Um gel vivo montado dentro do tumor
Os pesquisadores projetaram um material que se auto-monta apenas no ambiente ácido de um tumor. Ele é composto por três partes-chave: um polímero natural à base de açúcares chamado alginato, um pó inorgânico chamado peróxido de bário e glóbulos vermelhos que foram levemente modificados para carregar dois fármacos imunológicos. Quando a mistura é injetada no tumor, as condições ácidas fazem o peróxido de bário se decompor, liberando íons bário e peróxido de hidrogênio. Os íons de bário cruzam instantaneamente o alginato formando um hidrogel macio, aprisionando os glóbulos vermelhos modificados no local e impedindo que os fármacos sejam levados embora. Ao mesmo tempo, enzimas naturalmente presentes nos glóbulos vermelhos convertem o peróxido de hidrogênio em oxigênio, ajudando a aliviar a hipóxia tumoral e preparando o tumor para uma radiação mais eficaz.
Liberação temporizada de sinais imunológicos duplos
O verdadeiro poder do sistema reside em como ele escalona a liberação de dois agentes imunológicos: um anticorpo que bloqueia CTLA-4 e uma citocina chamada interleucina-12 (IL-12). O anticorpo é carregado dentro dos glóbulos vermelhos, enquanto a IL-12 está ancorada na superfície deles. À medida que o oxigênio é gerado, poros se abrem na membrana dos glóbulos vermelhos, permitindo que o anticorpo bloqueador de CTLA-4 escape rapidamente. Essa liberação precoce remove a supressão imune, estimula as células dendríticas a levar antígenos tumorais aos linfonodos próximos e ajuda a ativar células T específicas do tumor. A IL-12, por contraste, vaza lentamente à medida que a estrutura do hidrogel se afrouxa gradualmente. Esse sinal tardio estimula células T e células natural killer a produzirem interferon-gama, reforça o recrutamento de células imunes citotóxicas para o tumor e consolida um ciclo de feedback positivo entre sentinelas e efetoras imunes.
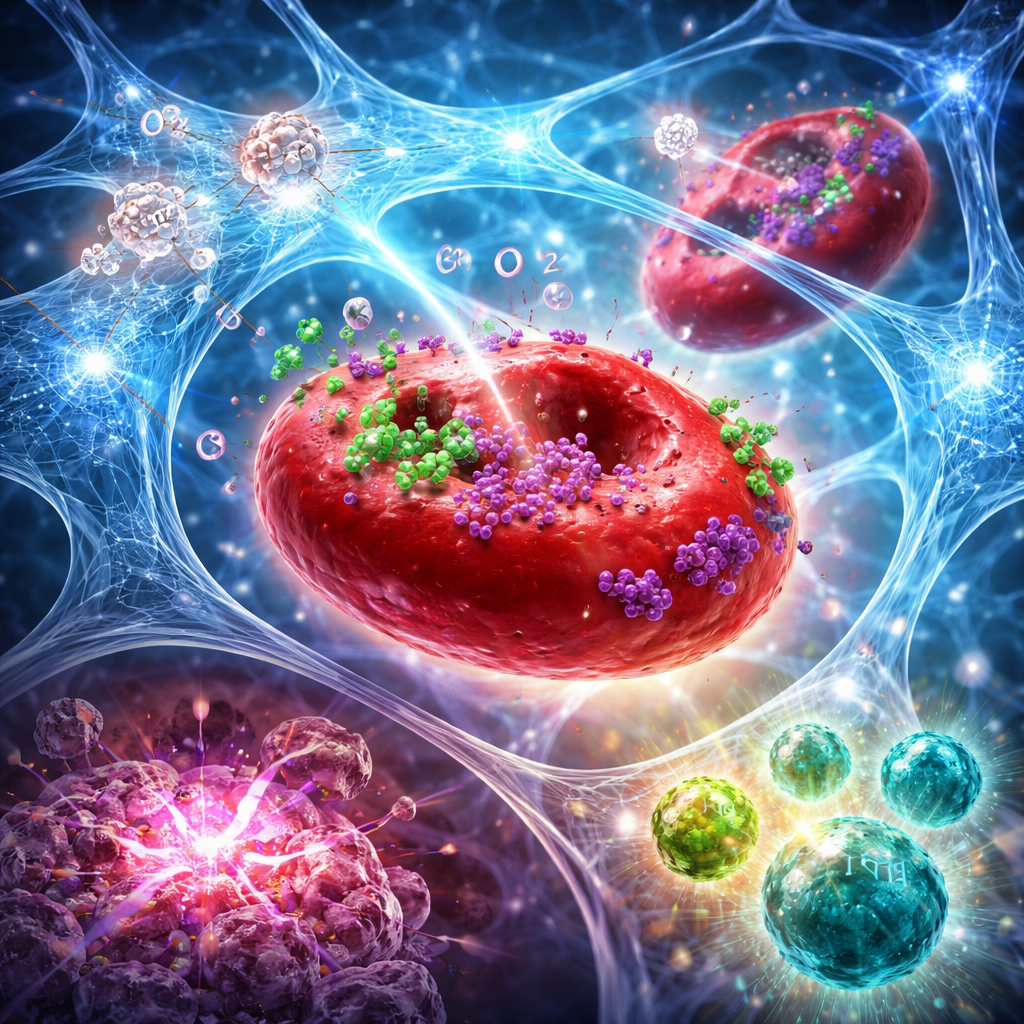
Da injeção local ao ataque imune sistêmico
Em modelos de camundongos com cânceres agressivos de mama e pâncreas, combinar este hidrogel com radiação focalizada fez mais do que apenas encolher o tumor tratado. A abordagem combinada aumentou os níveis de oxigênio nos tumores por dias, amplificou o dano ao DNA induzido pela radiação e desencadeou uma forma mais intensa de morte celular que naturalmente sinaliza os tumores para reconhecimento imune. Citometria de fluxo e colorações teciduais mostraram uma mudança pronunciada no microambiente tumoral: mais células T CD8 citotóxicas e células natural killer, menos células T reguladoras e uma maior proporção de células “efetoras” para “supressoras”. Células dendríticas especializadas nos linfonodos também aumentaram, indicando melhor apresentação de antígenos. Muitos camundongos experimentaram regressão tumoral completa, e alguns ficaram protegidos contra o re-implante tumoral semanas depois, sugerindo a formação de memória imune duradoura.
Segurança, praticidade e direções futuras
Porque o gel se forma localmente e retém sua carga, apenas pequenas quantidades de IL-12 e anti‑CTLA‑4 vazam para a corrente sanguínea, reduzindo o risco de efeitos colaterais graves, como tempestades de citocinas ou danos a órgãos, que limitaram esses agentes no passado. Os blocos de construção — alginato, glóbulos vermelhos e peróxido de bário — são relativamente baratos e escaláveis, levantando esperanças de que essa estratégia possa ser adaptada para diferentes cânceres. Embora desafios permaneçam na fabricação, controle de qualidade e na entrega do gel a tumores profundos ou amplamente disseminados, o trabalho demonstra uma maneira promissora de sincronizar a radiação com ativação imune precisamente temporizada, transformando um tratamento físico do câncer em um gatilho poderoso para imunidade antitumoral sistêmica.
O que isso pode significar para os pacientes
Em termos cotidianos, esta pesquisa sugere que, em vez de administrar radiação e drogas imunológicas separadamente e esperar que cooperem, podemos embalá-las em um material inteligente que fica dentro do tumor, produz seu próprio oxigênio e libera sinais imunológicos em uma sequência cuidadosamente coreografada. Em animais, essa abordagem não apenas tornou a radiação mais letal para as células cancerosas, como também treinou o sistema imunológico para reconhecer e lembrar o tumor, ajudando a prevenir sua recorrência. Se resultados semelhantes puderem ser obtidos em humanos, tais hidrogéis poderão um dia transformar tumores de difícil tratamento em alvos que as defesas do próprio corpo consigam localizar e destruir de forma confiável.
Citação: Chen, Y., Chen, Q., Ma, Y. et al. In situ self-assembled cell reservoir hydrogel for maneuvering multistage radioimmunotherapy. Nat Commun 17, 1784 (2026). https://doi.org/10.1038/s41467-026-68490-5
Palavras-chave: radioimunoterapia, hidrogel, imunoterapia contra o câncer, microambiente tumoral, radioterapia