Clear Sky Science · pt
Mult estabilidade continuamente ajustável em redes de replicação de DNA
De Interruptores Simples a Muitos Estados Possíveis
Sistemas biológicos, desde células em divisão até embriões em desenvolvimento, raramente funcionam como interruptores simples que estão apenas ligados ou desligados. Em vez disso, costumam manter muitos estados duradouros, como um dimmer que pode parar em posições infinitas. Este artigo descreve uma rede química baseada em DNA que se comporta mais como esse dimmer: ela pode manter de forma estável não apenas alguns estados distintos, mas essencialmente qualquer composição ao longo de um espectro contínuo. Essa capacidade pode se tornar uma base poderosa para materiais inteligentes futuros, memórias moleculares e computadores bioquímicos que processem informação analógica, e não apenas digital.
Por Que Múltiplos Estados Estáveis Importam
Muitas decisões celulares — se uma célula‑tronco se diferencia, se uma célula se autodestrói ou se uma rede gênica lembra um sinal passado — dependem da “multestabilidade”, a capacidade de repousar em mais de um padrão estável de atividade sob as mesmas condições. Versões sintéticas tradicionais desses sistemas foram construídas a partir de circuitos gênicos, enzimas ou fitas de DNA que ativam ou inibem umas às outras. Esses projetos tipicamente produzem um punhado de resultados discretos, como interruptores bistáveis clássicos com dois estados duradouros. Escalar essa ideia é difícil: um sistema de N estados pode exigir da ordem de N×(N−1) ligações inibitórias cuidadosamente ajustadas, e o sistema ainda salta apenas entre um pequeno conjunto de pontos fixos em vez de oferecer um contínuo suave de possibilidades.
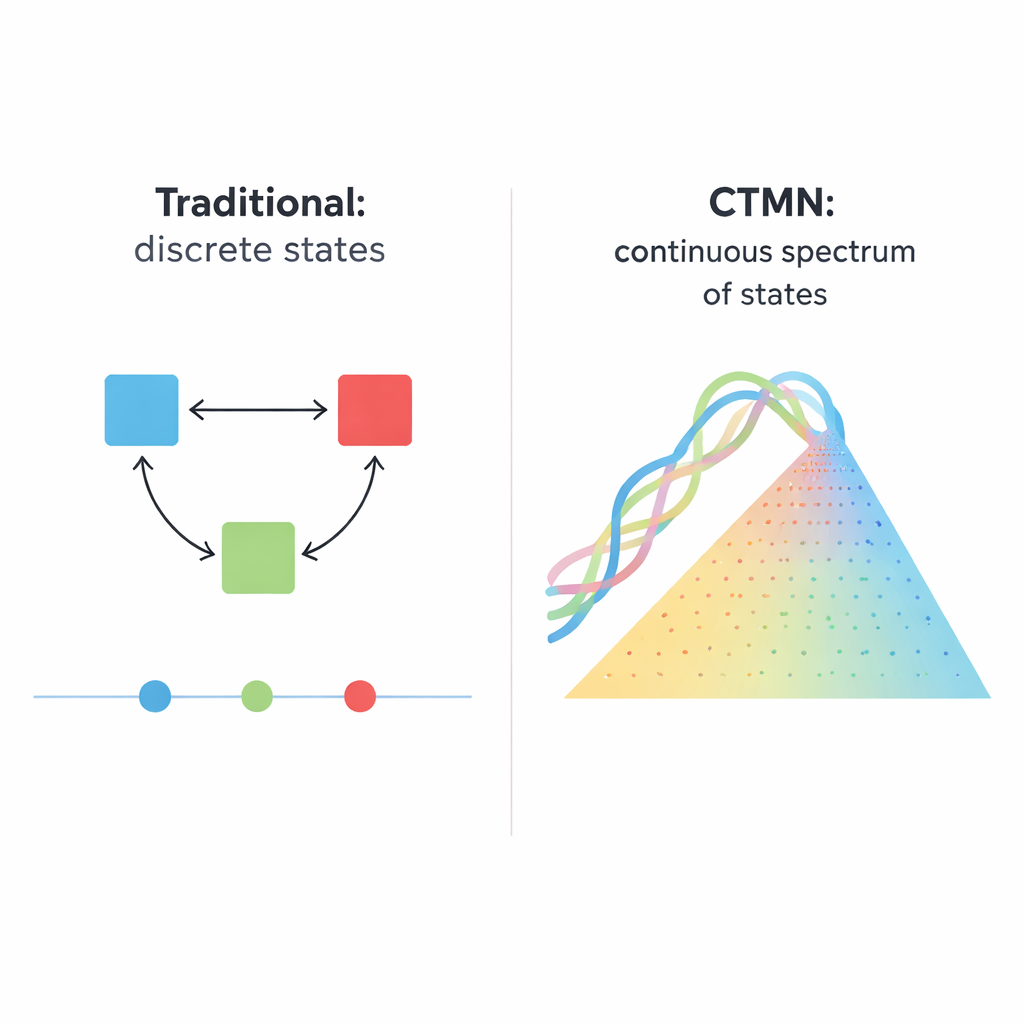
Um Novo Tipo de Rede de DNA: Continuamente Ajustável
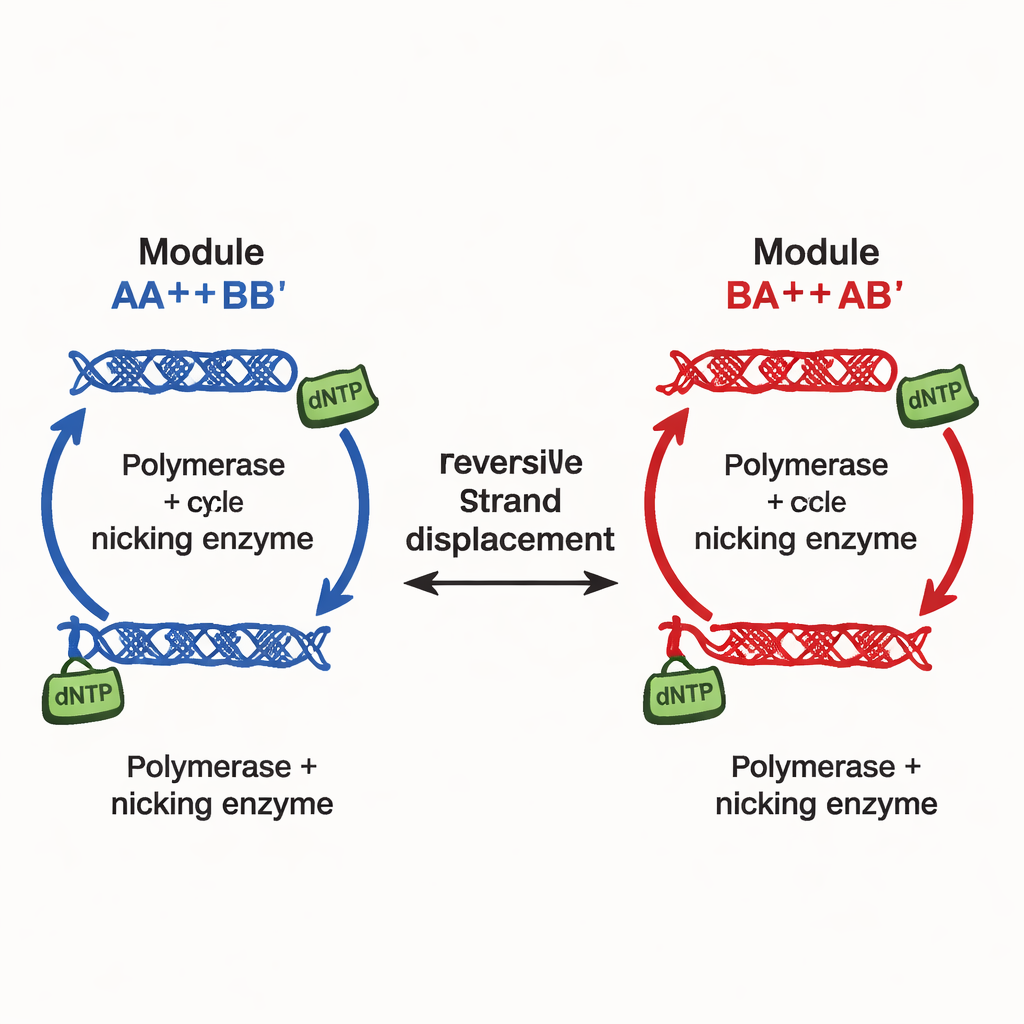
Os autores apresentam um princípio de projeto diferente, implementado no que chamam de redes de multestabilidade continuamente ajustável (CTMNs). Em vez de depender de muitos sinais inibitórios separados, eles usam competição direta entre módulos de replicação de DNA unidos por reações reversíveis de troca de fitas. Cada módulo é composto por duplexos de DNA projetados que tanto participam do deslocamento de fitas quanto servem de molde para a polimerase de DNA, auxiliada por uma enzima nicking que corta e regenera segmentos-chave. O combustível químico — blocos construtores nucleotídicos chamados dNTPs — impulsiona a polimerização e o nicking contínuos, mantendo o sistema longe do equilíbrio. Nestas condições, os módulos em competição efetivamente “congelam” nas proporções relativas com que começaram, produzindo não apenas dois ou três resultados, mas uma linha contínua inteira (ou, para mais módulos, um plano) de estados duradouros.
Como a Máquina Molecular Trava a Memória
No seu arranjo mais simples de dois módulos, CTMN‑1, a equipe demonstra experimentalmente e por meio de modelagem cinética detalhada que o sistema pode se estabilizar em uma família de misturas estáveis que abrangem quase toda a faixa de “principalmente módulo A” a “principalmente módulo B”. A polimerização converte duplexos ativos em formas estendidas que ficam temporariamente fora da competição de troca de fitas; o nicking então os restaura, fechando um laço autorregulatório. Quando ambos os módulos compartilham esse laço, eles suprimem a interconversão mútua com tanta força que o sistema permanece travado próximo à composição inicial por muitas horas, desde que haja combustível disponível. A análise de estabilidade linear das equações subjacentes revela uma variedade inteira — efetivamente um continuum — de estados estacionários, em contraste com o único ponto fixo observado quando as enzimas ou o combustível são removidos.
Respostas Programáveis e Memória Molecular
Como o estado da rede é armazenado nas composições de DNA, ele pode ser direcionado e lido de maneiras programáveis. Os autores projetam “gatilhos” curtos de RNA que se ligam temporariamente a fitas de DNA específicas, enviesando a competição e deslocando a rede para uma nova composição. Mesmo após o RNA ser degradado por uma enzima, o novo estado persiste, funcionando como uma forma de memória molecular. Estímulos repetidos ou mais fortes conduzem o sistema suavemente ao longo do continuum de estados em vez de simplesmente alterná‑lo entre posições on/off. Além disso, os próprios produtos da replicação de DNA podem ser customizados para atuar como sinais para processos a jusante: em demonstrações, diferentes estados do CTMN‑1 ativam seletivamente um de dois catalisadores baseados em DNA ou enviesam a transcrição de RNA em direção a uma de duas fitas mensageiras, sem perturbar a multestabilidade subjacente.
Escalando para “Dimmers” Moleculares Complexos
Para mostrar que essa estratégia é escalável, os pesquisadores constroem uma rede de três módulos, CTMN‑2, adicionando mais duplexos de DNA projetados que compartilham um domínio comum de troca, mas codificam moldes de replicação diferentes. Agora os estados estacionários possíveis preenchem uma região bidimensional, como pontos através de um diagrama de fases triangular, em vez de uma linha simples. Novamente, experimentos confirmam que muitas composições distintas são estáveis enquanto há combustível e enzimas presentes, e que todas colapsam para um único ponto de equilíbrio quando o suprimento de energia é removido. Como adicionar novos módulos requer apenas novos constructos de DNA que se encaixam na mesma estrutura de deslocamento, a interconexão geral não aumenta em complexidade como nos projetos tradicionais.
O Que Isso Significa para Tecnologias Moleculares Futuras
Para um não‑especialista, a mensagem central é que os autores transformaram uma rede de replicação de DNA em um dispositivo de memória analógico altamente flexível. Em vez de escolher entre algumas opções predefinidas, seu sistema pode manter de forma confiável uma entre dezenas de estados experimentalmente distinguíveis, cada um definido pela quantidade de cada módulo de DNA presente, e pode converter pulsos químicos transitórios em deslocamentos duradouros ao longo desse continuum. Como as fitas de saída de DNA são programáveis e desacopladas do mecanismo estabilizador, o mesmo arcabouço poderia, em princípio, regular uma ampla gama de reações bioquímicas a jusante ou propriedades de materiais com controle fino e graduado. Este trabalho, portanto, aponta para dispositivos moleculares que computam, lembram e se adaptam mais como sistemas analógicos neurais ou mecânicos do que como interruptores digitais simples.
Citação: Zhong, R., Fu, Y., Jiang, S. et al. Continuously tunable multistability in DNA replication networks. Nat Commun 17, 1782 (2026). https://doi.org/10.1038/s41467-026-68488-z
Palavras-chave: multestabilidade de DNA, memória molecular, redes bioquímicas sintéticas, deslocamento de fitas de DNA, computação molecular analógica