Clear Sky Science · pt
Previsão robusta e interpretável de marcadores gênicos e tipos celulares a partir de dados de transcriptômica espacial
Transformando lâminas de tecido rotineiras em mapas moleculares
Quando uma biópsia é realizada, os médicos normalmente veem apenas o que o microscópio revela: as formas e padrões das células em colorações rosas e roxas. Contudo, por trás dessas cores existe um mundo oculto de genes que se ligam e desligam, influenciando como um câncer cresce e responde ao tratamento. Este estudo apresenta o STimage, um novo sistema de inteligência artificial (IA) que busca ler esse roteiro molecular diretamente de imagens patológicas padrão, potencialmente oferecendo insights mais rápidos e baratos sem testes laboratoriais adicionais.
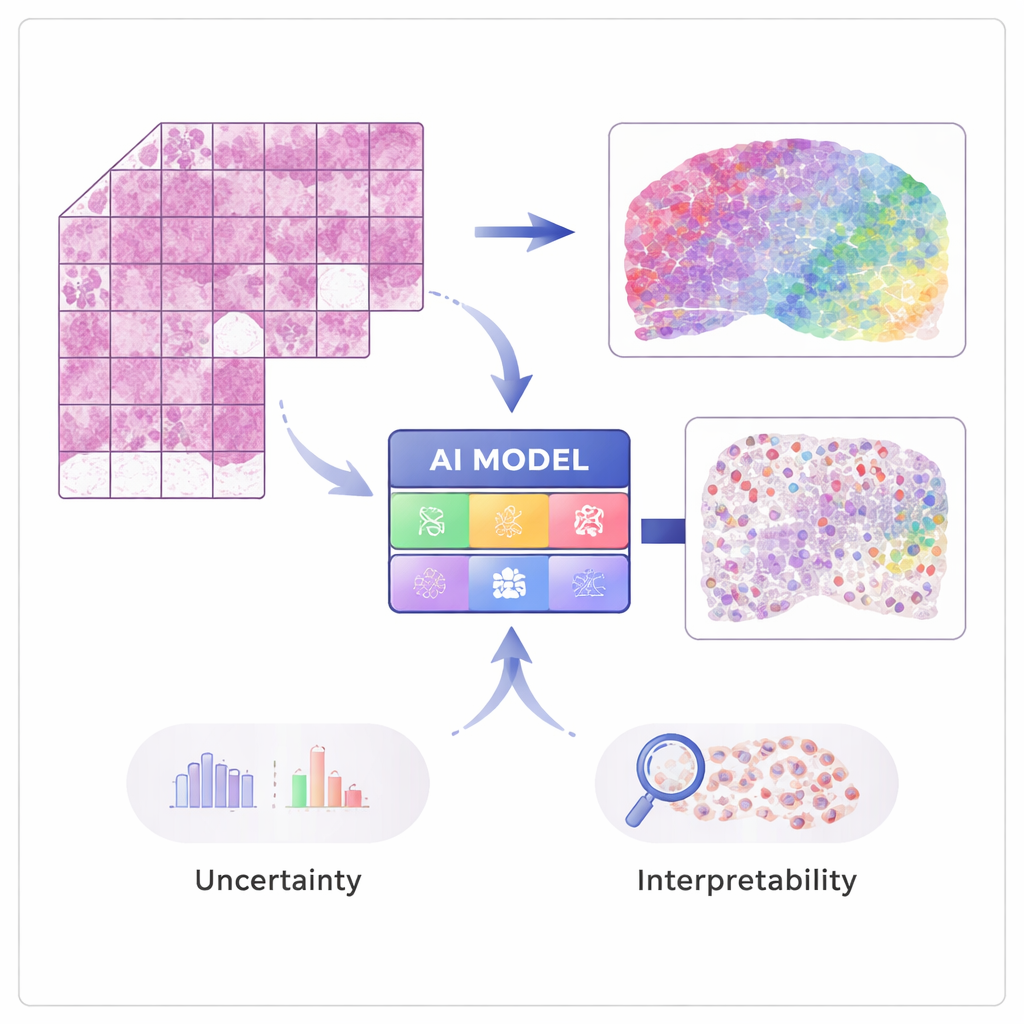
De imagens à atividade gênica
Técnicas modernas de “transcriptômica espacial” podem medir a atividade de dezenas de milhares de genes preservando onde cada sinal se originou no tecido. Esses métodos são poderosos, mas caros e ainda não rotineiros em hospitais. O STimage é treinado em um número modesto desses conjuntos de dados espaciais, nos quais cada imagem de tecido é emparelhada com medições gênicas detalhadas em muitos pontos minúsculos. A IA aprende a associar padrões visuais locais no corante hematoxilina e eosina (H&E) — como a densidade ou a irregularidade dos núcleos — com a atividade gênica subjacente, de modo que depois possa prever expressão gênica e tipos celulares apenas a partir de imagens comuns.
Construindo um patologista de IA mais confiável
Um objetivo central do trabalho não é apenas a precisão, mas a confiabilidade e a explicabilidade. Em vez de produzir um único número para cada gene, o STimage prevê uma distribuição de probabilidade completa, descrevendo uma faixa provável de atividade gênica em cada local. Ele também separa dois tipos de incerteza: uma causada por dados ruidosos ou variáveis, e outra que reflete a própria falta de conhecimento do modelo. Ao treinar muitas versões ligeiramente diferentes do modelo e fazer uma média entre elas — uma abordagem em “conjunto” (ensemble) — os pesquisadores tanto melhoram o desempenho quanto obtêm uma noção mais clara de onde o sistema está confiante e onde não está, o que é crucial para a tomada de decisões clínicas.
Testando em vários tipos de câncer, tecnologias e hospitais
A equipe avaliou o STimage em conjuntos de dados diversos de câncer de mama, pele e rim, bem como em uma doença hepática relacionada ao sistema imunológico. O sistema aprendeu a prever marcadores importantes do câncer e do sistema imune, muitas vezes correspondendo aos padrões espaciais verdadeiros observados em experimentos independentes. O modelo manteve seu desempenho quando desafiado por dados de diferentes laboratórios, métodos de preparo de amostras e até tecnologias subjacentes distintas, incluindo plataformas com resolução de célula única e sistemas mais antigos de resolução inferior. Em comparações diretas com várias ferramentas de IA existentes, o STimage e suas variantes em conjunto geralmente se destacaram, particularmente ao avaliar quão bem os padrões previstos correspondiam à distribuição real da atividade gênica ao longo do tecido.
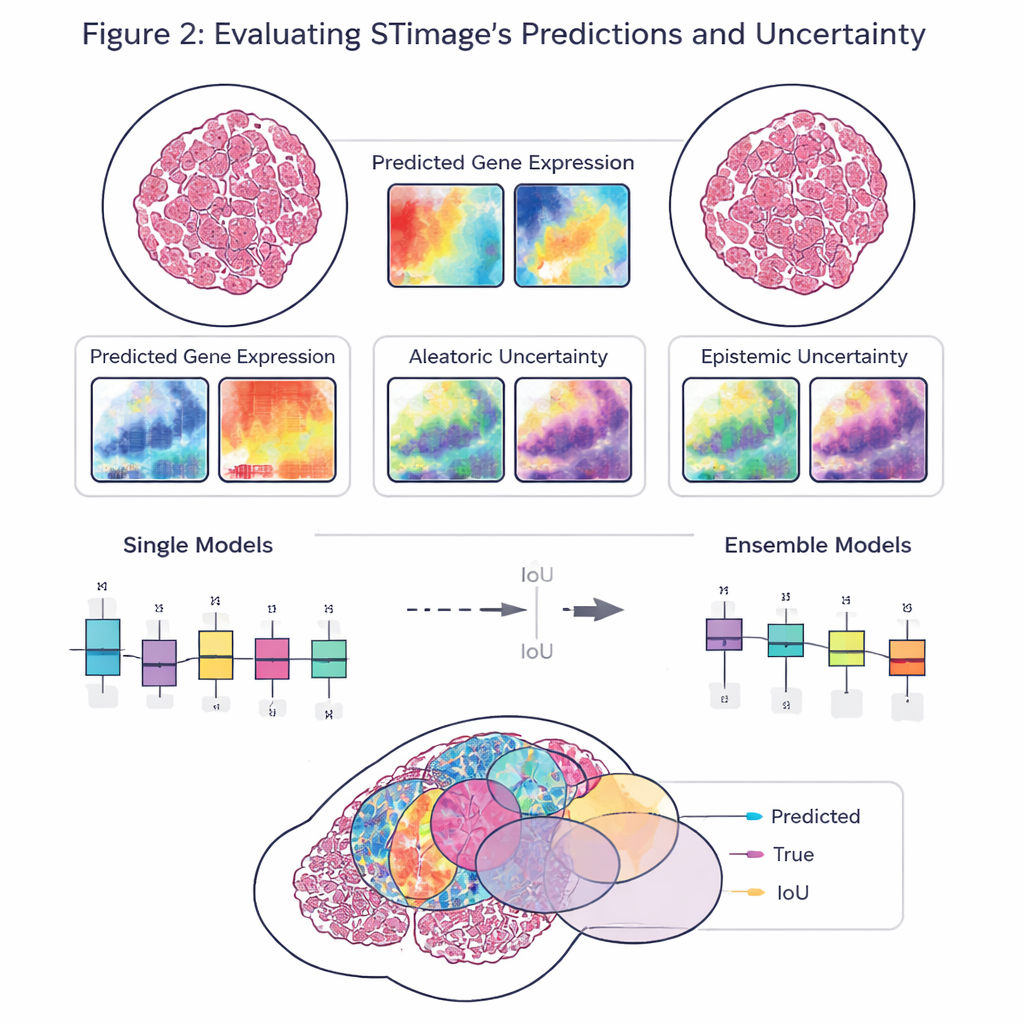
Vendo dentro dos tumores: células, sobrevivência e resposta ao fármaco
O STimage vai além da previsão gênica para inferir quais tipos celulares ocupam cada região, usando conjuntos de dados de alta resolução em que a identidade de cada célula é conhecida. O modelo foi capaz de distinguir células cancerosas de células imunes e de suporte e mapear seu arranjo na lâmina. Os autores então aplicaram o STimage a grandes coleções de imagens rotineiras de câncer do The Cancer Genome Atlas. Mesmo sem medições espaciais, os perfis gênicos previstos pela IA estavam fortemente alinhados com dados gênicos em larga escala (bulk). Essas previsões foram suficientemente robustas para agrupar pacientes em categorias de risco mais alto e mais baixo e para ajudar a distinguir aqueles com maior probabilidade de responder completamente a certas terapias do câncer de mama.
Por que isso importa para pacientes futuros
Para pacientes e clínicos, a promessa do STimage é uma espécie de “sobreposição molecular” na lâmina de patologia conhecida. Em vez de solicitar vários testes caros, uma única imagem digitalizada poderia um dia revelar onde programas gênicos agressivos estão ativos, como as células imunes estão distribuídas e quais marcadores apontam para piores ou melhores desfechos ou respostas a medicamentos diferentes. Embora o método ainda esteja sendo refinado e a correlação com medições reais não seja perfeita, sua capacidade de captar padrões espaciais, estimar sua própria incerteza e destacar quais células direcionam suas previsões o torna um passo prático rumo a uma patologia digital mais informativa e transparente.
Citação: Tan, X., Mulay, O., Xie, J. et al. Robust and interpretable prediction of gene markers and cell types from spatial transcriptomics data. Nat Commun 17, 1781 (2026). https://doi.org/10.1038/s41467-026-68487-0
Palavras-chave: patologia digital, transcriptômica espacial, biomarcadores do câncer, aprendizado profundo, microambiente tumoral