Clear Sky Science · pt
Visão espectroelectroquímica de catalisadores de cobre-cobalto para coaeletorredução de CO2 e nitrito até ureia
Transformando gases residuais em fertilizante
O fertilizante ureia sustenta a agricultura moderna, mas sua produção convencional consome muita energia e é intensiva em carbono. Este estudo explora uma abordagem bem diferente: usar eletricidade para converter dióxido de carbono (CO2) e resíduos contendo nitrogênio (como nitrito de emissões ou efluentes) diretamente em ureia. Para o leitor leigo, o apelo é claro: um caminho para um fertilizante essencial que pode reduzir emissões, usar correntes de resíduos como matérias-primas e, no futuro, ser alimentado por eletricidade renovável.
Por que repensar a produção de ureia?
Hoje, a ureia é produzida em grande parte pela via que primeiro gera amônia a partir de nitrogênio e hidrogênio de origem fóssil (processo Haber–Bosch), e depois faz reagir a amônia com CO2 em altas temperaturas e pressões. Essa cadeia de reações é centralizada, exige alto investimento e emite perto de uma tonelada de CO2 por tonelada de ureia produzida. À medida que a demanda global por fertilizantes cresce, aumentam também os custos ambientais. Uma alternativa é evitar os combustíveis fósseis ao conduzir as etapas químicas-chave com eletricidade — idealmente renovável — e utilizar CO2 e óxidos de nitrogênio (NOx) que hoje são tratados como resíduos.
Um novo papel para cobre e cobalto
Os autores projetam catalisadores em filme fino fabricados por co-sputtering de cobre (Cu) e cobalto (Co) sobre papel-carbono, ajustando cuidadosamente a razão Cu:Co. Eles se concentram na eletorredução simultânea de CO2 e nitrito (NO2⁻) em água com pH neutro, um ambiente que pode favorecer a formação sutil das ligações carbono–nitrogênio (C–N) necessárias para a ureia. A composição de destaque é uma mistura 1:1 de Cu e Co, que alcança uma taxa de produção de ureia de cerca de 61 mmol por hora por grama de catalisador em uma tensão aplicada moderada. Microscopia e medidas por raios X mostram que os metais estão intimamente misturados em escala atômica e permanecem em grande parte metálicos durante a operação, oferecendo uma plataforma robusta onde tanto CO2 quanto nitrito podem reagir de forma eficiente. 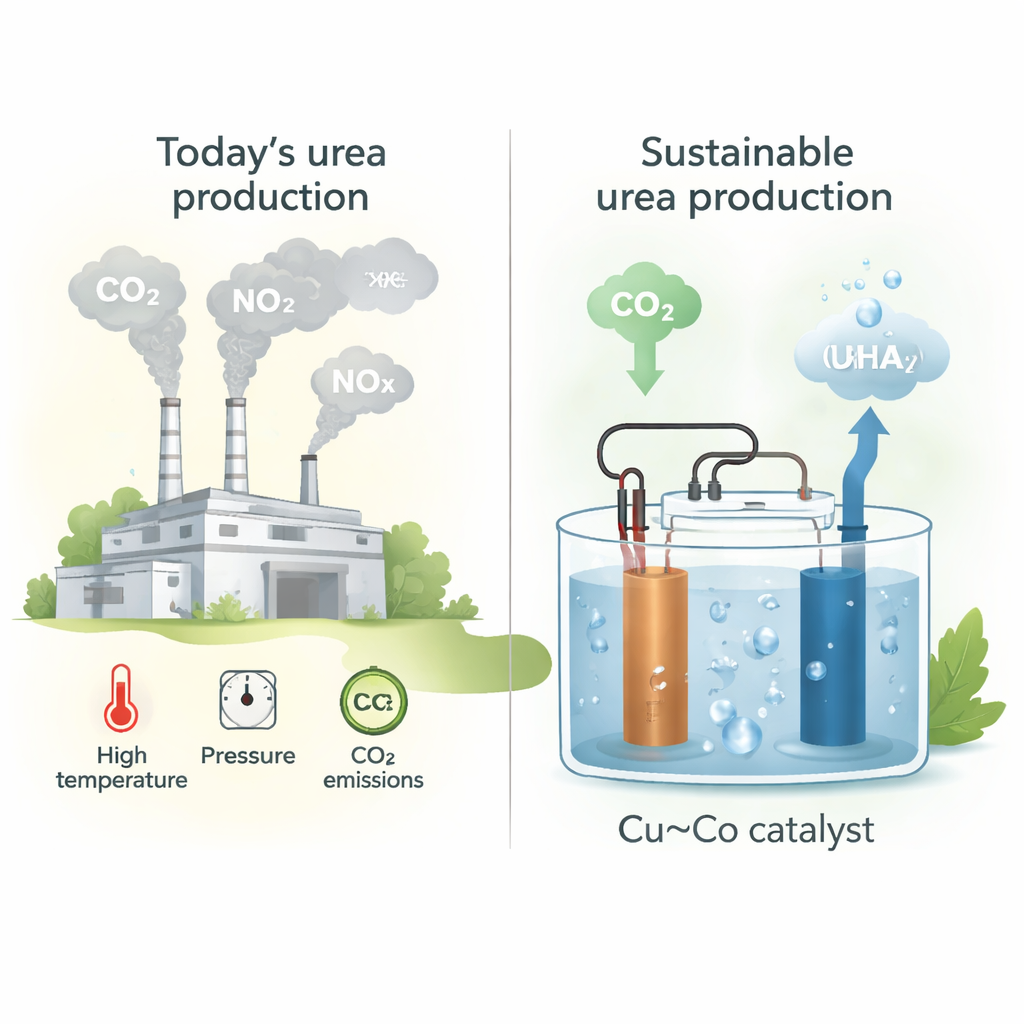
Como o catalisador divide e compartilha o trabalho
Produzir ureia dessa maneira é desafiador porque reações mais simples — como evolução de hidrogênio ou a redução isolada de CO2 ou nitrito — competem fortemente. A chave, constatam os pesquisadores, é uma divisão de tarefas entre sítios de cobre e cobalto que atuam em conjunto. Testes eletroquímicos mostram que o cobre isoladamente converte majoritariamente CO2 em combustíveis e produtos de carbono, enquanto o cobalto isoladamente converte principalmente nitrito em amônia, sem formação de ureia em nenhum dos casos. Só quando átomos de Cu e Co estão misturados de perto se observa produção significativa de ureia. “Instantâneos” espectroscópicos obtidos durante a reação detectam fragmentos ligados à superfície: espécies de carbono derivadas de CO2 (*CO e *COOH) que preferem o cobre, e espécies de nitrogênio derivadas do nitrito (*NH2 e grupos relacionados) que preferem o cobalto. Nas bordas entre Cu e Co, esses fragmentos podem se encontrar e acoplar-se para formar a espinha dorsal C–N da ureia.
Encontrando as condições certas para formar ligações
O estudo mostra que a composição por si só não basta; a solução circundante e a membrana também precisam ser ajustadas. A ureia aparece apenas em um eletrólito bicarbonato neutro, que mantém CO2 dissolvido suficiente e fornece a quantidade adequada de prótons (íons hidrogênio) para impulsionar etapas de “transferência de elétrons acoplada a prótons” sem inundar a superfície com evolução de hidrogênio. Em condições fortemente ácidas ou fortemente alcalinas, a ureia ou não se forma ou se decompõe rapidamente em produtos mais simples. Experimentos com diferentes fontes de nitrogênio revelam que o nitrito é especialmente eficaz para a formação de ureia, superando nitrato e hidroxilamina. Testes por várias horas indicam que os filmes Cu–Co são relativamente estáveis, com perda metálica modesta e produção sustentada de ureia.
Olhando por baixo do capô com teoria
Para entender por que esse catalisador em tandem funciona tão bem, a equipe recorre a simulações computacionais baseadas em teoria do funcional da densidade. Esses cálculos apoiam a ideia de que o cobre favorece a ligação de espécies derivadas de CO2, enquanto o cobalto ativa melhor o nitrito e estabiliza fragmentos contendo nitrogênio. As simulações apontam para uma etapa particular como o gargalo energético: o acoplamento de um fragmento *NH2 (do nitrito) com um fragmento *COOH (do CO2) para formar um intermediário às vezes escrito como *NH2CO. Uma vez que essa peça esteja formada, as etapas restantes até a ureia são comparativamente mais fáceis. A interface Cu–Co reduz o custo energético desse acoplamento crucial em comparação com cobre puro ou cobalto puro, explicando o aumento observado experimentalmente no rendimento de ureia para o sistema bimetálico. 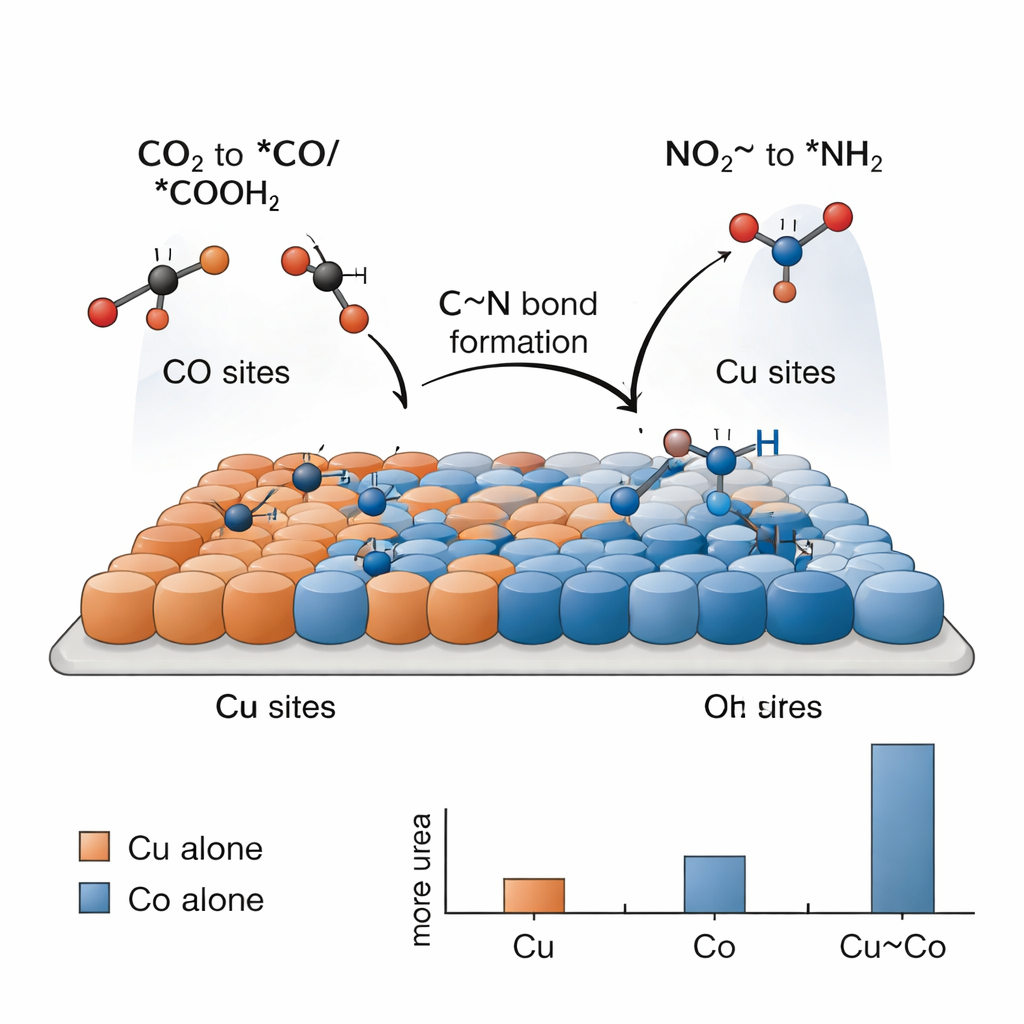
Da descoberta de laboratório para fertilizante mais verde
Em termos práticos, este trabalho ainda não substitui as gigantescas plantas de ureia atuais, mas esclarece como uma rota eletroquímica futura poderia ser projetada. Ao mostrar que cobre e cobalto podem operar em tandem — um fornecendo espécies de carbono ativadas, o outro espécies de nitrogênio ativadas, ambos sob condições de prótons cuidadosamente controladas — o estudo traça um caminho realista rumo a uma produção de ureia mais limpa e potencialmente descentralizada que use CO2 e resíduos nitrogenados como recursos em vez de poluentes.
Citação: Ramadhany, P., Trần-Phú, T., Yuwono, J.A. et al. Spectroelectrochemical insight into copper cobalt catalysts for CO2 and nitrite co-electroreduction to urea. Nat Commun 17, 1776 (2026). https://doi.org/10.1038/s41467-026-68481-6
Palavras-chave: síntese eletroquímica de ureia, catalisador cobre cobalto, utilização de CO2, redução de nitrito, formação de C–N