Clear Sky Science · pt
Base estrutural para a inibição seletiva do transportador de GABA humano GAT3
Por que acalmar os sinais cerebrais é importante
Nossos cérebros dependem de um equilíbrio delicado entre sinais que excitam e aqueles que acalmam. Um mensageiro calmante fundamental é o GABA, um químico que ajuda a prevenir atividade descontrolada associada a condições como epilepsia, lesão por AVC e doença de Alzheimer. Este estudo foca em uma proteína chamada GAT3, que remove o GABA do entorno das células nervosas. Ao revelar, em detalhes atômicos, como uma nova molécula se prende ao GAT3 e o desativa, os pesquisadores oferecem um mapa estrutural para projetar drogas de próxima geração que possam reforçar de forma sutil o sistema de freio natural do cérebro.
O próprio pedal de freio do cérebro
O GABA é o principal neurotransmissor inibitório, ou calmante, do sistema nervoso central. Depois que o GABA é liberado nas terminações nervosas, ele precisa ser removido rapidamente para que os circuitos cerebrais possam se reiniciar. Essa limpeza é realizada por proteínas transportadoras que bombeiam o GABA de volta para as células. Duas dessas transportadoras predominam no cérebro: GAT1, encontrada principalmente em neurônios, e GAT3, presente em células de suporte chamadas astrócitos. Enquanto um medicamento que bloqueia GAT1 (tiagabina) tem sido usado há décadas para tratar a epilepsia, medicamentos comparáveis que miram GAT3 ficaram para trás. No entanto, o GAT3 é especialmente interessante porque controla os níveis de GABA fora das sinapses e molda a inibição de fundo, de longa duração, que pode ajustar finamente a atividade cerebral. 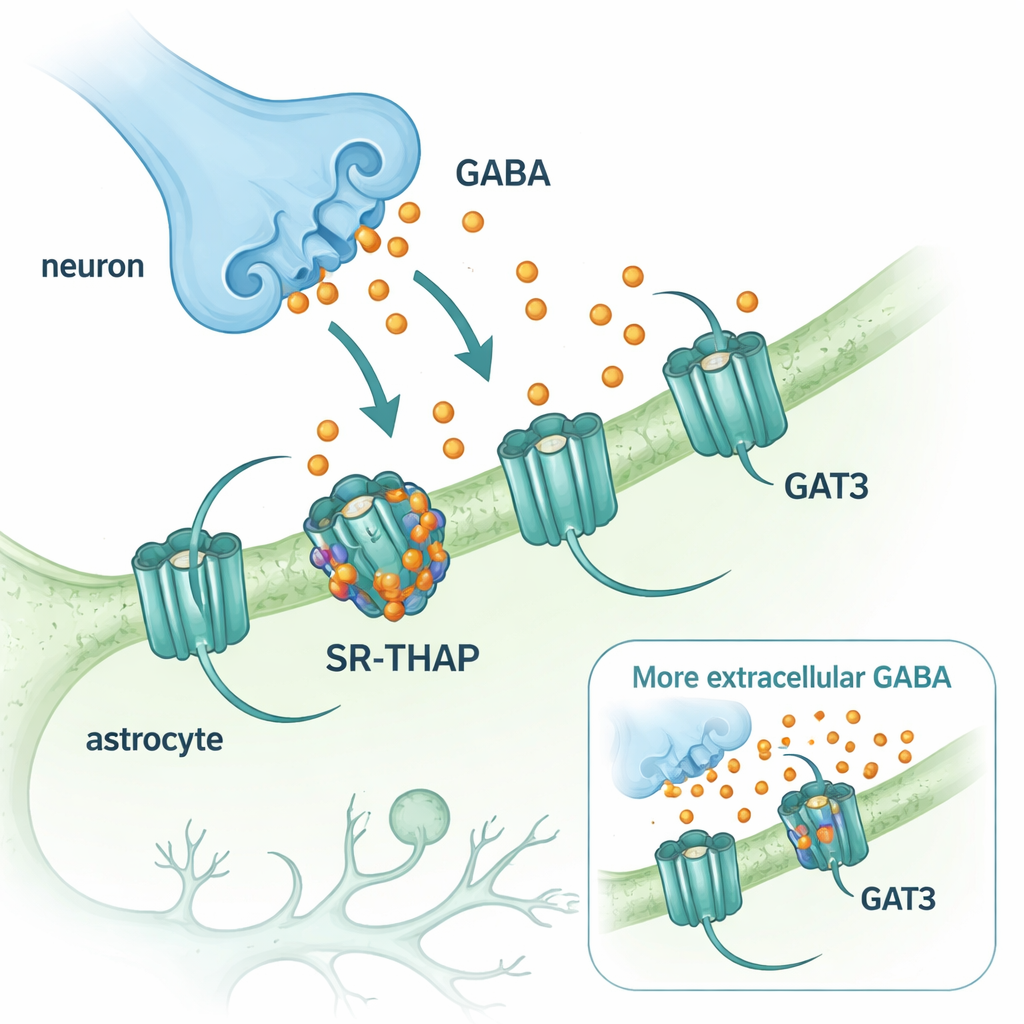
Projetando uma trava molecular mais precisa
As tentativas de inibir o GAT3 foram dificultadas pela falta de informações estruturais detalhadas. Muitos compostos anteriores foram criados por tentativa e erro, frequentemente fazendo variações volumosas de moléculas conhecidas semelhantes ao GABA. Um dos mais conhecidos, (S)‑SNAP‑5114, mostrou‑se quimicamente instável e difícil de usar em animais vivos. Com base em um parente mais resistente dessa substância, os autores desenvolveram o SR‑THAP, uma nova pequena molécula projetada para encaixar‑se melhor no GAT3 e resistir à degradação. Experimentos em culturas de células humanas mostraram que o SR‑THAP bloqueia fortemente o GAT3 e o faz de forma não competitiva: em vez de simplesmente competir com o GABA no sítio habitual, ele altera o funcionamento do transportador, reduzindo sua capacidade máxima de transporte.
Observando o GAT3 em resolução quase atômica
Para entender exatamente como o SR‑THAP atua, a equipe recorreu à crio‑microscopia eletrônica, uma técnica que imagina proteínas congeladas rapidamente com elétrons e reconstrói sua forma tridimensional. Eles resolveram três versões do GAT3 humano: ligado ao SR‑THAP, ligado ao GABA e em um estado sem substrato. Todas as três revelam a arquitetura típica observada em transportadores de neurotransmissores relacionados: 12 hélices compactas que atravessam a membrana e formam um caminho central para o GABA e seus íons acompanhantes, sódio e cloro. Na estrutura ligada ao GABA, o transportador está em um estado “o cluído para dentro” — o GABA e um íon de sódio estão fixados no meio, selados tanto do lado de fora quanto do interior. Um aminoácido aromático-chave forma uma interação especializada com o grupo amino do GABA, ajudando a explicar como o GAT3 reconhece seu substrato.
Como o SR‑THAP emperra o transportador aberto
Em contraste marcante, a estrutura ligada ao SR‑THAP captura o GAT3 em um estado “aberto para dentro”, com o lado interno da proteína escancarado em direção ao interior da célula. O SR‑THAP repousa profundamente nessa cavidade interna, preso entre várias hélices que normalmente se movem durante o ciclo de transporte. Ele ocupa três pequenos bolsões com caracteres químicos diferentes, estabelecendo uma rede de ligações de hidrogênio e contatos hidrofóbicos. Esse posicionamento efetivamente trava o transportador de modo que o GABA e os íons não podem completar sua jornada. Os autores mostram que alguns aminoácidos específicos que revestem essa cavidade diferem entre o GAT3 e seus parentes próximos; trocar um desses resíduos altera tanto a atividade de transporte quanto a potência do SR‑THAP, ajudando a explicar por que o inibidor é muito mais seletivo para GAT3 do que para GAT1 ou transportadores relacionados. 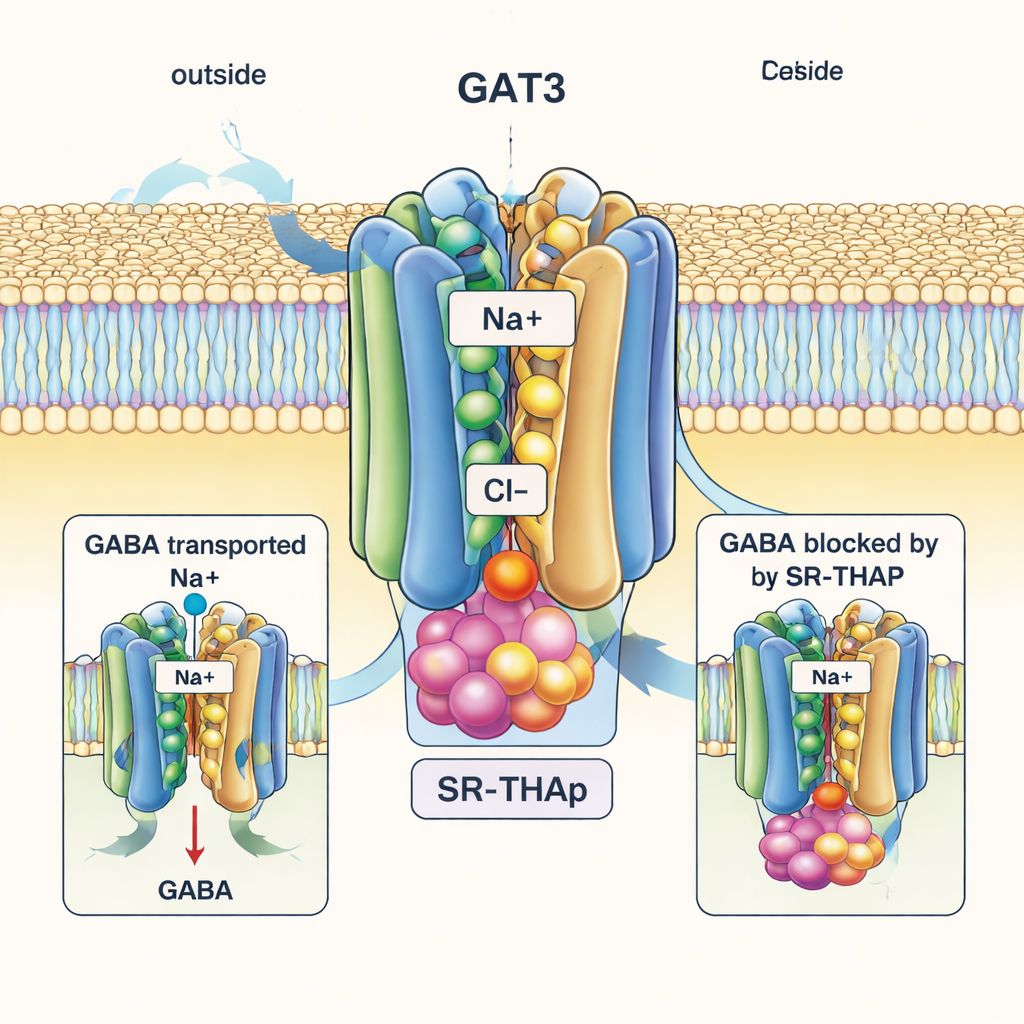
Abrindo portas para novos fármacos contra epilepsia e para a saúde cerebral
Juntas, essas estruturas revelam como o GAT3 alterna entre diferentes conformações para mover o GABA, e como o SR‑THAP explora um bolso interno menos conservado para congelar esse ciclo. Para não especialistas, a principal conclusão é que o estudo fornece uma planta molecular detalhada para desligar o GAT3 de forma altamente seletiva. Compostos desse tipo poderiam elevar os níveis de GABA calmante de maneira mais finamente ajustada do que as drogas existentes, possivelmente levando a novos tratamentos ou ferramentas de pesquisa para epilepsia, recuperação de AVC, doença de Alzheimer e outras condições em que a sinalização inibitória está perturbada.
Citação: Mortensen, J.S., Bavo, F., Jensen, M.H. et al. Structural basis for selective inhibition of human GABA transporter GAT3. Nat Commun 17, 1774 (2026). https://doi.org/10.1038/s41467-026-68479-0
Palavras-chave: transportador de GABA, GAT3, epilepsia, crio‑ME, inibição de neurotransmissores