Clear Sky Science · pt
Um mecanismo estocástico impulsiona a translocação rápida de substrato na máquina AAA+ ClpB
Como as Máquinas Celulares Mantêm as Proteínas em Movimento
Dentro de cada célula, pequenas máquinas moleculares puxam, tensionam e remodelam proteínas constantemente para evitar que se aglutinem e para reparar danos. Uma dessas máquinas, chamada ClpB, ajuda a resgatar proteínas que ficaram emaranhadas—uma função essencial para a sobrevivência celular sob estresse. Este estudo investiga uma pergunta simples, porém profunda: como o ClpB converte o combustível químico ATP no trabalho mecânico de puxar uma cadeia proteica através de seu poro central, e ele faz isso em passos ordenados, como um relógio, ou de modo mais aleatório e difusivo?
Um Anel de Resgate de Proteínas em Ação
O ClpB pertence a uma grande família de enzimas chamadas máquinas AAA+ que se montam em estruturas em forma de anel com um túnel central. Muitas foram capturadas em detalhe excepcional por criomicroscopia eletrônica, levando ao popular modelo de "passo a passo": cada molécula de ATP consumida impulsionaria um pequeno passo preciso, como uma equipe de pessoas puxando uma corda em sequência. No entanto, outros experimentos sugeriram que o ClpB poderia mover proteínas muito mais rápido do que sua lenta taxa de consumo de ATP pareceria permitir. Para resolver esse quebra-cabeça, os autores observaram moléculas individuais de ClpB em tempo real enquanto elas conduziam uma proteína-teste flexível, κ-caseína, através de seu poro.
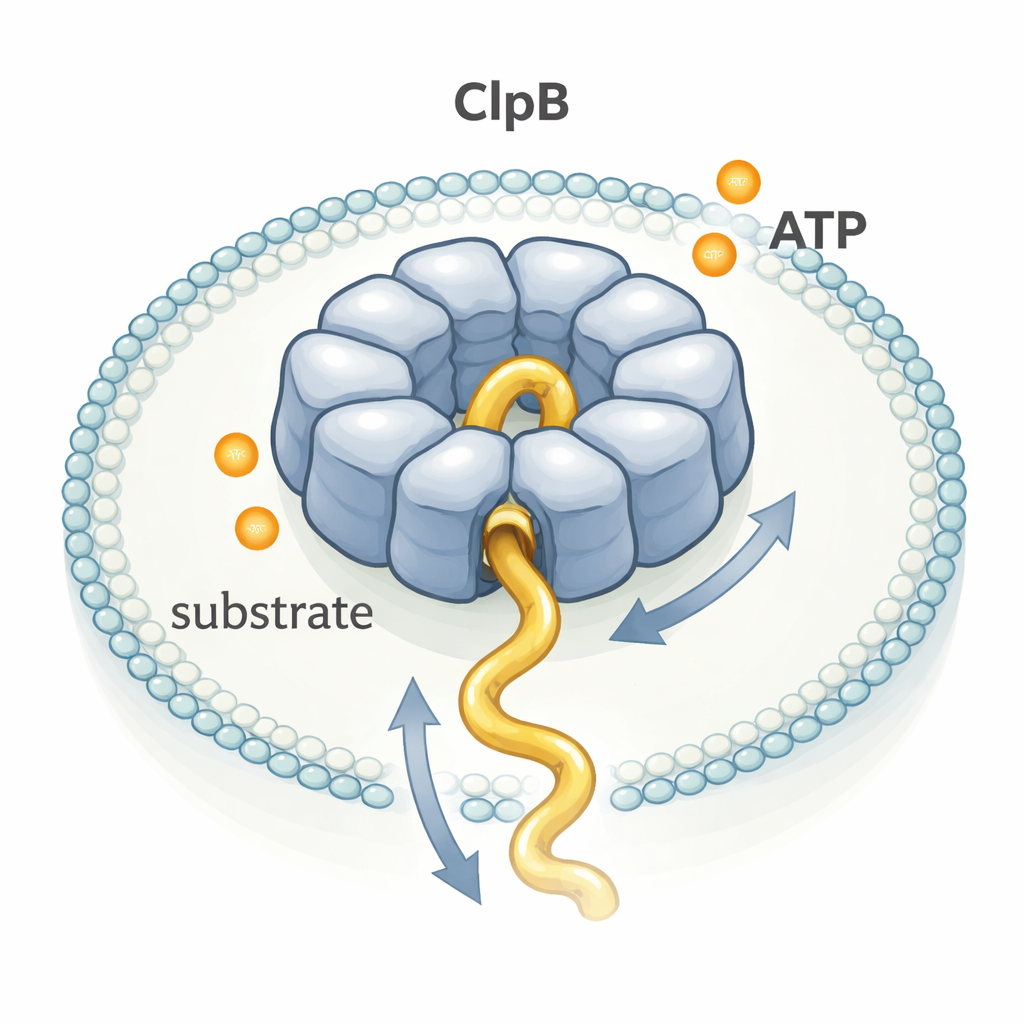
Observando Uma Molécula por Vez
Os pesquisadores aprisionaram anéis individuais de ClpB e moléculas isoladas de κ-caseína juntos dentro de minúsculas bolhas lipídicas presas a uma superfície de vidro. Eles fixaram corantes fluorescentes em pontos específicos do ClpB e na cadeia proteica, e então usaram FRET de única-molécula, uma técnica que reporta mudanças de distância entre corantes na escala de nanômetros. Quando a κ-caseína deslizava para o poro do ClpB, os corantes se aproximavam e o FRET disparava como um pico breve; quando a cadeia saía, o sinal caía novamente. Medindo a duração e a amplitude de milhares desses picos, puderam inferir com que rapidez e por quanto trecho segmentos da proteína atravessavam o poro.
Rápido, Pouco Alimentado e Quase Isento de Temperatura
Surpreendentemente, os eventos de translocação foram extremamente rápidos: o segmento rotulado da κ-caseína tipicamente atravessava vários nanômetros do poro em cerca de 1–2 milissegundos—aproximadamente mil vezes mais rápido que o tempo médio entre eventos de hidrólise de ATP no ClpB. A maioria dos eventos teve essa curta duração e seguiu uma ampla distribuição em lei de potência, em vez de um único tempo característico. Mudar a temperatura de 10 para 32 °C mal desacelerou esses movimentos, o que implica que a barreira energética para o movimento é minúscula em comparação com a de motores de "golpe de força" clássicos, como a cinesina. Da mesma forma, reduzir a concentração de ATP diminuiu fortemente a frequência com que os eventos ocorriam, mas teve quase nenhum efeito sobre a duração de cada evento. O ATP, em outras palavras, controlava quando o ClpB se engajava e com que frequência atuava, mais do que a velocidade de cada explosão individual de passagem.
Movimento de Vai-e-Vem com Tendência a Avançar
Para verificar se as cadeias sempre se moviam em uma única direção, a equipe realizou experimentos de FRET tricor coloridos mais complexos, tingindo ambas as extremidades do poro e o substrato. Isso lhes permitiu distinguir se a κ-caseína entrava pela parte superior ou inferior do anel e se ela atravessava completamente ou recuava. Descobriram seis padrões distintos: translocações completas para frente e para trás, "visitas" parciais mais longas nas quais a cadeia amostrava ambas as extremidades do poro antes de sair, e encontros fugazes próximos a apenas uma extremidade. Cerca de três quartos dos eventos completos seguiram na direção avançada, mas uma fração substancial foi para trás, revelando que o ClpB permite difusão bidirecional do substrato com apenas um viés moderado para frente. Quando o ATP foi substituído por um análogo de hidrólise lenta, os eventos se tornaram raros e muito mais lentos, e a preferência por avançar praticamente desapareceu.
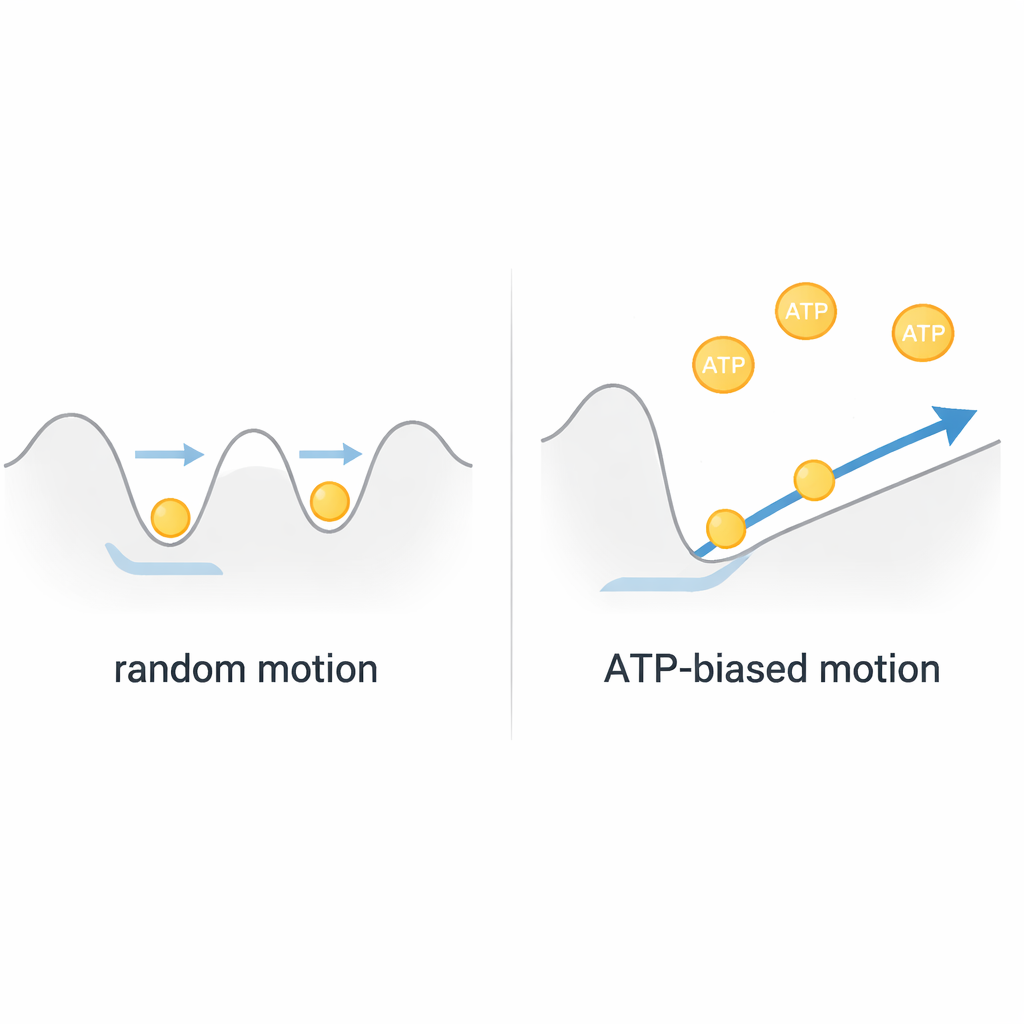
Um Motor Browniano, Não um Guincho Simples
Reunindo essas observações, os autores concluem que o ClpB funciona mais como um motor browniano do que como um guincho rígido movido a combustível. A cadeia proteica vibra termicamente dentro de um paisagem energética rasa no interior do poro, movendo-se rapidamente para frente e para trás. O ATP não alimenta diretamente grandes puxões discretos; em vez disso, ele ajusta a forma desse terreno energético por meio de movimentos rápidos de "laços de poro" internos, favorecendo sutilmente o movimento em uma direção. Como cada evento completo de passagem se correlaciona com apenas cerca de uma ou duas moléculas de ATP consumidas, o ClpB alcança um transporte notavelmente eficiente e rápido ao retificar o movimento aleatório em vez de combatê-lo. Essa visão reformula nosso entendimento sobre muitas máquinas AAA+, sugerindo que nanomotores biológicos frequentemente aproveitam a aleatoriedade em vez de eliminá-la.
Citação: Casier, R., Levy, D., Riven, I. et al. A stochastic mechanism drives fast substrate translocation in the AAA+ machine ClpB. Nat Commun 17, 1773 (2026). https://doi.org/10.1038/s41467-026-68478-1
Palavras-chave: translocação de proteínas, máquina AAA+, motor browniano, chaperona molecular, FRET de única-molécula