Clear Sky Science · pt
Identificação de PAMs não-canônicos termotolerantes para detecção robusta one-pot com CRISPR-Cas12a
Aumentando a temperatura nos testes de DNA
Testes rápidos e precisos para infecções e alterações genéticas são vitais para a medicina, mas os testes de DNA atuais frequentemente exigem equipamentos laboratoriais complexos e podem deixar escapar alvos raros ou sutis. Este estudo mostra como simplesmente executar um teste baseado em CRISPR um pouco mais quente desbloqueia muito mais “pegadas” úteis no DNA, tornando diagnósticos em um único tubo mais rápidos, mais sensíveis e capazes de distinguir até diferenças de uma única letra no código genético. 
Por que o CRISPR precisa de um código postal
Ferramentas CRISPR como a Cas12a funcionam ao localizar trechos específicos de DNA, guiadas por um pequeno RNA que atua como uma string de busca. Mas elas só conseguem se fixar e começar a atuar se uma etiqueta de quatro letras próxima, chamada PAM, tiver a sequência correta—tradicionalmente um conjunto restrito começando com “TTT”. Isso é como precisar de um número da casa para entregar uma carta: se o número certo está ausente, a mensagem nunca chega. Essa exigência de PAM limita onde o CRISPR pode procurar, um problema sério quando médicos precisam detectar mutações específicas, marcadores de resistência a drogas ou variantes virais que não ficam ao lado dessas etiquetas clássicas.
Descobrindo novas “portas” em temperaturas mais altas
Os pesquisadores testaram sistematicamente todas as 256 combinações possíveis de PAMs de quatro letras para avaliar como elas alimentavam a atividade de corte “colateral” da Cas12a—sua capacidade de fatiar muitas peças de DNA próximas uma vez que encontra seu alvo, o que é a base dos sinais diagnósticos de CRISPR. À temperatura corporal normal (37 °C), apenas algumas PAMs não-padrão performavam tão bem quanto as clássicas. Mas quando elevaram a temperatura da reação para cerca de 45 °C, algo notável aconteceu: 82 PAMs não-canônicas diferentes passaram a produzir forte atividade de corte de sinal, rivalizando com as etiquetas padrão. A equipe acredita que mais calor afrouxa a estrutura local do DNA e torna o complexo Cas12a mais flexível, diminuindo a barreira para reconhecer essas PAMs anteriormente “fracas”.
Sinal forte, cuidado com o molde
A Cas12a apresenta dois modos de corte. No modo “cis”, ela corta o DNA específico que foi instruída a encontrar; no modo “trans”, uma vez ativada, ela rapidamente fragmenta quaisquer fitas portadoras de sinal nas proximidades, o que ilumina o teste. Os pesquisadores descobriram que, em temperaturas mais altas, PAMs não-canônicas proporcionavam corte trans muito forte—ótimo para uma leitura brilhante e rápida—mas mantinham o corte cis do DNA principal relativamente fraco. Essa combinação é ideal para testes one-pot, onde o DNA precisa ser primeiro amplificado sem ser destruído. Também mostraram que nessas condições mais quentes a Cas12a fica muito mais exigente quanto a incompatibilidades entre o RNA guia e o alvo: até uma única letra errada pode cortar o sinal, especialmente ao usar PAMs não-canônicas. 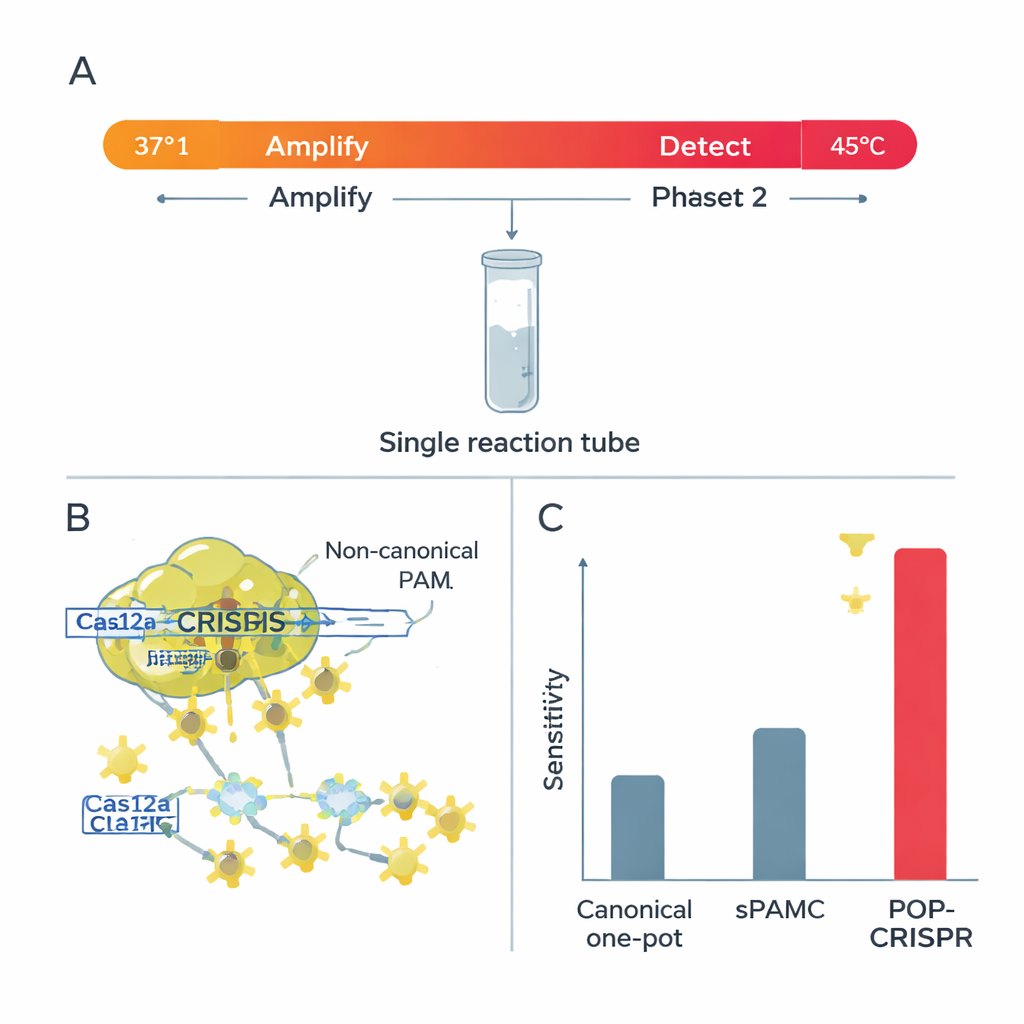
Um teste one-pot mais esperto: POP-CRISPR
Com base nesses achados, a equipe criou o POP-CRISPR, um ensaio one-pot “poiquilotérmico” (temperatura variável). A reação começa em torno de 37 °C, onde um método de amplificação isotérmica multiplica discretamente qualquer DNA ou RNA alvo enquanto a Cas12a está relativamente inativa. Após cerca de 10 minutos, a mistura é aquecida para cerca de 45 °C, um ponto ideal em que a Cas12a—agora guiada para locais PAM não-canônicos—ativa um potente corte trans e gera um forte sinal fluorescente. Esse simples programa de duas temperaturas aumentou a sensibilidade de detecção em aproximadamente dez vezes em comparação com métodos one-pot CRISPR anteriores que também usavam PAMs mais fracos, e superou claramente os formatos one-pot com PAMs canônicos convencionais.
Do banco ao leito em minutos
O sistema POP-CRISPR foi testado em amostras clínicas reais. Detectou sensivelmente o papilomavírus humano (HPV-16) em swabs vaginais e Mycoplasma pneumoniae em swabs respiratórios, incluindo casos de nível muito baixo na “zona cinzenta” que desafiam métodos padrão. Crucialmente, o POP-CRISPR conseguiu distinguir cepas de Mycoplasma resistentes a drogas que carregam uma mudança de uma única letra em um gene ribossomal, mesmo quando não havia um PAM clássico próximo a essa mutação—uma tarefa que frustra muitos testes Cas12a existentes. Para tornar a abordagem adequada ao campo, os autores combinaram um passo rápido de lise por aquecimento e Chelex de dois minutos (evitando extração completa de DNA) com um leitor de fluorescência do tamanho da palma controlado por smartphone. Juntos, esse fluxo de trabalho pode transformar um swab bruto em um resultado digital sim/não em cerca de 20 minutos.
O que isso significa para os testes do dia a dia
Ao elevar a temperatura da reação e explorar um conjunto muito mais amplo de “portas” PAM, este trabalho transforma a Cas12a em um sensor mais flexível e preciso. O POP-CRISPR oferece detecção de ácidos nucleicos mais rápida, mais sensível e mais específica em um único tubo fechado, ao mesmo tempo em que amplia a gama de locais genéticos que podem ser alvos—incluindo mutações de base única associadas à resistência a drogas ou ao câncer. Para pacientes, isso pode se traduzir em diagnósticos no local mais rápidos e tratamentos mais bem ajustados; para pesquisadores e desenvolvedores de testes, oferece uma nova maneira poderosa de projetar diagnósticos CRISPR mais robustos e mais discriminativos.
Citação: Tian, T., Zhang, T., Zhang, W. et al. Identification of thermotolerant non-canonical PAMs for robust one-pot CRISPR-Cas12a detection. Nat Commun 17, 1771 (2026). https://doi.org/10.1038/s41467-026-68476-3
Palavras-chave: diagnósticos CRISPR, Cas12a, locais PAM, testes ponto de atendimento, detecção de ácidos nucleicos