Clear Sky Science · pt
Mecanismos estruturais de inibição e ativação do canal de potássio humano SK2 ativado por Ca2+ de pequena condutância
Por que canais de potássio minúsculos importam
Cada pensamento que você tem e cada batida do seu coração dependem de sinais elétricos nas suas células. Esses sinais são moldados por poros microscópicos, chamados canais iônicos, que permitem a passagem de átomos carregados para dentro e para fora. Uma dessas famílias, os canais de potássio ativados por cálcio de pequena condutância (canais SK), ajuda a controlar como os neurônios disparam e como o coração mantém seu ritmo. Este artigo revela, em detalhe atômico, como diferentes fármacos e uma toxina de abelha podem tanto bloquear quanto potenciar um membro-chave dessa família, o canal humano SK2 — percepções que podem orientar novos tratamentos para doenças que vão da fibrilação atrial ao tremor e a problemas de memória.
Como os canais SK2 atuam como freios celulares
Os canais SK2 ficam na membrana celular e atuam como pequenos freios na atividade elétrica. Quando o interior de uma célula se enche brevemente de íons de cálcio durante um sinal elétrico, uma proteína auxiliar chamada calmodulina detecta esse aumento. A calmodulina está ligada ao lado interno do SK2 e, quando se liga ao cálcio, puxa uma parte do canal como um cordão de acionamento, abrindo um portão que permite a saída de íons de potássio. Esse fluxo para fora ajuda a acalmar a célula após o disparo, determinando com que frequência os neurônios podem enviar sinais e quão regular é o batimento das células cardíacas. Como os canais SK1–3 são amplamente distribuídos no cérebro e no coração, e o SK2 é um subtipo particularmente importante, entender exatamente como eles se abrem, fecham e respondem a fármacos é crucial para projetar medicamentos precisos.
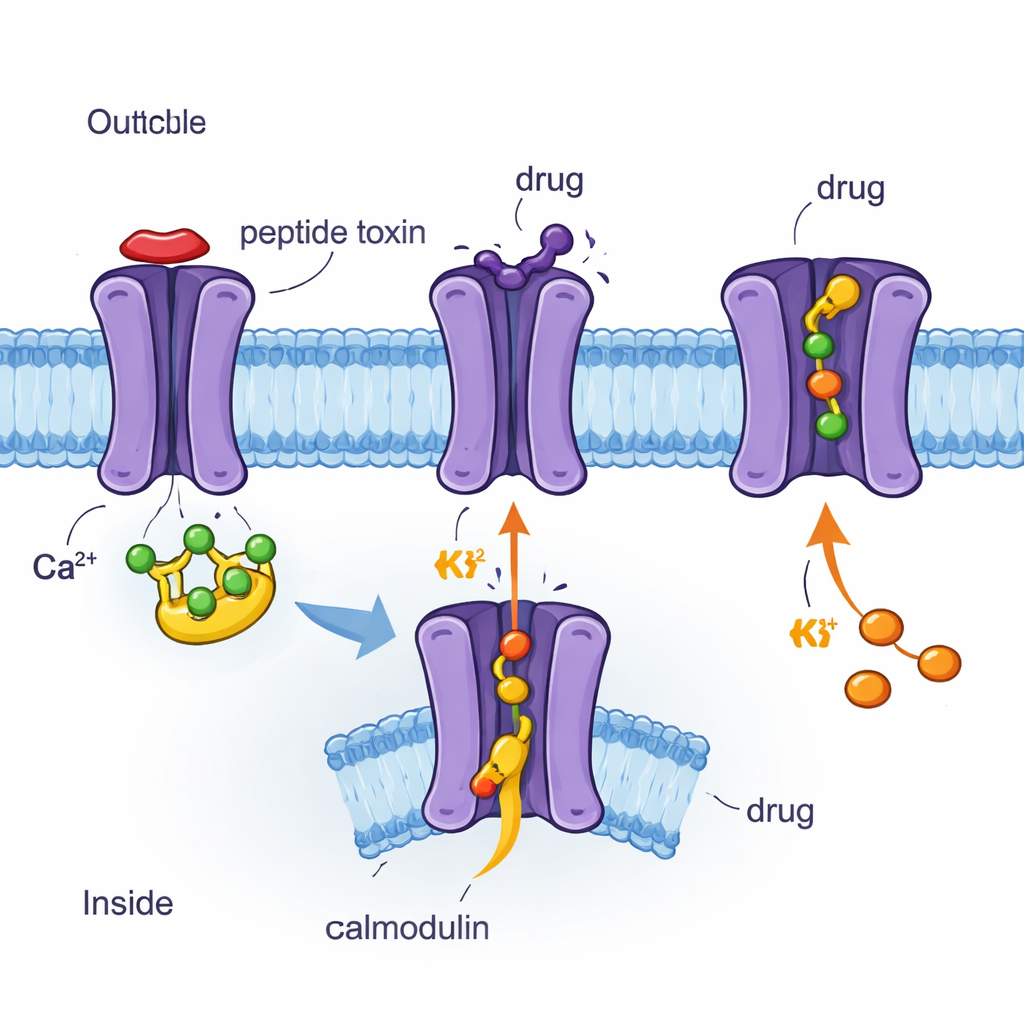
Usando crio‑ME para ver canais e fármacos átomo a átomo
Os autores usaram microscopia crioeletrônica (crio‑ME), uma técnica que imagina proteínas congeladas por vitrificação em resolução quase atômica, para determinar quatro estruturas tridimensionais do canal humano SK2 ligado à calmodulina e a diferentes moléculas. Essas incluíram o peptídeo do veneno de abelha apamina, o bloqueador sintético UCL1684, o inibidor clínico AP30663 e o ativador clínico CAD‑1883. Todas as quatro estruturas mostram o SK2 como um arranjo em quatro partes que atravessa a membrana, com a calmodulina ligada no interior. Comparar essas imagens revelou quais partes do canal são rígidas, quais são flexíveis e como a calmodulina se move quando o canal está em um estado fechado ou aberto. Os pesquisadores também combinaram essas imagens com medidas elétricas em células, testando como mudanças em aminoácidos específicos alteram a resposta do canal a cada composto.
Uma toxina de abelha e um fármaco de laboratório que tampam a boca externa
A apamina, um pequeno peptídeo do veneno de abelha, é conhecida há muito tempo como um bloqueador extremamente potente e seletivo do SK2 usado em pesquisas. As novas estruturas mostram que a apamina se liga como uma rolha na boca externa do poro do SK2. Ela se acomoda em um vestíbulo em forma de taça formado por uma alça curta entre duas hélices (o conector S3–S4) que é bem ordenada no SK2, mas frouxa em um canal relacionado, o SK4, explicando por que o SK4 é insensível à apamina. Resíduos positivamente carregados chave na apamina alcançam entre quatro cadeias aromáticas do canal, estabelecendo fortes interações eletrostáticas e de empilhamento que selam completamente a via do potássio. O UCL1684, um composto bis‑quinolínio sintético, ocupa essencialmente o mesmo bolso externo e também bloqueia a saída de íons, mas seu tamanho menor permite que ele se sente mais profundamente, imitando a posição das cargas positivas críticas da apamina. Mutar resíduos do canal que moldam esse vestíbulo reduz drasticamente a sensibilidade à apamina e, em menor grau, ao UCL1684, confirmando que esse laço externo esculpido é um determinante principal da ação da toxina e do fármaco.
Um tampão central e uma cunha interna que ajustam a atividade
Em contraste, o candidato clínico AP30663 se liga dentro da cavidade central do SK2, logo abaixo do filtro de seletividade que seleciona os íons de potássio. Ali ele atua como um tampão físico, encravado entre cadeias laterais específicas que revestem o poro. Alterações nesses resíduos de revestimento enfraquecem a capacidade do AP30663 de inibir o SK2, e comparações de sequência explicam por que seus análogos próximos podem distinguir SK1–3 de SK4. O CAD‑1883, um modulador positivo desenvolvido para distúrbios do movimento, usa outra estratégia. Ele se encaixa em um bolso na interface entre o lóbulon N da calmodulina e um curto conector (S4–S5) que acopla o movimento da calmodulina ao portão do canal. Ao reforçar contatos nesse bolso, o CAD‑1883 efetivamente cola a calmodulina e o SK2 em uma configuração que puxa o portão interno e alarga o poro. Comparações estruturais mostram que esse estado ligado ao CAD‑1883 assemelha‑se a um canal totalmente aberto, embora o filtro de seletividade possa adotar uma forma inativada após abertura prolongada.
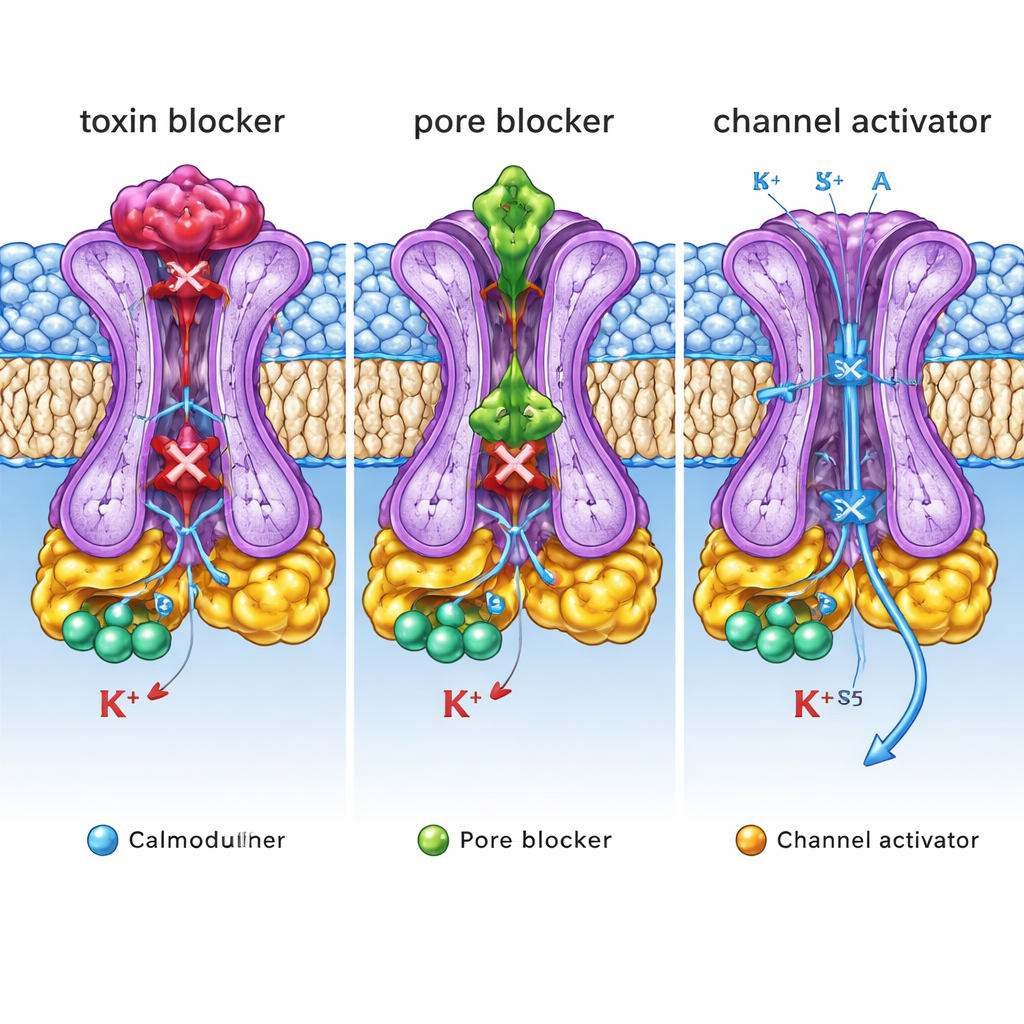
O que esses projetos estruturais significam para a medicina
Em conjunto, essas estruturas revelam três “botões de controle” distintos em um único canal SK2: uma tampa externa onde toxinas e alguns bloqueadores se assentam, uma cavidade interna do poro onde outros inibidores tampam o fluxo, e um bolso lateral onde ativadores estabilizam a abertura. Para um público não especializado, a mensagem-chave é que o mesmo canal iônico pode ser ajustado para cima ou para baixo por fármacos que agarram alças estruturais muito diferentes. Ao mapear essas alças com precisão atômica e relacioná‑las a efeitos funcionais, este trabalho fornece um roteiro detalhado para projetar moléculas de próxima geração que reduzam ou aumentem seletivamente a atividade do SK2. Tais fármacos sob medida poderiam, um dia, ajudar a normalizar ritmos cerebrais anormais, aliviar tremores ou corrigir batimentos cardíacos irregulares com menos efeitos colaterais.
Citação: Ma, B., Wu, D., Cao, E. et al. Structural mechanisms for inhibition and activation of human small-conductance Ca2+-activated potassium channel SK2. Nat Commun 17, 1770 (2026). https://doi.org/10.1038/s41467-026-68475-4
Palavras-chave: Canais de potássio SK2, canais ativados por cálcio, estruturas por crio‑ME, moduladores de canais iônicos, fibrilação atrial e tremor