Clear Sky Science · pt
Migração e divisão de células-tronco prejudicadas na distrofia muscular de Duchenne reveladas por imageamento ao vivo
Por que esta história muscular importa
A distrofia muscular de Duchenne (DMD) é uma doença infantil fatal que destrói gradualmente o músculo. Por décadas, a maior parte das pesquisas concentrou-se nas grandes fibras musculares que se degradam na DMD. Este estudo mostra que um segundo ator, mais discreto, também está comprometido: as próprias células-tronco do músculo, que normalmente reparam danos. Ao observar essas células vivas dentro de músculos de camundongos e em fibras individuais, os autores revelam como as células-tronco na DMD perdem o rumo, oferecendo novas ideias para tratamentos que podem ajudar os músculos a regenerar-se de forma mais eficaz.
A equipe de reparo integrada do músculo
Cada fibra muscular esquelética é ladeada por um punhado de células-tronco residentes, conhecidas como células satélites musculares. Em músculo saudável, essas células ficam dormindo na maior parte do tempo. Quando ocorre uma lesão, elas despertam, dividem-se e ou geram novas células-tronco para reabastecer a reserva ou produzem células especializadas que se fundem às fibras danificadas. Esse equilíbrio cuidadoso entre autorrenovação e diferenciação mantém o tecido muscular forte ao longo da vida. Na DMD, no entanto, as fibras musculares se rompem repetidamente porque carecem de distrofina, uma proteína estrutural essencial, suscitando a questão de saber se a própria equipe de reparo se exaure ou se desorienta.
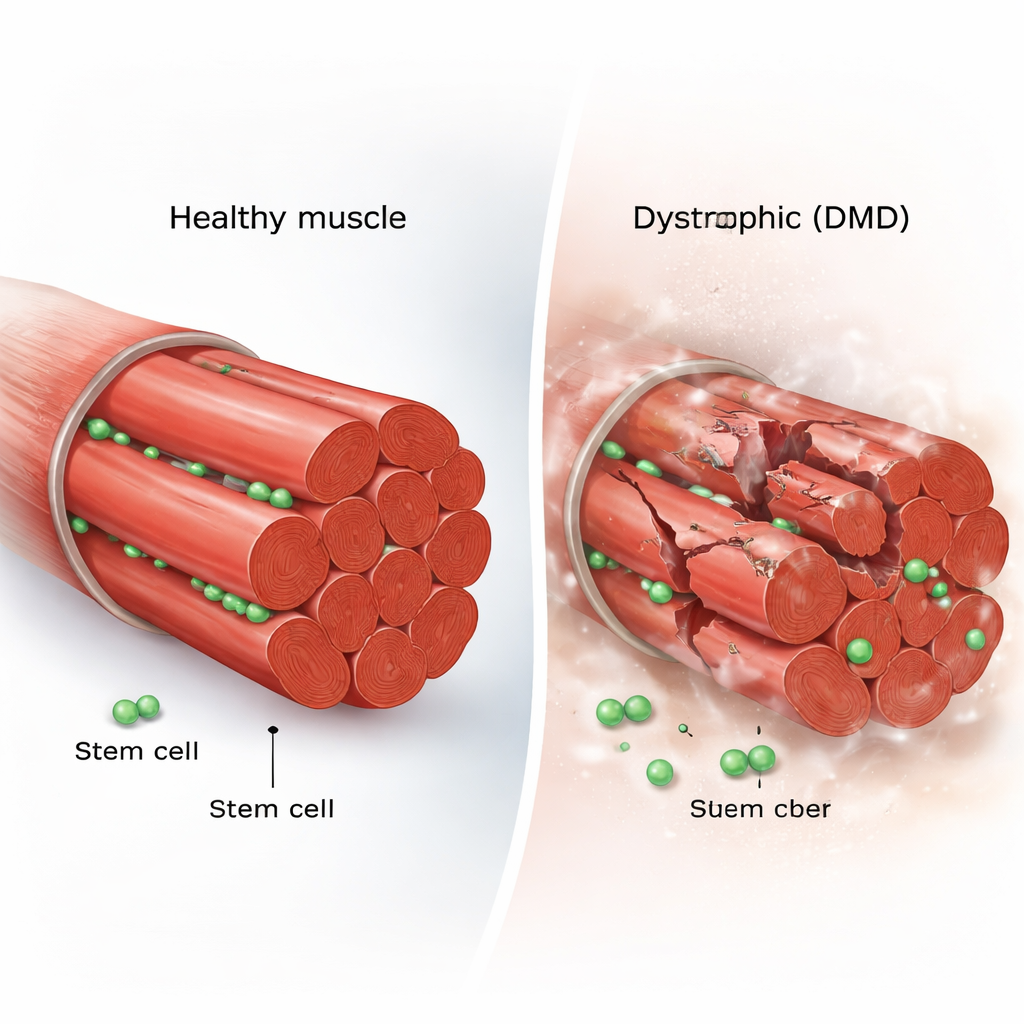
Filmando células-tronco em ação
Para responder a isso, os pesquisadores usaram o camundongo mdx, um modelo padrão de DMD, e projetaram as células-tronco musculares dele para brilharem sob o microscópio. Em seguida, realizaram imageamento intravital, uma técnica que permite filmar células vivas dentro de um animal anestesiado por muitas horas. Também desenvolveram um sistema “micropoço” personalizado para manter fibras musculares individuais em cultura enquanto rastreavam cada divisão e movimento das células-tronco. Essa abordagem dupla permitiu acompanhar células individuais desde o repouso até divisões repetidas, migrações e, por fim, fusão em novo músculo, capturando comportamentos que imagens estáticas facilmente deixariam passar.
Quando as células de reparo correm e tropeçam
Em músculos saudáveis lesionados, células miógenas derivadas de células-tronco alongavam-se e rastejavam ao longo das fibras por trajetórias relativamente retas e direcionadas, dividindo-se e espalhando-se com eficiência. Em contraste, células distróficas (mdx) frequentemente tornavam-se arredondadas e lentas. Moviam-se mais devagar e com menos direção, e uma fração notável permanecia quase imóvel. A equipe também descobriu que células mdx se fundiam em novas fibras musculares mais cedo do que o normal, e muitas células filhas migravam juntas em vez de se separarem após a divisão. No conjunto, os músculos mdx exibiram sinais de “diferenciação precoce”: as células-tronco apressavam-se em tornar-se células musculares e formar fibras, em vez de manter um reservatório robusto para reparos contínuos.
Divisões celulares desequilibradas e um ambiente confuso
Em fibras isoladas, os pesquisadores puderam classificar como cada célula-tronco se dividia. Em músculos saudáveis, a maioria das divisões era simétrica, porém equilibrada—muitas produziam duas filhas proliferativas que podiam continuar expandindo a reserva de reparo, e menos geravam duas células terminalmente diferenciadas. Divisões assimétricas, nas quais uma filha permanecia célula-tronco e a outra se comprometia com o reparo, eram relativamente raras, mas presentes. Nos músculos mdx, o padrão mudou dramaticamente: as divisões simétricas tenderam a produzir duas células diferenciadas, com muito menos divisões gerando duas células renovadoras. Experimentos de enxerto cruzado, nos quais células-tronco saudáveis foram colocadas em fibras distróficas e vice-versa, mostraram que os defeitos de migração foram amplamente ditados pelo ambiente da fibra danificada, enquanto o comportamento excessivamente diferenciador das células mdx seguiu as próprias células, moldado em parte por seu histórico inflamatório.
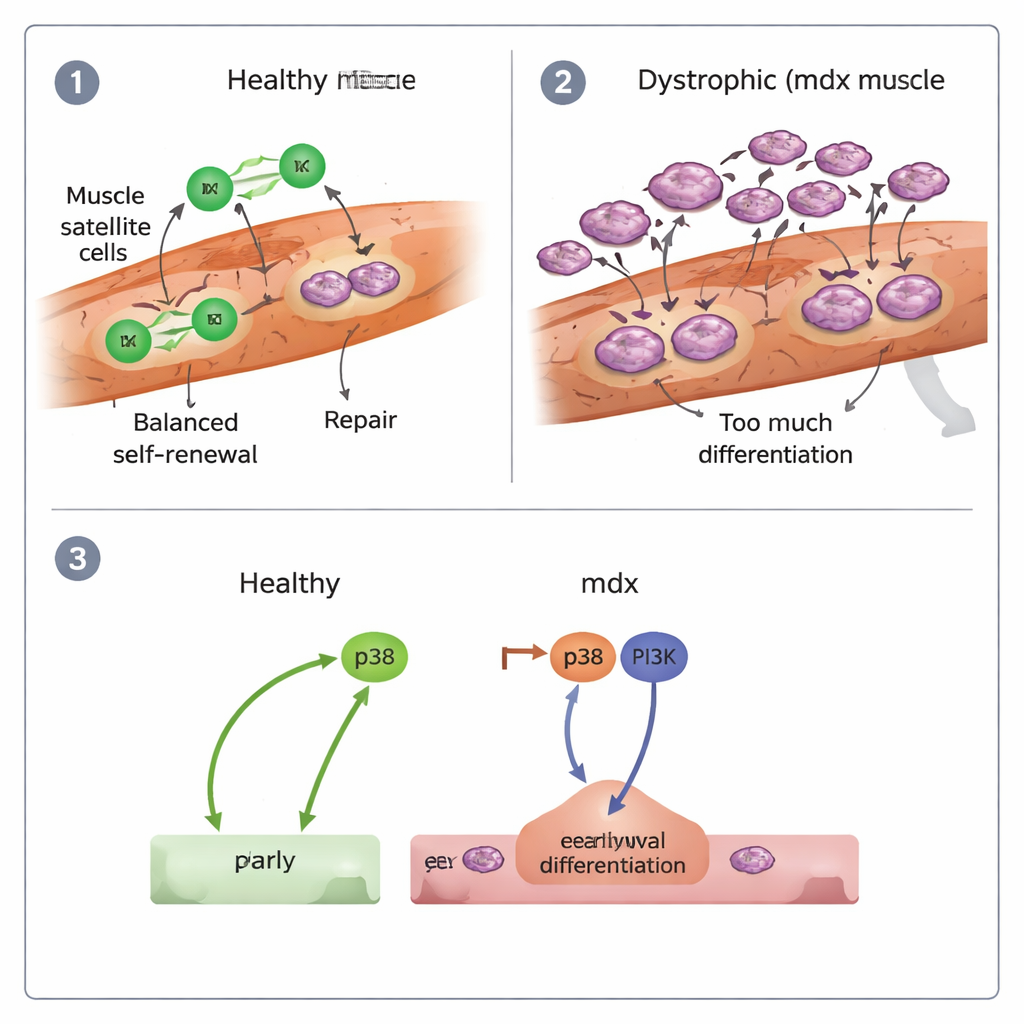
Sinais trocados e o que isso significa para a terapia
Os autores também investigaram os interruptores moleculares que empurram as células-tronco à diferenciação. Eles focaram em duas vias de sinalização, conhecidas como p38 e PI3K. Em células saudáveis, bloquear p38 reduziu fortemente a diferenciação, enquanto inibir PI3K teve pouco efeito. Em células mdx, porém, foi necessário bloquear ambas as vias em conjunto para conter a corrida excessiva à especialização, e ainda assim a capacidade de manter a proliferação permaneceu fraca. Isso sugere que as células-tronco na DMD são empurradas para um “esgotamento precoce” pela atividade combinada de p38 e PI3K, contribuindo para uma regeneração que começa rápida, mas não pode ser sustentada.
Uma nova visão de Duchenne: também uma doença das células-tronco
Para um leitor leigo, a mensagem central é que a DMD não é apenas um problema de fibras musculares frágeis; é também um problema do sistema de reparo que deveria consertá-las. Em músculo distrófico, as células-tronco movem-se com menos eficiência, dividem-se de forma a esgotar a reserva e respondem de maneira anômala a sinais de crescimento chave. Ao identificar quais aspectos são causados pelo ambiente muscular danificado e quais estão embutidos no estado alterado das células-tronco, este trabalho sugere novas estratégias: terapias que amenizem a sinalização p38 e PI3K, restabeleçam divisões celulares equilibradas ou melhorem o nicho local poderiam ajudar a reconstruir o músculo de forma mais eficaz e ampliar os benefícios de tratamentos genéticos ou baseados em células para pessoas que vivem com a distrofia muscular de Duchenne.
Citação: Sarde, L., Letort, G., Varet, H. et al. Impaired stem cell migration and divisions in Duchenne muscular dystrophy revealed by live imaging. Nat Commun 17, 1769 (2026). https://doi.org/10.1038/s41467-026-68474-5
Palavras-chave: Distrofia muscular de Duchenne, células-tronco musculares, migração celular, divisão de células-tronco, medicina regenerativa