Clear Sky Science · pt
Imprinting dependente de H3K27me3 e regulação transcricional em embriões de camundongo precoces requerem restrição da atividade de PRC2 mediada por EZHIP
Por que embriões minúsculos precisam de sincronização genética cuidadosa
Cada mamífero começa a vida como uma única célula que carrega um conjunto de cromossomos da mãe e outro do pai. Embora esses dois pacotes genéticos contenham quase as mesmas letras do DNA, eles chegam revestidos por marcas químicas diferentes que ajudam a decidir quais genes são ativados ou silenciados. Este estudo examina como um desses sistemas de marcação é mantido em equilíbrio durante os primeiros dias após a fertilização em camundongos, e por que perturbar esse equilíbrio pode atrapalhar o desenvolvimento normal.
Dois pais, dois genomas embalados de forma diferente
Em mamíferos, certos genes se comportam de maneira diferente dependendo se provêm da mãe ou do pai, um fenômeno chamado imprinting genômico. O imprinting clássico depende de marcas químicas no próprio DNA, mas nos últimos anos os cientistas descobriram um segundo tipo, mais transitório, que depende de uma modificação das proteínas histonas chamada H3K27me3. Essas histonas atuam como carretéis em torno dos quais o DNA é enrolado, e a H3K27me3 tende a silenciar genes próximos. Em embriões de camundongo normais, o genoma materno carrega mais dessa marca do que o genoma paterno logo após a fertilização, ajudando a silenciar cópias maternas específicas de genes enquanto permite que as cópias paternas funcionem.
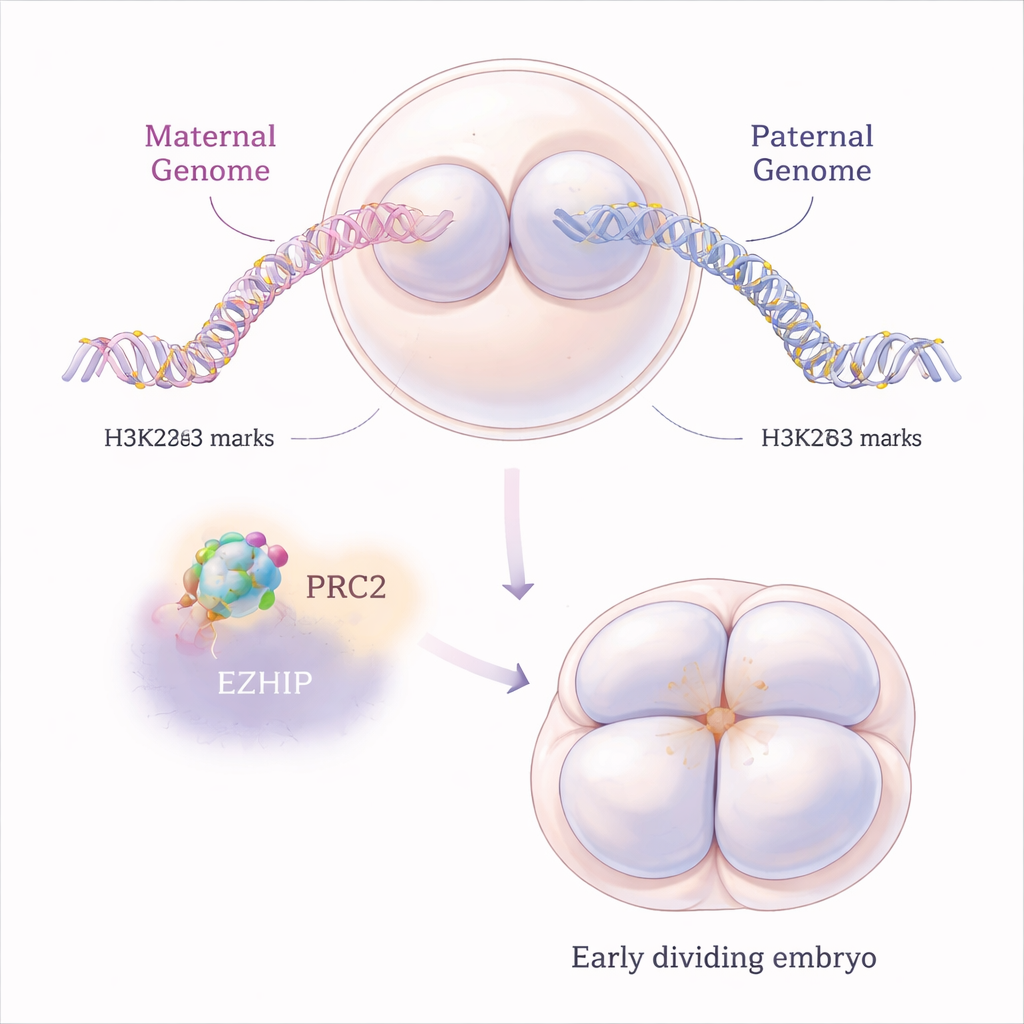
Um freio molecular em um reprimidor poderoso
A H3K27me3 é depositada na cromatina por uma grande máquina proteica chamada PRC2. Os autores focaram em EZHIP, uma proteína menos conhecida que se liga ao PRC2 e o desacelera. Os ovócitos de camundongo produzem muito RNA de Ezhip, e a proteína EZHIP resultante persiste nos embriões durante as primeiras divisões celulares. Estudando camundongos cujas mães não possuem Ezhip, os pesquisadores perguntaram o que acontece quando esse freio natural é removido. Eles descobriram que, sem EZHIP, óvulos e embriões precoces acumulavam marcas extras de H3K27me3, mas de uma maneira surpreendentemente “achatada”: em vez de domínios nítidos e bem definidos, a marca repressora se espalhava mais amplamente e borrava os padrões normais, afetando tanto cromossomos maternos quanto paternos.
Quando repressão demais quebra o imprinting
Usando métodos sensíveis de mapeamento genômico, a equipe mostrou que a assimetria habitual entre os pais nas paisagens de H3K27me3 é em grande parte perdida em embriões que se desenvolvem a partir de óvulos deficientes em Ezhip. Muitas regiões que normalmente mantêm H3K27me3 em apenas uma cópia parental agora a adquiriam em ambas, ou tiveram seus padrões esmaecidos. Essa mudança teve consequências importantes para genes imprintados que normalmente são controlados por H3K27me3 em vez de metilação do DNA. Em embriões de controle, esses genes tendem a ser expressos principalmente a partir do alelo paterno. Em embriões sem EZHIP materno, no entanto, os mesmos genes frequentemente eram ativados a partir de ambas as cópias parentais, e os níveis de RNA de muitos deles aumentaram em vez de permanecer silenciados duplamente.
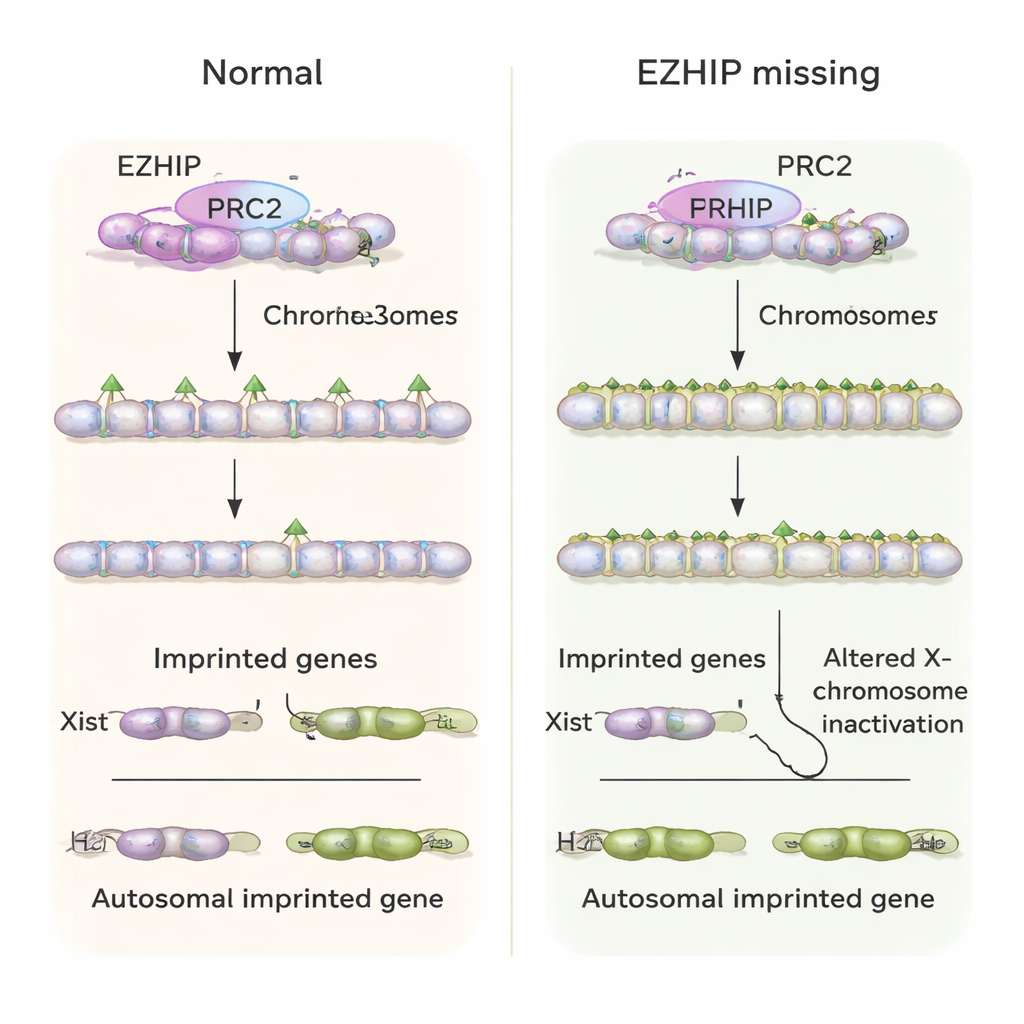
Controle do cromossomo X perturbado e saúde do embrião
Um gene imprintado dependente de H3K27me3 de grande importância é Xist, um RNA longo que reveste e inativa um cromossomo X em células femininas para equilibrar a dosagem gênica com os machos. Normalmente, embriões de camundongo precoces expressam Xist apenas a partir do X paterno em fêmeas, e não o expressam em machos. Na ausência de EZHIP materno, os autores observaram que embriões femininos frequentemente expressavam Xist em ambos os cromossomos X, enquanto embriões masculinos “inapropriadamente” ativavam Xist a partir de seu único X. Isso levou a padrões anormais de inativação de genes ligados ao X. Em nível do animal inteiro, camundongos nascidos de mães deficientes em Ezhip foram menos numerosos, e os embriões mostraram crescimento alterado e problemas em tecidos extraembrionários que sustentam a placenta, consistente com estresse de desenvolvimento duradouro causado pela falha inicial de imprinting.
Mais do bem pode ser prejudicial
Para um não especialista, pode parecer intuitivo que mais de uma marca de silenciamento como H3K27me3 simplesmente calaria mais genes. Em vez disso, este trabalho mostra que sobrecarregar o genoma com tais marcas no padrão errado pode, na verdade, minar sua capacidade de atuar como interruptores precisos. Ao remover EZHIP, os pesquisadores liberaram o PRC2, fazendo com que a H3K27me3 se espalhasse tão amplamente que os sinais de imprinting foram borrados e reguladores críticos como Xist ficaram descontrolados. O estudo destaca que embriões precoces dependem não apenas de ter as moléculas certas, mas de manter suas atividades afinadas de forma rígida para que os genomas materno e paterno sejam lidos em equilíbrio apropriado.
Citação: Diop, S., Richart, L., Petitalot, A. et al. H3K27me3-dependent imprinting and transcriptional regulation in early mouse embryos requires EZHIP-mediated restriction of PRC2 activity. Nat Commun 17, 1758 (2026). https://doi.org/10.1038/s41467-026-68467-4
Palavras-chave: epigenética, imprinting genômico, desenvolvimento embrionário precoce, inativação do cromossomo X, Polycomb PRC2