Clear Sky Science · pt
Triagem CRISPR in vivo identifica membros do complexo SAGA como reguladores-chave da hematopoese
Por que manter a produção de sangue em equilíbrio importa
Cada dia, seu corpo produz discretamente centenas de bilhões de novas células sanguíneas que transportam oxigênio, combatem infecções e estancam sangramentos. Essa produção contínua depende de raras “células-mãe” na medula óssea, chamadas células-tronco formadoras de sangue. Quando a máquina que controla essas células falha, as pessoas podem desenvolver anemia, imunidade enfraquecida ou cânceres como a leucemia. Este estudo faz uma pergunta simples, mas potente: entre os milhares de genes do nosso genoma, quais são realmente essenciais para manter a produção de células sanguíneas saudável e equilibrada?
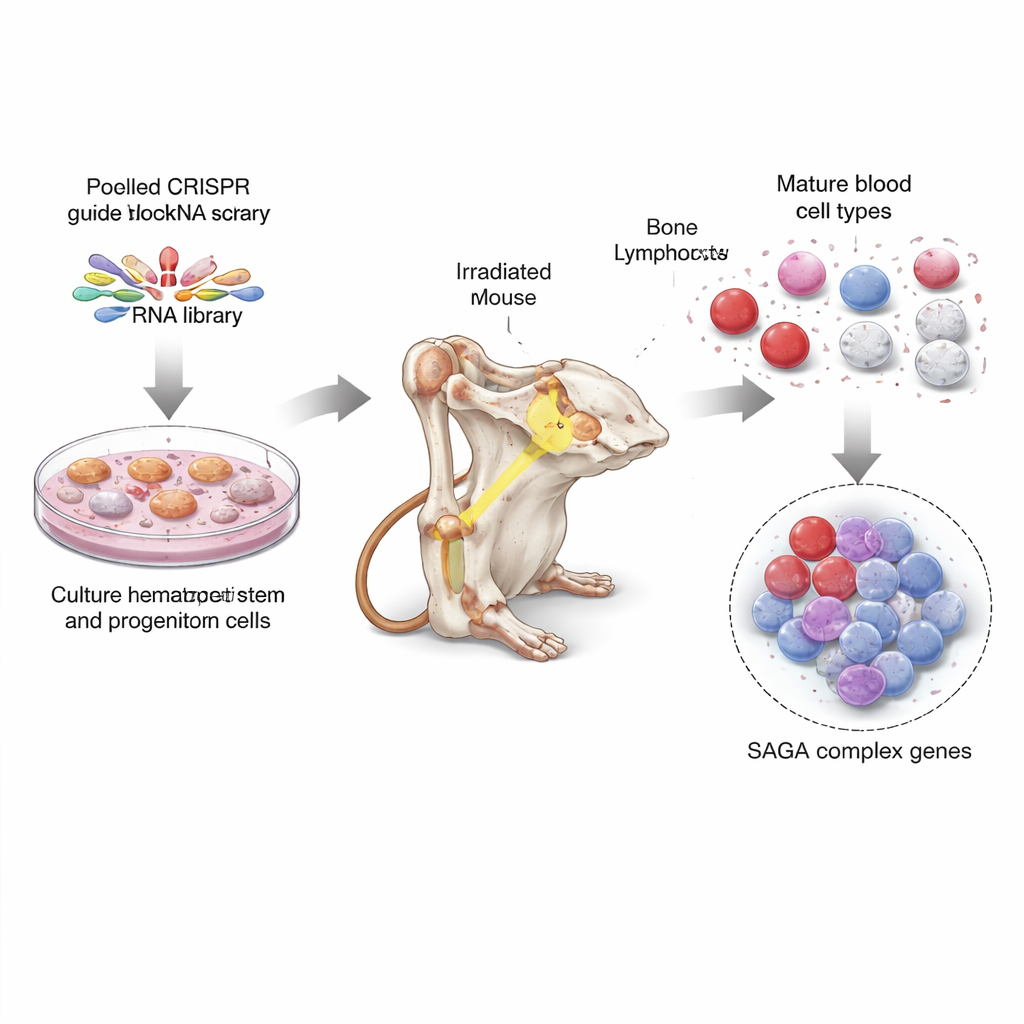
Uma caça ao tesouro em todo o genoma nas células-tronco de camundongos
Para enfrentar essa questão, os pesquisadores usaram o CRISPR, a ferramenta de edição genética frequentemente comparada a tesouras moleculares, para desligar quase todos os genes do genoma do camundongo, com dez guias por gene. Primeiro cultivaram grande número de células-tronco e progenitoras da medula óssea em condições especiais de cultura e depois infectaram essas células com pools de guias CRISPR de modo que cada célula carregasse a desativação de um gene diferente. Em seguida, transplantaram essas células editadas e misturadas em dezenas de camundongos irradiados, permitindo que as células reconstruíssem os sistemas sanguíneos dos animais. Meses depois, purificaram vários tipos de células sanguíneas maduras e células com características de tronco da medula óssea e leram quais guias CRISPR estavam sob ou sobre‑representados. Isso revelou quais perdas gênicas favoreciam células imaturas e quais sustentavam a produção de células sanguíneas totalmente formadas.
Um centro de controle oculto chamado SAGA ganha foco
Entre muitos reguladores conhecidos da formação sanguínea, surgiu um conjunto surpreendente de candidatos: vários componentes estruturais de um grande complexo protéico chamado SAGA, incluindo genes chamados Tada2b, Taf5l e Tada1. O SAGA não produz células sanguíneas diretamente; em vez disso, ajuda a ligar ou desligar outros genes marcando quimicamente proteínas que empacotam o DNA, chamadas histonas. Quando a equipe nocauteou individualmente esses componentes do SAGA e transplantou as células editadas em camundongos, observaram um padrão consistente. Células imaturas da medula óssea se acumularam, mas sua capacidade de amadurecer em leucócitos circulantes, eritrócitos e certos tipos de células imunes foi fortemente reduzida. Em essência, as células-tronco e progenitoras ficaram presas em um gargalo, incapazes de completar a jornada até se tornarem células sanguíneas plenamente funcionais.
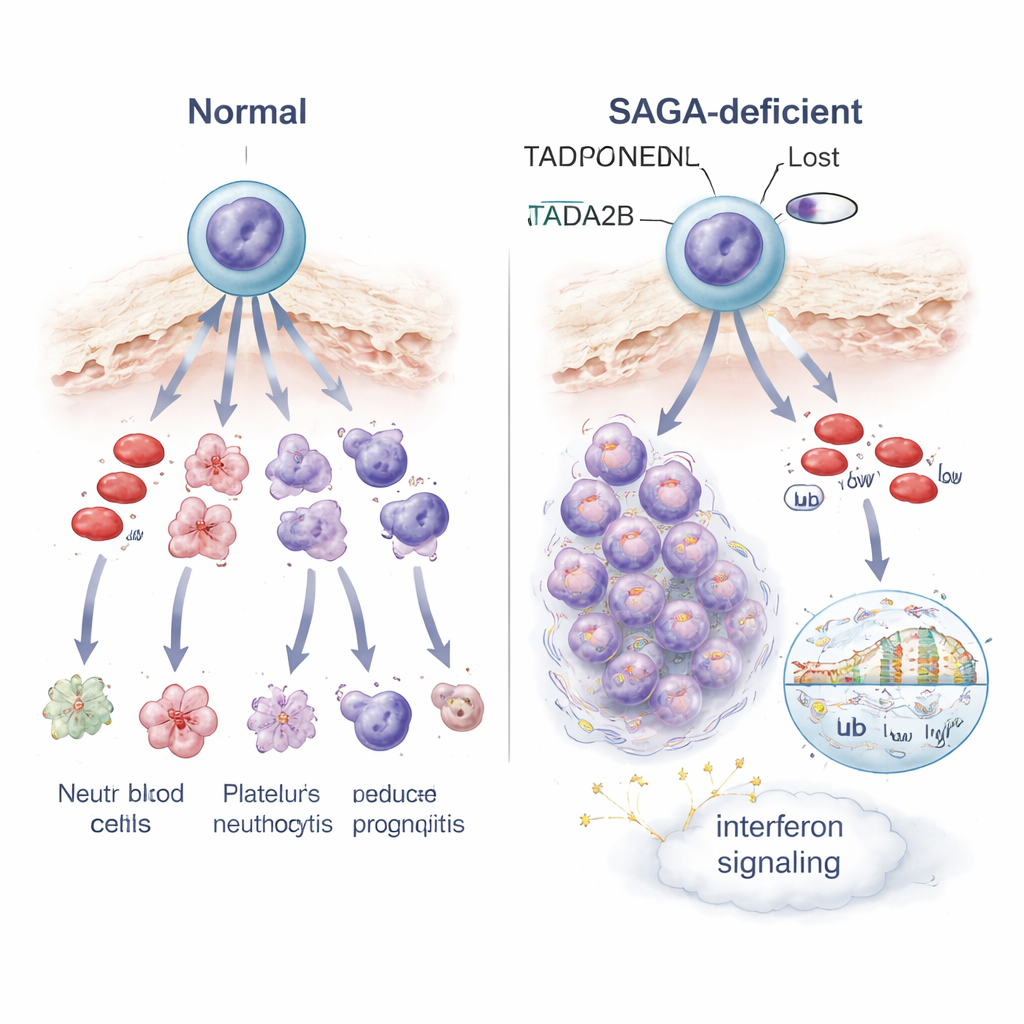
Como o controle gênico perturbado altera destino celular e sinais de estresse
Para entender o que dá errado dentro dessas células bloqueadas, os cientistas perfilaram a atividade gênica célula a célula e em amostras agregadas. A perda de Tada2b ou Taf5l reprogramou a atividade de muitos genes em células-tronco, com dois temas marcantes. Primeiro, genes envolvidos na sinalização por interferon — normalmente parte da defesa antiviral do organismo — foram ativados, indicando um alarme interno ou estado de estresse. Segundo, as mitocôndrias das células, as pequenas usinas que abastecem o trabalho celular, tornaram-se menos ativas, e as células alteradas ficaram mais sensíveis a um fármaco que atinge a produção de energia mitocondrial. No nível do empacotamento do DNA, células sem Tada2b mostraram níveis reduzidos de uma marca de histona associada a cromatina aberta e ativa, e mudanças em outra marca ligada à leitura dos genes. Essas alterações na química da cromatina provavelmente ajudam a explicar por que muitos genes, incluindo os que orientam a maturação sanguínea adequada, ficam desregulados.
De mecanismos básicos a modelos de doença
A equipe então perguntou se aumentar ou diminuir a atividade do SAGA poderia reverter esses efeitos. Forçar as células a produzir Tada2b extra reduziu a atividade de genes relacionados ao interferon e diminuiu a proporção de células com características de tronco, o espelho inverso do nocaute. Tratar células-tronco normais com um fármaco que inibe subunidades enzimáticas chave do SAGA reproduziu grande parte da assinatura da perda de Tada2b, reforçando a ideia de que a atividade de modificação de cromatina do SAGA é central para sua função. Por fim, os pesquisadores recorreram a um modelo de células humanas de síndrome mielodisplásica, um distúrbio pré-leucêmico em que a produção de sangue falha e as vias de interferon costumam estar elevadas. Quando nocauteavam componentes do SAGA nessas células humanas e as transplantavam em camundongos imunodeficientes, as células editadas ganharam vantagem de crescimento e novamente ativaram programas gênicos de interferon e mieloides, sugerindo que esse centro regulatório também molda o comportamento da doença.
O que isso significa para a saúde do sangue e terapias futuras
Para o leitor leigo, a mensagem central é que este estudo revela um potente centro de controle — o complexo SAGA — que ajuda as células-tronco formadoras de sangue a decidir quando permanecer imaturas, quando maturar e como evitar respostas de estresse prejudiciais. Quando partes-chave do SAGA desaparecem, as células-tronco se acumulam, mas não conseguem produzir células sanguíneas operacionais suficientes, enquanto sinais de estresse e respostas tipo antiviral aumentam e as mitocôndrias falham. Essas descobertas não só aprofundam nossa compreensão de como a produção saudável de sangue é mantida ao longo da vida, mas também sugerem que alterações sutis na atividade do SAGA podem contribuir para problemas sanguíneos relacionados à idade e distúrbios como a síndrome mielodisplásica. A longo prazo, mapear essa circuitaria de controle pode ajudar cientistas a projetar terapias que empurrem células-tronco defeituosas de volta a uma produção sanguínea equilibrada e resiliente.
Citação: Shankar, A., Olender, L., Hsu, I. et al. In vivo CRISPR screening identifies SAGA complex members as key regulators of hematopoiesis. Nat Commun 17, 1756 (2026). https://doi.org/10.1038/s41467-026-68465-6
Palavras-chave: células-tronco hematopoiéticas, triagem CRISPR, complexo SAGA, sinalização por interferon, síndrome mielodisplásica