Clear Sky Science · pt
Inferindo a arquitetura da cromatina em um único locus por meio da localização probabilística in situ do DNA
Como a forma 3D do DNA controla quando genes são ativados
Nosso DNA costuma ser imaginado como uma escada reta, mas dentro das células ele se dobra em laços e espirais intrincados. Essas formas importam: elas ajudam a decidir quais genes são ativados, quando e onde. Este estudo apresenta uma nova maneira de observar os arranjos 3D minúsculos do DNA ao redor de um único gene em embriões de mosca-das-frutas em desenvolvimento, revelando como mudanças sutis no dobramento do DNA podem alterar padrões de atividade gênica que moldam o plano corporal.
Observando o controle gênico em um embrião em desenvolvimento
À medida que um embrião se desenvolve, milhares de genes precisam ligar e desligar nos momentos certos. Muitas dessas decisões são tomadas por trechos curtos de DNA chamados enhancers, que podem estar a dezenas de milhares de letras de distância dos genes que regulam. Para funcionar, os enhancers devem se aproximar fisicamente do gene alvo no espaço 3D, fazendo com que o DNA forme laços para que sítios distantes se toquem. Mas esses laços são minúsculos, dinâmicos e difíceis de ver. Os autores concentraram-se em um único gene, brinker (brk), em Drosophila. Esse gene ajuda a padronizar o embrião inicial, ligando-se em uma faixa ao longo do lado do ovo. Três elementos regulatórios próximos — dois enhancers (E1 e E2) e um elemento promotor-próximo (PPE) ao lado do gene — cooperam para produzir esse padrão preciso.
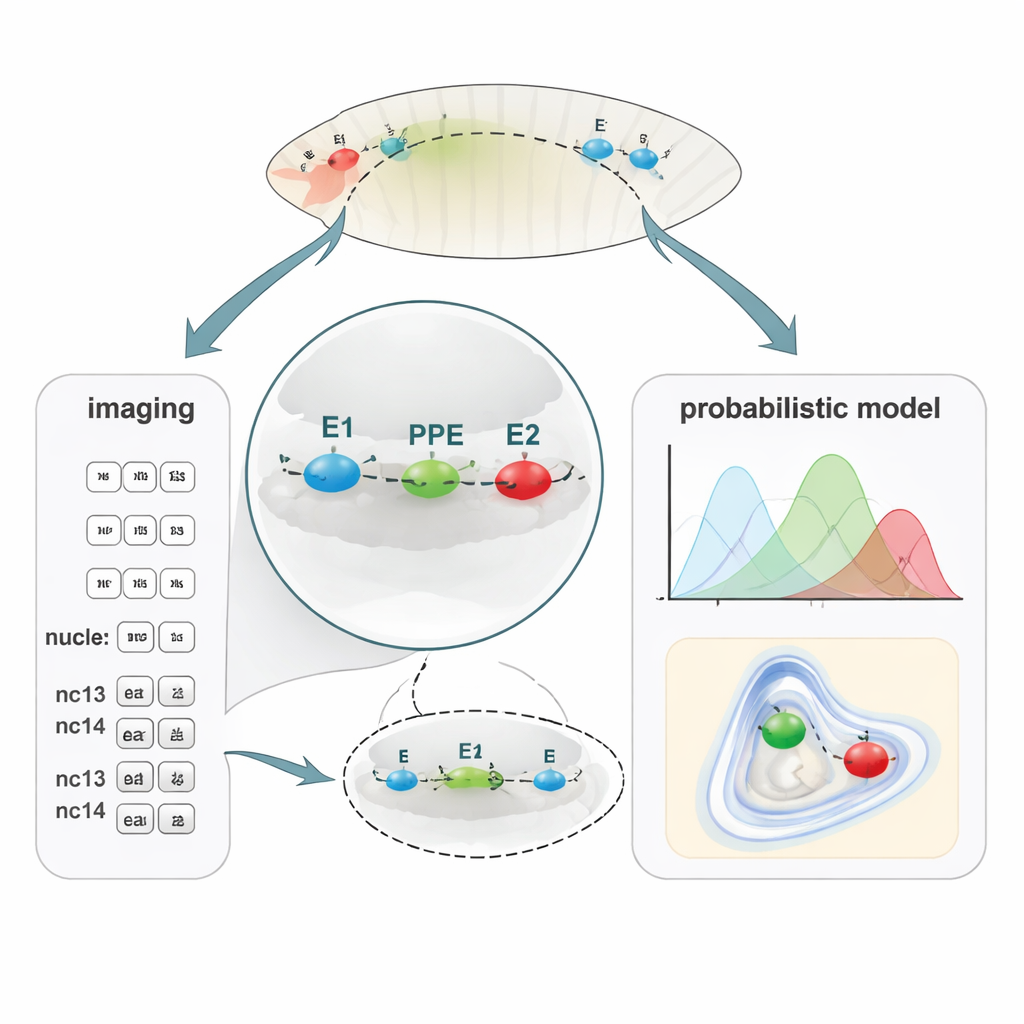
Uma nova maneira de mapear distâncias minúsculas do DNA
Para ligar o dobramento do DNA à atividade gênica, a equipe desenvolveu o PLOTTED (Localização Probabilística de Distâncias de Elementos Alvo marcados por Oligopaint). Primeiro, eles usaram um método de marcação do DNA chamado Oligopaint FISH para anexar três corantes fluorescentes diferentes às regiões E1, PPE e E2 em embriões fixos de mosca. Usando um microscópio confocal de super-resolução, mediram distâncias 3D entre esses três pontos coloridos em dezenas de milhares de núcleos em embriões ao longo de ciclos nucleares sucessivos, desde pouco antes de a atividade gênica começar (pré-nc13) até estágios posteriores (nc13 e nc14). Em seguida, alimentaram todas essas distâncias em um pipeline computacional personalizado que filtra medições ruidosas e constrói mapas de probabilidade mostrando onde cada elemento tem maior probabilidade de se situar em relação aos outros. Em vez de um único “laço” estático, o PLOTTED produz uma paisagem de formas cromatínicas prováveis em cada estágio do desenvolvimento.
Quando o DNA se compacta, o gene desperta
Em embriões normais, os pesquisadores descobriram que, ao alcançar o ciclo nuclear 13, ambos os enhancers se aproximam do PPE: o bairro local do DNA ao redor do gene brk torna-se mais compacto. Depois desse ponto, as distâncias entre os três elementos permanecem relativamente estáveis. Importante, esse momento coincide com o início da expressão de brk, sugerindo que o apertamento da configuração do DNA ajuda a permitir que o gene seja ativado. O PLOTTED também revelou que esse arranjo compacto aparece com mais frequência em regiões do embrião onde brk está ativo, e configurações mais frouxas dominam onde o gene é reprimido, reforçando a ligação entre arquitetura 3D e transcrição.
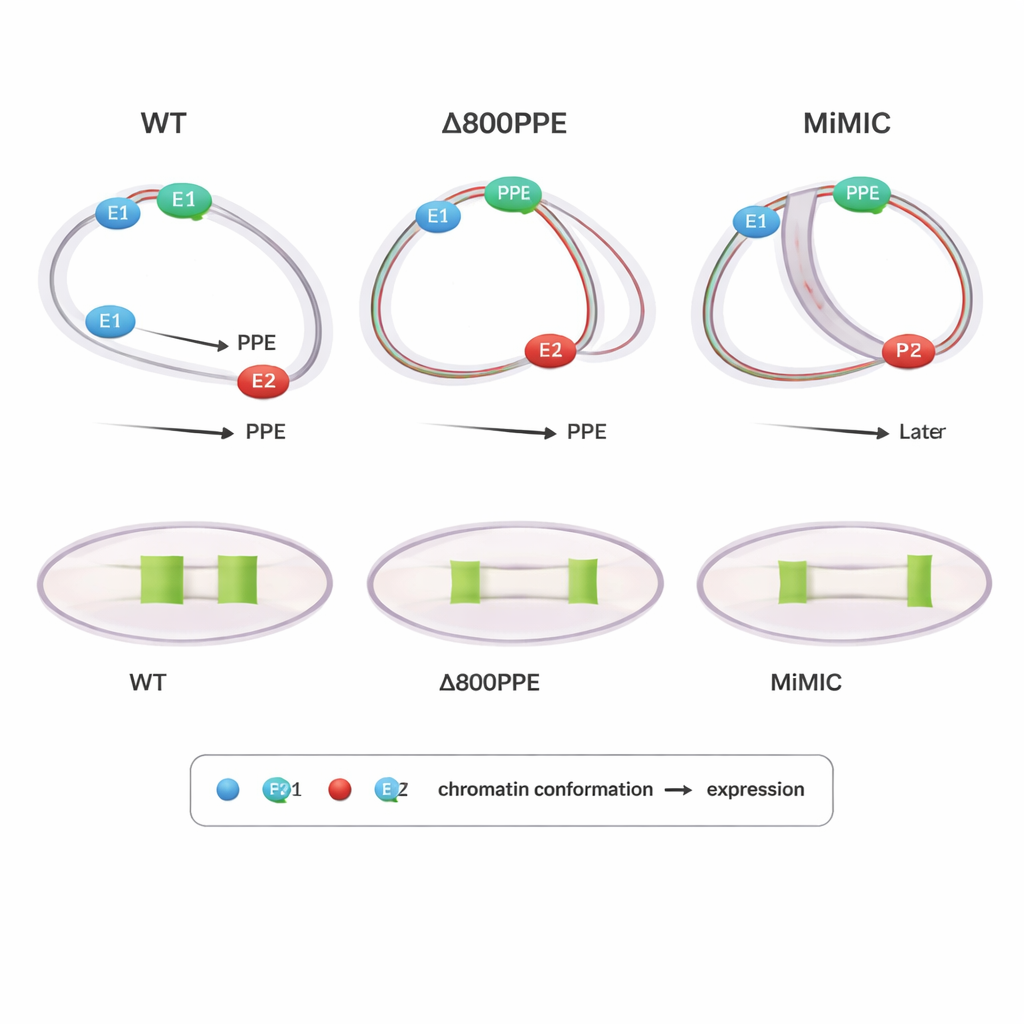
Mutações revelam como tempo e posição importam
Para sondar causa e efeito, os autores examinaram moscas com mudanças engenheiradas no locus brk. Em um mutante, 800 pares de bases do PPE foram deletados, enfraquecendo esse elemento central; em outro, uma cassete de DNA de 7,3 kilobases (MiMIC) foi inserida entre E1 e o PPE, efetivamente afastando-os e adicionando um promotor extra. Ambos os mutantes mostraram expressão de brk atrasada ou reduzida. O PLOTTED mostrou o porquê: na linha com deleção do PPE, a compactação das distâncias entre o PPE e ambos os enhancers ocorreu mais tarde do que o normal, e em estágios tardios o PPE permaneceu muito próximo de E1, impedindo que E2 dirigisse o padrão de expressão amplo observado no tipo selvagem. Na linha MiMIC, o PPE associou-se cedo e fortemente com E2 e só mais tarde aproximou-se de E1, novamente perturbando a passagem normal entre enhancers. Esses resultados sugerem que não é apenas se os elementos se juntam, mas quando e com qual parceiro eles ficam mais próximos, que é crucial para a saída gênica correta.
O dobramento do DNA varia pelo embrião
Porque o PLOTTED preserva informação espacial dentro de embriões intactos, a equipe também pôde perguntar se a arquitetura do DNA difere em várias regiões do corpo. Comparando zonas laterais onde brk está ativo com zonas ventrais onde ele é reprimido, descobriram que os três elementos ficam mais próximos nas regiões ativas e se afastam nas áreas reprimidas. Ao longo do eixo cabeça-cauda, observaram que as distâncias E1–PPE mudam de forma diferente na frente versus na parte traseira do embrião, sugerindo que sinais regionais ajustam a arquitetura da cromatina para afinar padrões de expressão gênica. Essas descobertas sustentam a visão de que o arranjo 3D do DNA regulador é dependente do contexto, acompanhando tanto o tempo quanto a posição no organismo em desenvolvimento.
Por que isso importa além das moscas
Em termos simples, este estudo mostra que o modo como o DNA se dobra ao redor de um único gene está intimamente ligado a quando e onde esse gene é ativado. O novo método PLOTTED fornece uma maneira prática de mapear esses bairros microscópicos do DNA em tecidos intactos usando microscópios amplamente disponíveis e química direta, combinados com modelagem probabilística poderosa. Embora demonstrado em embriões de mosca, o método pode ser aplicado a muitos organismos e modelos de doença. À medida que os cientistas descobrem cada vez mais que cromatina mal dobrada está na raiz de distúrbios do desenvolvimento e cânceres, ferramentas como o PLOTTED ajudarão a revelar como pequenas mudanças na disposição 3D de enhancers e genes podem repercutir em grandes alterações no destino celular e na saúde.
Citação: Le, M.T., McGehee, J., Dunipace, L. et al. Inferring chromatin architecture at a single locus through probabilistic in situ DNA localization. Nat Commun 17, 1752 (2026). https://doi.org/10.1038/s41467-026-68460-x
Palavras-chave: arquitetura da cromatina, interações enhancer-promotor, embriogênese de Drosophila, regulação gênica, imagens de super-resolução