Clear Sky Science · pt
Células da crista neural derivadas DKK1 e NEDD4 modulam a sinalização Wnt no segundo campo cardíaco para orquestrar o desenvolvimento do trato de saída
Por que os pequenos construtores do coração importam
O coração do embrião precoce começa como um tubo simples, mas precisa remodelar-se rapidamente em um órgão complexo que bombeia sangue tanto para o corpo quanto para os pulmões. Pequenos desvios nesse processo de construção podem causar defeitos congênitos sérios, incluindo condições que exigem cirurgia logo após o nascimento. Este estudo revela como dois grupos de células se comunicam enquanto moldam a principal via de saída do coração e identifica um erro molecular que pode contribuir para doenças cardíacas congênitas em camundongos e humanos.
Dois times construindo a rampa de saída do coração
A porção do coração que conduz o sangue para fora dos ventrículos — o trato de saída — forma-se a partir de uma região chamada segundo campo cardíaco. As células nessa área precisam permanecer como “progenitores” flexíveis tempo suficiente para serem adicionadas ao trato de saída em crescimento e, então, se transformar em músculo maduro no momento certo. Logo ao lado delas viajam as células da crista neural, uma população migratória que contribui para a formação das grandes artérias e válvulas. Trabalhos anteriores sugeriam que essas células da crista neural de algum modo influenciam o segundo campo cardíaco, mas como essa comunicação ocorria era desconhecido. 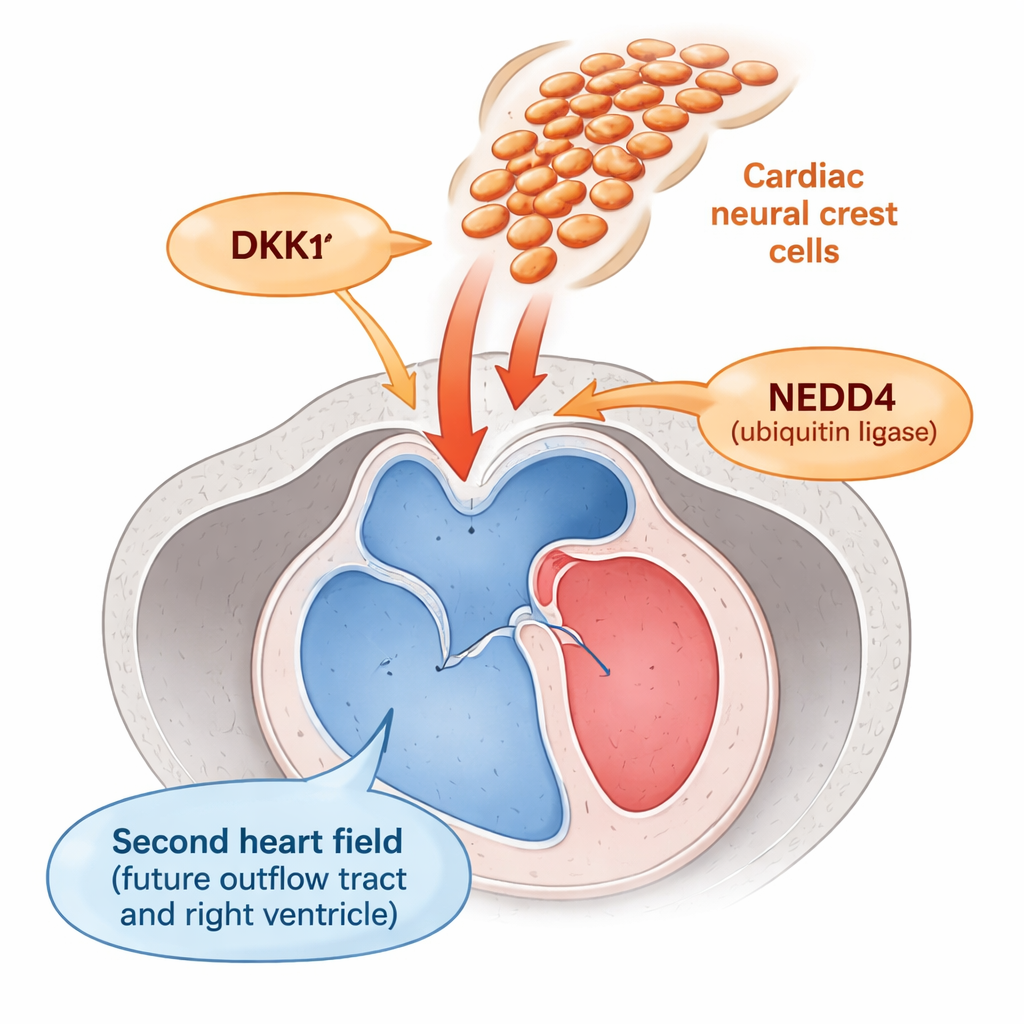
Um dimmer molecular para sinais de crescimento
Os autores descobriram que as células da crista neural atuam como um dimmer para um sinal de crescimento chave chamado Wnt, que mantém os progenitores em divisão e atrasa sua maturação. Eles constataram que as células da crista neural são uma fonte importante de DKK1, uma pequena proteína secretada que inibe a sinalização Wnt nas células vizinhas. O próprio DKK1 é normalmente controlado por NEDD4, uma proteína que marca o DKK1 para eliminação. Em embriões de camundongo que careciam de Nedd4 especificamente nas células da crista neural, DKK1 acumulou-se em níveis anormalmente altos. Esse excesso de DKK1 reduziu a atividade Wnt no segundo campo cardíaco vizinho, evidenciado pela redução de beta‑catenina nuclear — uma medida padrão da sinalização Wnt — e por níveis mais baixos de múltiplos genes responsivos a Wnt.
Quando o timing falha, a geometria do coração se compromete
Demais DKK1 e pouca Wnt tiveram uma consequência clara: as células do segundo campo cardíaco começaram a se transformar em músculo cardíaco cedo demais. Marcadores de músculo maduro apareceram precocemente nessa zona de progenitores, e havia menos células indiferenciadas disponíveis para alongar o trato de saída. Ao rastrear células em divisão ao longo do tempo, a equipe mostrou que menos células do segundo campo cardíaco foram incorporadas ao trato de saída nos mutantes. Como resultado, o trato de saída ficou mais curto e rotacionou de forma incorreta, levando ao desalinhamento entre as grandes artérias e os ventrículos. Esses erros estruturais lembraram defeitos conotruncais humanos, como ventrículo direito com dupla saída, e malformações semelhantes observadas em camundongos com nocaute total de Nedd4.
Provando o papel do sinal e um elo com a doença humana
Para confirmar que a alteração na sinalização Wnt realmente causava esses problemas, os pesquisadores manipularam a via com fármacos em camundongas prenhes. Bloquear Wnt em embriões por outro lado saudáveis os levou aos mesmos defeitos de diferenciação prematura e rotação observados quando Nedd4 foi perdido, enquanto reduzir a dosagem de Dkk1 no contexto deficiente em Nedd4 resgatou parcialmente o tamanho e a rotação do trato de saída. Finalmente, a equipe identificou uma criança com Tetralogia de Fallot que carregava uma variante rara herdada em NEDD4 que enfraquecia sua capacidade de marcar DKK1 para degradação. Camundongos modificados para portar a mesma variante de Nedd4 desenvolveram defeitos na parede e no septo cardíaco no lado direito, apoiando a ideia de que controle defeituoso de NEDD4–DKK1 pode contribuir para doenças cardíacas congênitas humanas. 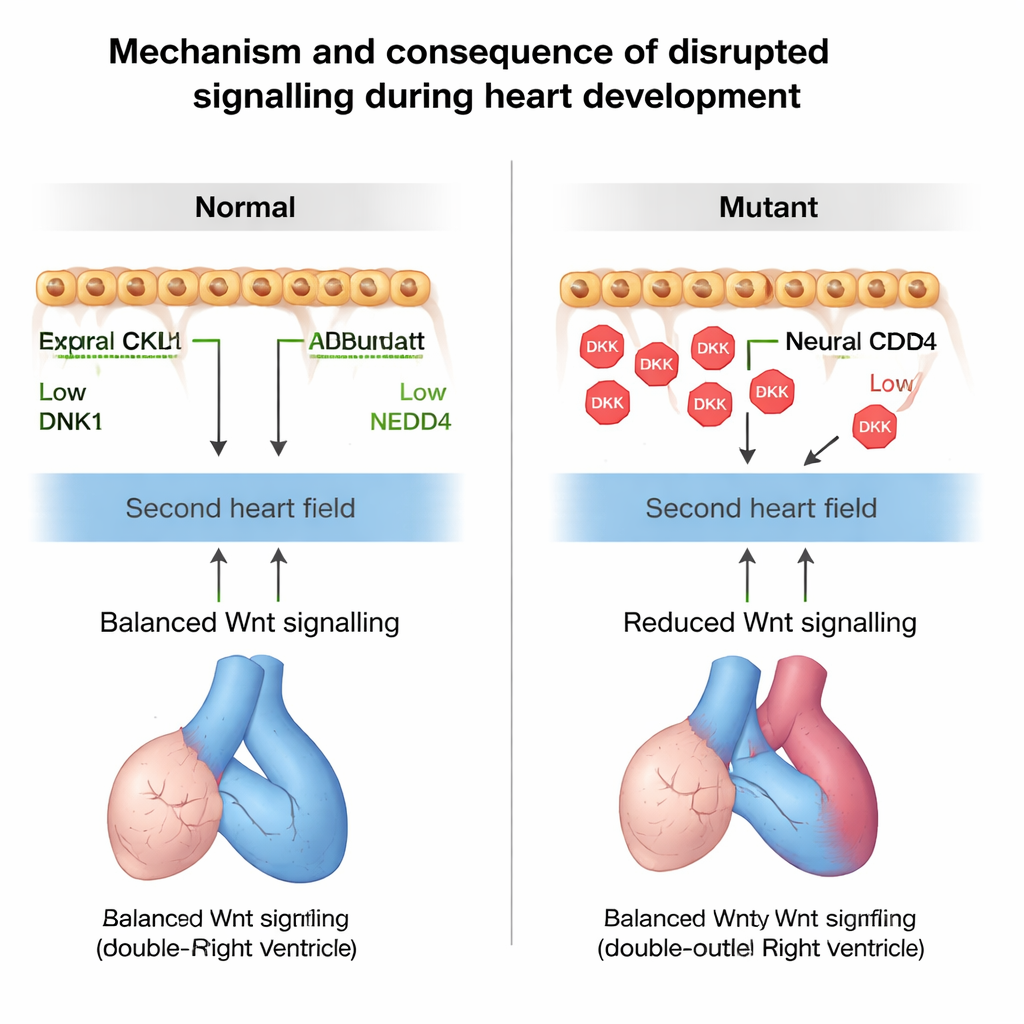
O que isso significa para entender defeitos cardíacos
Para não‑especialistas, a mensagem principal é que a “rampa de saída” do coração depende do tempo preciso em que seus blocos de construção cessam de se multiplicar e começam a se tornar músculo. Esse timing é controlado não apenas pelo tecido cardíaco em si, mas também por células da crista neural vizinhas que afinam um sinal de crescimento via o par NEDD4–DKK1. Quando esse dimmer molecular fica excessivamente desligado, o trato de saída fica subdesenvolvido e desalinhado, levando a defeitos congênitos sérios. Ao mapear essa via e conectá‑la a uma variante genética humana, o estudo oferece novas pistas sobre como alguns defeitos cardíacos congênitos surgem e destaca potenciais alvos moleculares para diagnóstico ou intervenção futuros.
Citação: Wiszniak, S., Alankarage, D., Lohraseb, I. et al. Neural crest cell-derived DKK1 and NEDD4 modulate Wnt signalling in the second heart field to orchestrate outflow tract development. Nat Commun 17, 1751 (2026). https://doi.org/10.1038/s41467-026-68459-4
Palavras-chave: doença cardíaca congênita, desenvolvimento do coração, células da crista neural, sinalização Wnt, trato de saída cardíaco