Clear Sky Science · pt
Af-CUT&Tag: um método sensível e sem anticorpos para mapeamento de cromatina usando etiquetas geneticamente codificadas e ligantes de alta afinidade fundidos ao Tn5
Espiando a sala de controle do nosso DNA
Cada célula do seu corpo decide constantemente quais genes ativar ou silenciar, moldando desde a reparação do fígado até o risco de câncer. Cientistas estudam essas decisões mapeando onde proteínas-chave se posicionam no DNA, mas as melhores ferramentas para isso historicamente dependem de anticorpos frágeis e caros que nem sempre funcionam bem. Este trabalho apresenta uma nova forma, sem anticorpos, de traçar essas interações DNA–proteína, chamada Af-CUT&Tag, que é mais sensível, mais confiável e suficientemente potente para funcionar até em amostras minúsculas e em células individuais.
Por que os anticorpos nos limitam
Métodos clássicos de mapeamento de cromatina precisam de anticorpos—grandes proteínas em forma de Y que reconhecem uma proteína-alvo específica—para guiar uma enzima aos locais corretos no DNA. Quando funcionam perfeitamente, esses anticorpos permitem aos pesquisadores ver onde fatores de transcrição e outros reguladores estão ligados no genoma. Mas na prática os anticorpos podem ser difíceis de obter, inconsistentes em qualidade e bloqueados por modificações químicas comuns nas proteínas, como fosforilação ou acetilação. Esses problemas podem turvar os mapas resultantes, limitar as proteínas que podem ser estudadas e dificultar a comparação de resultados entre laboratórios ou experimentos.
Etiquetas minúsculas e ligantes inteligentes substituem anticorpos
Af-CUT&Tag evita completamente o uso de anticorpos ao dar à proteína de interesse uma pequena etiqueta genética. Usando edição genômica por CRISPR, os pesquisadores fundem pequenas etiquetas peptídicas, como HiBiT ou ALFA, à proteína natural dentro das células ou tecidos. Em seguida, usam proteínas parceiras projetadas—ligantes de alta afinidade que reconhecem essas etiquetas—fundidas diretamente à enzima Tn5, que corta o DNA e anexa adaptadores para sequenciamento. Quando a fusão ligante–Tn5 se liga à etiqueta na proteína de interesse, ela corta o DNA nas proximidades e marca esses sítios para sequenciamento. Como as etiquetas são muito pequenas e a fusão ligante–Tn5 é bem menor que um anticorpo, esse sistema entra facilmente nas células e nos núcleos, liga-se com precisão excepcional e não é afetado por modificações químicas na proteína-alvo. 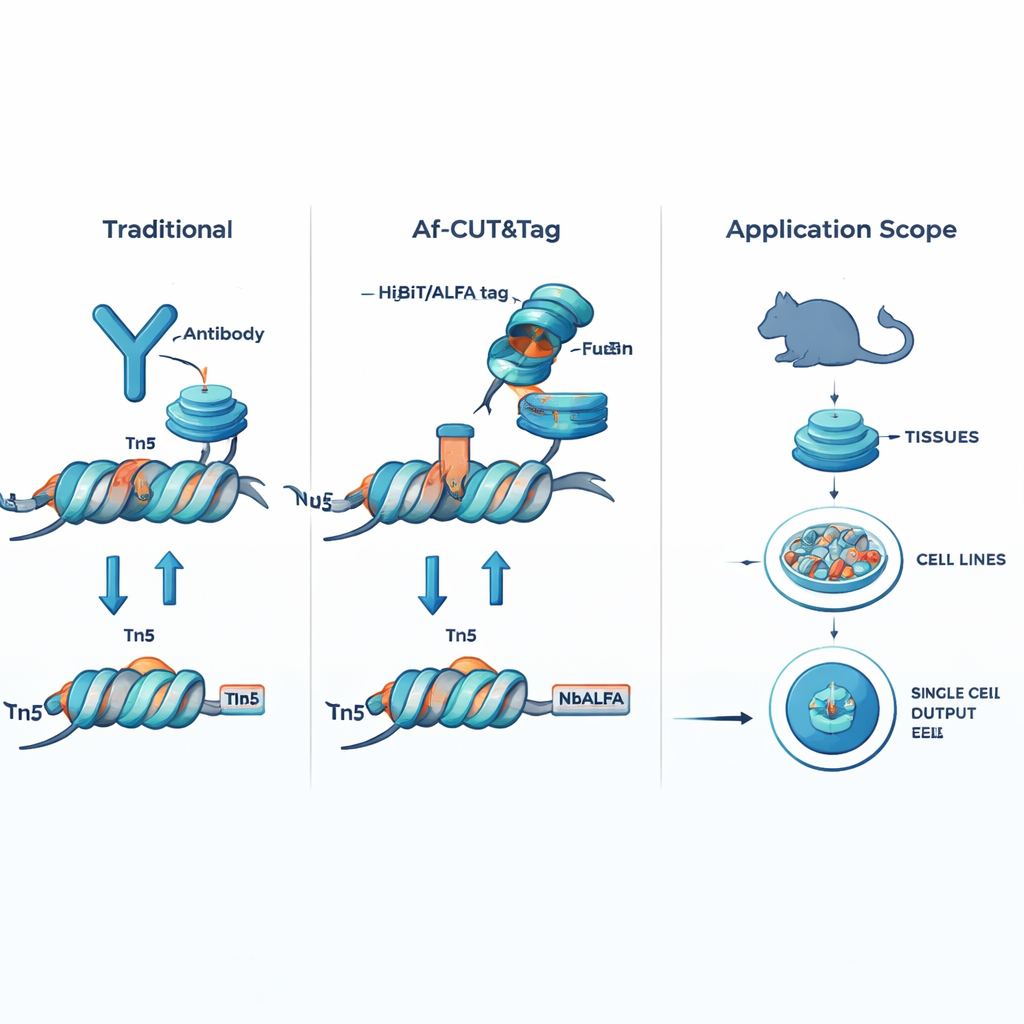
Mapas mais nítidos a partir de menos células
A equipe primeiro demonstrou que suas fusões ligante–Tn5 ainda capturam fortemente as etiquetas e cortam o DNA de forma eficiente. Depois compararam Af-CUT&Tag com métodos de ponta baseados em anticorpos para mapear a RNA polimerase II, a enzima que lê genes codificadores de proteínas, e a proteína CTCF, um importante organizador da estrutura do genoma. Em linhas celulares humanas, Af-CUT&Tag produziu sinal mais limpo em pontos de início de genes, menos cortes fora do alvo em regiões de DNA abertas mas irrelevantes, e bibliotecas de sequenciamento de qualidade superior. Notavelmente, gerou mapas robustos a partir de apenas cerca de 500 células, e a mesma estratégia pôde ser adaptada a muitos ligantes diferentes direcionados a características distintas do DNA. O método também foi estendido a células únicas através da indexação por códigos de barras dos fragmentos de cada célula, permitindo a construção de mapas de cromatina detalhados célula a célula.
Acompanhando a reparação do fígado em tempo real
Para demonstrar o que essa tecnologia pode revelar em animais vivos, os autores aplicaram Af-CUT&Tag à regeneração do fígado de camundongos. Usaram vírus e CRISPR para adicionar etiquetas HiBiT a dois reguladores-chave da via Hippo, YAP1 e TAZ, que ajudam a controlar o tamanho do órgão e a reparação. Após a remoção cirúrgica de parte do fígado, isolaram núcleos de células hepáticas antes da operação e 24 horas depois, e então usaram Af-CUT&Tag para ver onde YAP1 e TAZ estavam ligados no genoma. Os mapas mostraram que, logo após a lesão, essas proteínas reduzem sua presença em genes que impulsionam o processamento e a síntese de lipídios, enquanto as células do fígado acumulam temporariamente gotículas de gordura. Ao mesmo tempo, YAP1/TAZ aumentam a ligação em genes envolvidos na depuração do heme, um componente potencialmente tóxico do sangue, e em Mir122, um gene que produz um microRNA altamente enriquecido no fígado.
miR-122 como guardião da regeneração
miR-122 é uma pequena molécula de RNA que ajuda a afinar a atividade de muitos outros genes. Usando Af-CUT&Tag, os pesquisadores observaram ligação mais forte de YAP1/TAZ nas proximidades da região de Mir122, juntamente com cromatina mais aberta e marcas químicas aumentadas associadas à ativação gênica. Experimentos confirmaram que os níveis de miR-122 sobem durante a janela inicial de regeneração. Quando a equipe removeu especificamente miR-122 em células hepáticas de camundongos, os animais exibiram maior acúmulo de gordura, respostas inflamatórias mais intensas e menos células hepáticas entrando no ciclo celular após a cirurgia. Em conjunto, esses resultados sugerem que YAP1/TAZ ajudam o fígado a manter um equilíbrio cuidadoso durante a reparação: estocando gordura brevemente para energia, limitando danos do heme e da inflamação, e usando miR-122 para conter o estresse excessivo enquanto promovem o crescimento do tecido. 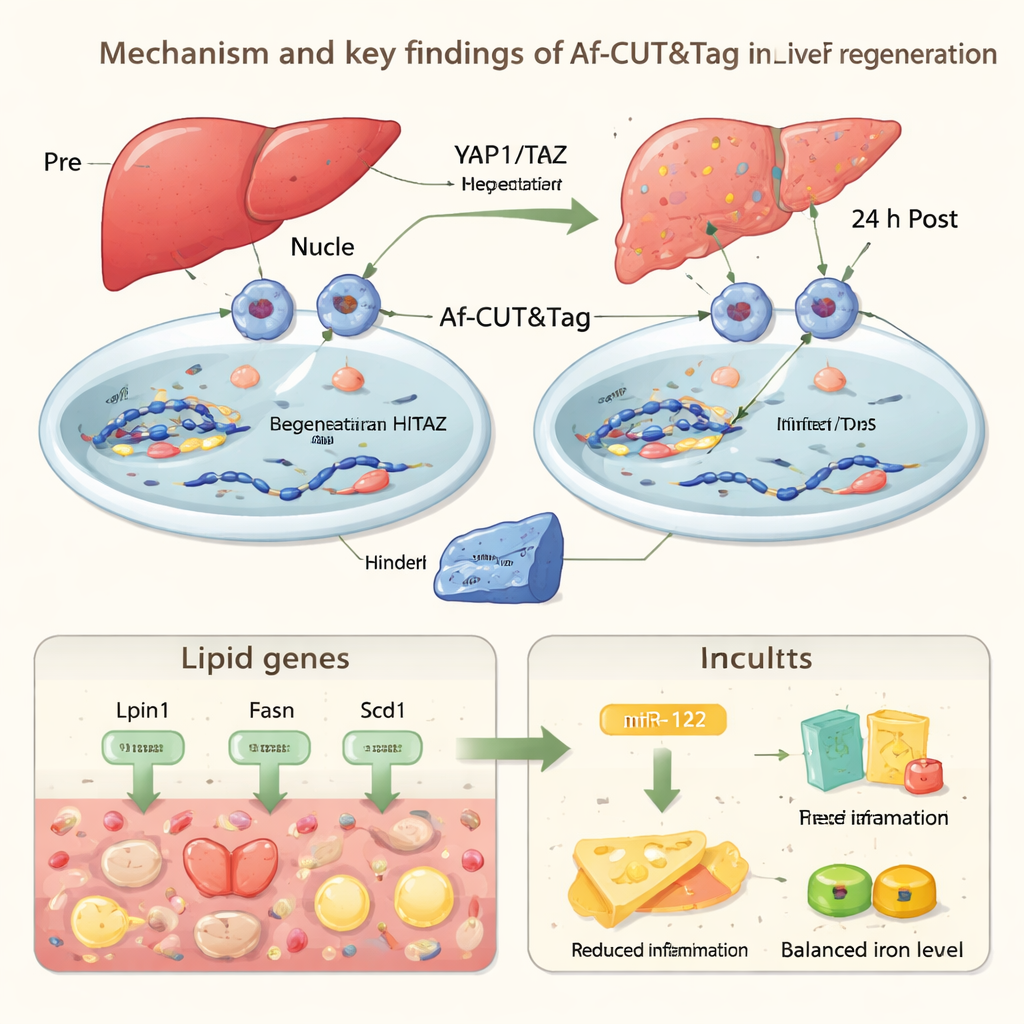
Uma nova lente versátil sobre o controle gênico
Af-CUT&Tag oferece uma forma modular e sem anticorpos de ver onde proteínas-chave se posicionam no DNA em linhas celulares, tecidos e até em células individuais. Ao substituir anticorpos imprevisíveis por pequenas etiquetas genéticas e ligantes projetados, ele fornece mapas mais nítidos e mais reprodutíveis com muito menos células. Aplicado à regeneração do fígado, revelou como YAP1 e TAZ coordenam metabolismo, manejo do ferro e o microRNA miR-122 para apoiar a reparação inicial. Conforme a edição genômica e os ligantes de desenho customizado continuam a melhorar, essa estratégia pode se tornar uma ferramenta padrão para dissecar como a regulação gênica funciona corretamente no desenvolvimento e na regeneração—e como falha em doenças como câncer e insuficiência hepática.
Citação: Wang, X., Deng, X., Qiu, L. et al. Af-CUT&Tag: a sensitive and antibody-free chromatin profiling method using genetically encoded tags and high-affinity binders fused to Tn5. Nat Commun 17, 1746 (2026). https://doi.org/10.1038/s41467-026-68454-9
Palavras-chave: mapeamento de cromatina, epigenética, regeneração do fígado, YAP1 TAZ, microRNA-122