Clear Sky Science · pt
Variantes funcionais em 1p36.23 conferem risco de esquizofrenia ao modular RERE
Por que pequenas mudanças no DNA importam para a saúde mental
A esquizofrenia é uma doença mental grave que afeta como as pessoas pensam, sentem e se relacionam. Ela tem forte hereditariedade, mas a maioria das alterações genéticas envolvidas são ajustes pequenos e dispersos no nosso DNA. Este estudo foca em uma dessas regiões do genoma e mostra, passo a passo, como duas variantes sutis do DNA podem alterar o desenvolvimento e a comunicação entre células cerebrais de maneiras que podem aumentar o risco de esquizofrenia de uma pessoa. 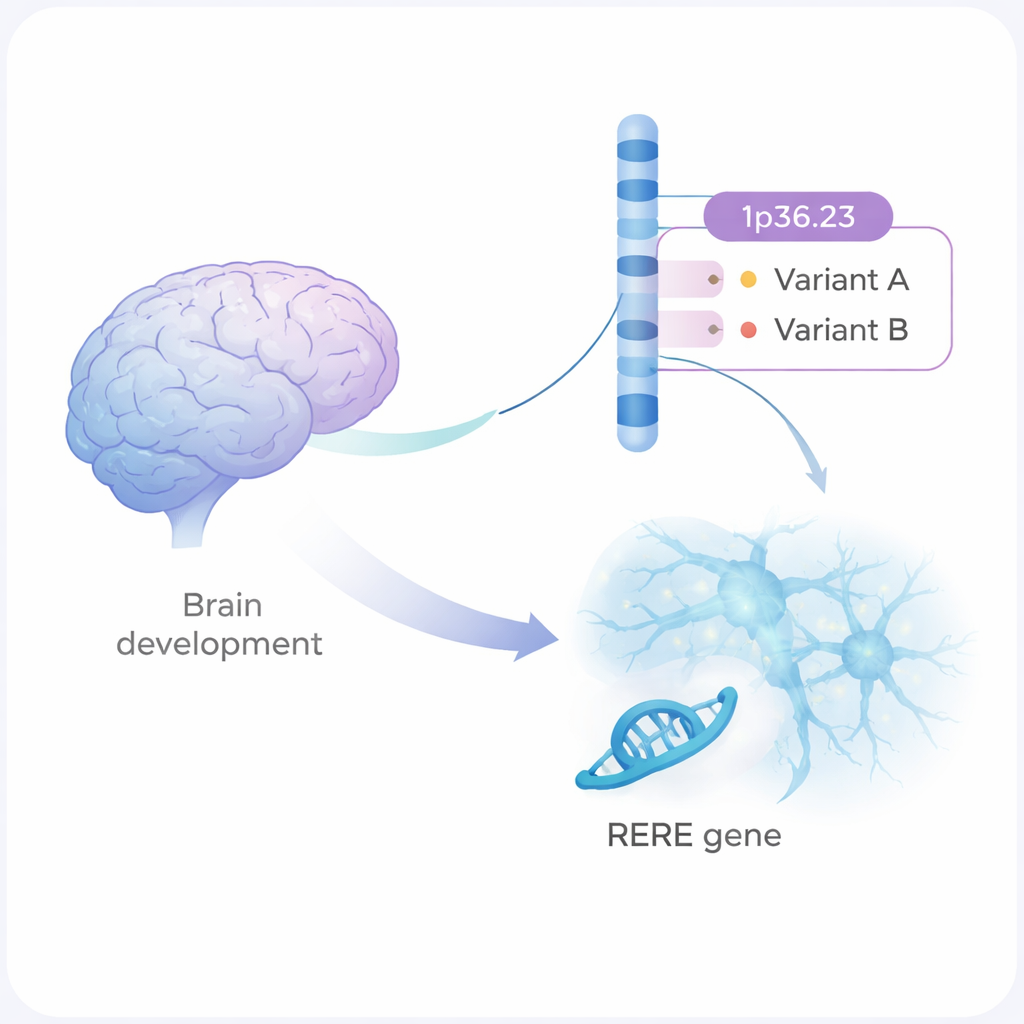
Um ponto quente genético no cromossomo 1
Grandes estudos genéticos identificaram mais de 300 regiões do genoma humano associadas à esquizofrenia. Uma delas é um trecho do DNA no cromossomo 1, chamado 1p36.23. Até agora, os cientistas não sabiam quais mudanças exatas nessa região, ou qual gene, eram as responsáveis. Os autores combinaram genética estatística com experimentos de laboratório e apontaram duas variantes do DNA, denominadas rs159961 e rs301792, localizadas dentro do gene RERE. Essas variantes não alteram a proteína RERE em si; em vez disso, estão em zonas regulatórias — "chaves" — dentro do gene que controlam quão fortemente o RERE é ativado.
Como variantes de risco aumentam o volume do RERE
A equipe primeiro investigou se essas duas variantes realmente funcionam como chaves regulatórias. Usando ensaios repórter — testes em que um fragmento de DNA dirige um gene que produz luz — eles mostraram que as versões associadas à esquizofrenia de rs159961 e rs301792 atuam como reforçadores (enhancers) mais fortes em células do tipo nervoso, mas não em tipos celulares não relacionados. Testes bioquímicos de ligação revelaram o motivo: a forma de risco de uma variante enfraquece a afinidade de REST, uma proteína que normalmente reprime atividade gênica, enquanto a forma de risco da outra aumenta a ligação de POLR2A, um componente central da maquinaria de transcrição. Juntas, essas mudanças no recrutamento de proteínas elevam a atividade dos segmentos enhancers e impulsionam a expressão de RERE.
Do RERE aumentado ao crescimento alterado de células cerebrais
Em seguida, os pesquisadores investigaram o que o excesso de RERE faz no cérebro. Eles encontraram níveis mais altos de RERE em tecido cerebral de pessoas que morreram com esquizofrenia em comparação com indivíduos não afetados. Para modelar isso, elevaram artificialmente os níveis de RERE em células-tronco neurais de camundongo — as células imaturas que dão origem a neurônios e glia. Quando RERE foi superexpresso, essas células-tronco dividiram-se menos, ficaram retidas em uma fase tardia do ciclo celular e geraram menos neurônios maduros, enquanto outros tipos celulares foram pouco afetados. Em neurônios em cultura, excesso de RERE reconfigurou os padrões de ramificação e reduziu o número e o tipo de pequenas protrusões chamadas espinhas dendríticas, onde as sinapses se formam. Essas alterações são coerentes com evidências de longa data de que a esquizofrenia envolve desenvolvimento cerebral perturbado e perda de espinhas. 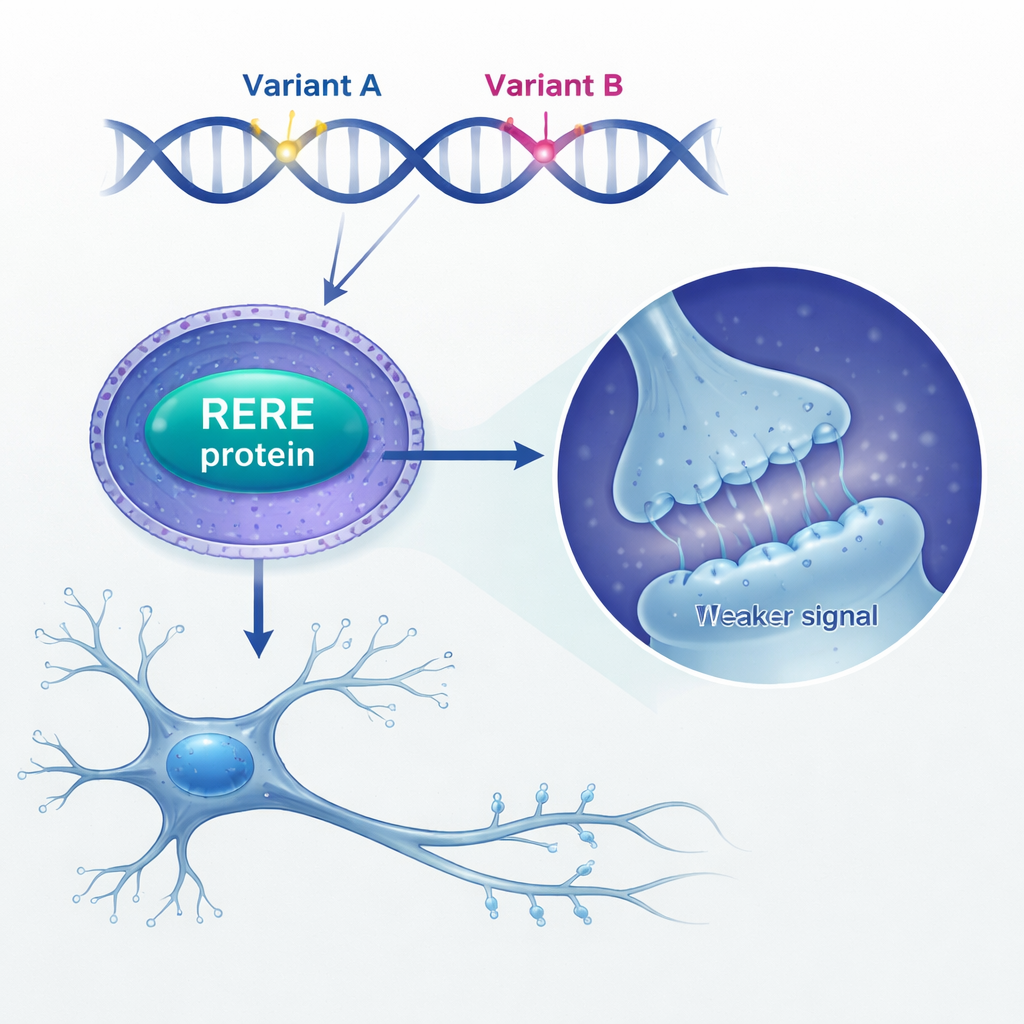
Interrompendo a "conversa" de glutamato do cérebro
Ao examinar mais de perto a atividade gênica, a equipe descobriu que a superexpressão de RERE perturbou redes de genes envolvidas no crescimento dendrítico e em grandes sistemas de sinalização química, especialmente a via do glutamato. Um alvo-chave emergiu: o gene GRIN2A, que codifica uma subunidade crucial (GluN2A) dos receptores de glutamato do tipo NMDA, há muito implicados na esquizofrenia. Os autores mostraram que RERE forma parceria com outras duas proteínas nucleares, RARB e RXRA, para se ligar diretamente ao promotor de GRIN2A e atenuar sua atividade. Em neurônios com excesso de RERE, os níveis de GluN2A diminuíram e gravações elétricas revelaram correntes sinápticas mediadas por NMDA mais fracas, embora a frequência dos eventos sinápticos permanecesse inalterada. Em outras palavras, o "volume" de sinais excitatórios individuais foi reduzido.
Ligando variantes do DNA à função cerebral
Ao combinar genética, biologia molecular, culturas celulares e eletrofisiologia, este trabalho descreve uma cadeia causal clara: variantes de risco em 1p36.23 aumentam elementos regulatórios dentro do gene RERE, levando a maior expressão de RERE em células cerebrais. RERE elevado, por sua vez, prejudica o crescimento e a maturação dos neurônios, altera a forma e o número de suas espinhas sinápticas e enfraquece a sinalização baseada em glutamato via receptores NMDA — especialmente os que contêm GluN2A. Para o leitor não especialista, a mensagem principal é que mudanças muito pequenas no DNA podem deslocar um pouco a atividade de um único gene e, ao longo de muitas células cerebrais e muitos anos, isso pode desviar o desenvolvimento e a comunicação cerebral em direções que contribuem para a esquizofrenia.
Citação: Liu, Y., Wang, J., Yang, H. et al. Functional variants at 1p36.23 confer risk of schizophrenia through modulating RERE. Nat Commun 17, 1742 (2026). https://doi.org/10.1038/s41467-026-68449-6
Palavras-chave: genética da esquizofrenia, gene RERE, neurodesenvolvimento, sinalização do glutamato, função sináptica