Clear Sky Science · pt
Polarização de CO2 induzida por campo elétrico e bloqueio de prótons bioinspirado liberam a redução de CO2 em ácidos fortes sem cátions metálicos
Transformando um Gás Problemático em um Ingrediente Útil para Combustíveis
Dióxido de carbono (CO2) é o principal gás de efeito estufa que impulsiona as mudanças climáticas, mas também é uma matéria‑prima potencial para produzir combustíveis e produtos químicos usando eletricidade renovável. Um dos maiores obstáculos é que o CO2 é persistentemente pouco reativo, especialmente em líquidos muito ácidos onde o hidrogênio indesejado se forma em vez dos produtos desejados. Este estudo mostra como um nanomaterial de ouro de formato inteligente, revestido por uma camada bioinspirada, pode superar esses entraves e converter CO2 em monóxido de carbono (CO) de forma eficiente em condições ácidas severas, sem depender de sais metálicos dissolvidos que normalmente causam incrustação e desperdício.

Por que Trabalhar em Ácido Forte Importa
A maioria dos dispositivos que convertem eletricamente CO2 opera em meios neutros ou alcalinos. Nesses meios, porém, o CO2 tende a reagir com o líquido e formar sais de carbonato e bicarbonato, desperdiçando grande parte do gás e encurtando a vida útil dos dispositivos à medida que sólidos se acumulam. Executar a reação em ácido forte poderia evitar essas perdas e aproveitar melhor cada molécula de CO2. O problema é que em ácido, íons de hidrogênio positivamente carregados estão por toda parte e se combinam prontamente para formar gás hidrogênio, competindo com o CO2 pelos elétrons na superfície do eletrodo. Ao mesmo tempo, moléculas neutras de CO2 não se adsorvem facilmente em superfícies metálicas. Os autores propuseram projetar um catalisador e um ambiente ao redor que atraíssem e ativassem o CO2 e, ao mesmo tempo, mantivessem os prótons afastados, tudo em uma solução ácida sem cátions metálicos.
Triângulos Aguçados de Ouro que Supercarregam o CO2
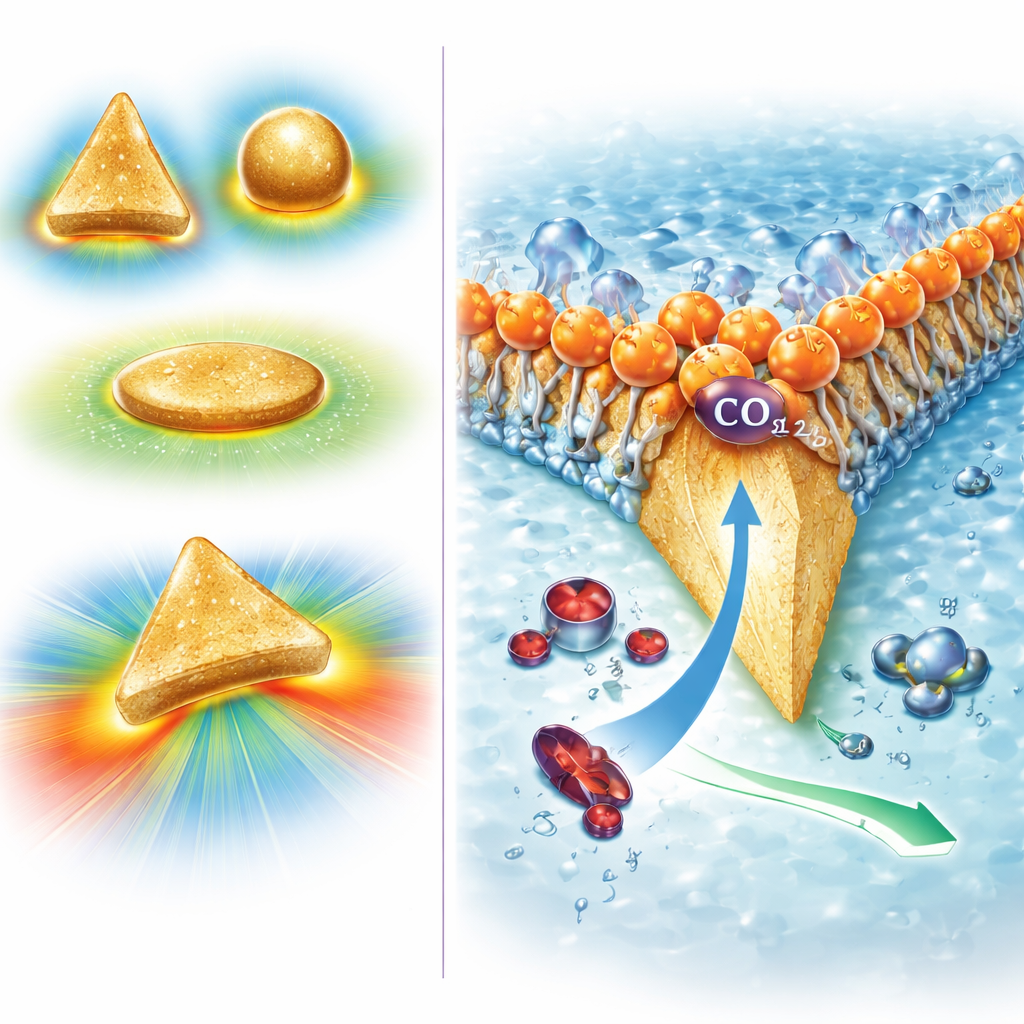
A equipe criou pequenos triângulos planos de ouro com cerca de 70 nanômetros de lado, com cantos muito afiados. Simulações por computador mostraram que, quando uma voltagem é aplicada, a carga elétrica se concentra nesses pontos agudos, produzindo campos elétricos locais extremamente fortes — cerca de dez vezes mais intensos do que em partículas mais arredondadas. Esses campos intensos distorcem a nuvem eletrônica das moléculas de CO2 próximas, transformando‑as de espécies não polares e simétricas em moléculas polarizadas com um dipolo mensurável. Essa distorção alonga e dobra levemente as ligações carbono–oxigênio, tornando as moléculas mais fáceis de ligar e transformar na superfície do ouro. Cálculos e experimentos indicam que esse efeito de campo torna a adsorção do CO2 efetivamente espontânea e reduz a barreira energética para o passo inicial crucial de sua conversão em CO, de modo que a reação ocorre mais rapidamente e com menor custo energético.
Um Revestimento Bioinspirado que Bloqueia Prótons
Para resolver o segundo problema — formação excessiva de hidrogênio — os pesquisadores se inspiraram em aquaporinas, proteínas nas membranas celulares de certos microorganismos acidófilos. Aquaporinas permitem a passagem de moléculas neutras de água enquanto bloqueiam prótons usando cargas positivas posicionadas de forma precisa. Imitando essa ideia, os autores revestiram seus nanotriângulos de ouro com uma camada de um surfactante carregado positivamente chamado CTAC. Essa camada forma uma concha macia e ordenada cujos grupos de cabeça carregados repelem os prótons que chegam, sem dificultar a passagem do CO2 neutro. Experimentos mostraram que, quando esse revestimento catiônico está presente, quase toda a corrente elétrica é direcionada para produzir CO em vez de hidrogênio, enquanto o ouro nu ou revestido de outra forma produz muito mais hidrogênio. Modelos computacionais confirmaram que a camada carregada desacelera o transporte de prótons, eleva o pH local imediatamente adjacente ao catalisador e, assim, suprime a reação secundária.
Desempenho que Persiste
Quando os triângulos afiados de ouro com CTAC foram testados em um eletrólito em fluxo a pH 1, eles produziram CO com quase 100% de seletividade em uma ampla faixa de voltagem e continuaram operando por pelo menos 100 horas em densidade de corrente elevada. A eficiência energética atingiu cerca de 60%, o que é competitivo ou superior a muitos sistemas que dependem de sais metálicos em ambientes menos ácidos. Comparações com formas de ouro mais lisas e com versões de ponta arredondada dos triângulos mostraram que tanto a forma bidimensional triangular quanto, crucialmente, os cantos afiados são necessários para alcançar esse desempenho. O trabalho demonstra uma verdadeira sinergia: campos elétricos realçados pela geometria atraem e ativam o CO2, enquanto o revestimento carregado bioinspirado molda a química local para manter os prótons afastados.
O Que Isso Significa para Dispositivos de Energia Limpa no Futuro
Para não especialistas, a principal mensagem é que esta pesquisa oferece uma nova receita para transformar CO2 em uma matéria‑prima útil sob condições que antes pareciam desfavoráveis. Ao tomar emprestado ideias da biologia e explorar a física de pontas afiadas, os autores mostram que é possível executar a conversão de CO2 em ácido forte sem íons metálicos adicionados, evitando o acúmulo de sais e melhorando o aproveitamento do CO2. Se escalados e integrados a energia renovável, esses catalisadores poderiam ajudar a transformar o CO2 de um resíduo em um bloco de construção para combustíveis e produtos químicos carbono‑neutros, ao mesmo tempo tornando dispositivos eletroquímicos mais robustos e fáceis de operar.
Citação: Chen, L., Guo, Z., Huang, HZ. et al. Electric-field-driven CO2 polarization and bioinspired proton blocking unlock CO2 reduction in strong acid without metal cations. Nat Commun 17, 1734 (2026). https://doi.org/10.1038/s41467-026-68435-y
Palavras-chave: Eletroredução de CO2, eletrólito ácido, nanocatalisador de ouro, realce de campo elétrico, bloqueio de prótons