Clear Sky Science · pt
Knockout gênico in vivo aprimorado com alta especificidade usando sgRNAs Cas12a multiplexados
Editando genes com mais confiabilidade
A edição gênica promete novas maneiras de estudar a biologia, tratar doenças e até controlar pragas de insetos, mas em animais reais muitas vezes funciona de forma menos limpa do que as manchetes sugerem. Muitas células escapam da edição ou são apenas parcialmente alteradas, o que pode borrar os resultados experimentais e limitar o uso no mundo real. Este artigo descreve um novo método baseado em CRISPR em moscas-da-fruta que torna os nocaute gênicos mais completos e mais precisos, oferecendo um roteiro para uma edição genômica mais confiável em organismos complexos.
Por que o CRISPR padrão frequentemente fica aquém
As ferramentas CRISPR tradicionais, como o Cas9, cortam o DNA em um local escolhido usando um único ou poucos RNAs-guia. Em animais vivos, essa abordagem enfrenta vários obstáculos. Alguns guias simplesmente funcionam mal; alguns locais alvo são de difícil acesso para a enzima; e a maquinaria de reparo da célula frequentemente “conserta” a quebra com pequenas alterações que deixam o gene ainda funcional. O resultado é um mosaico: células vizinhas no mesmo tecido podem carregar mutações diferentes, ou nenhuma. Essa irregularidade dificulta ver o que acontece quando um gene é realmente desligado e representa um desafio para aplicações como terapia gênica ou gene drives que precisam agir de forma eficiente na maioria das células.
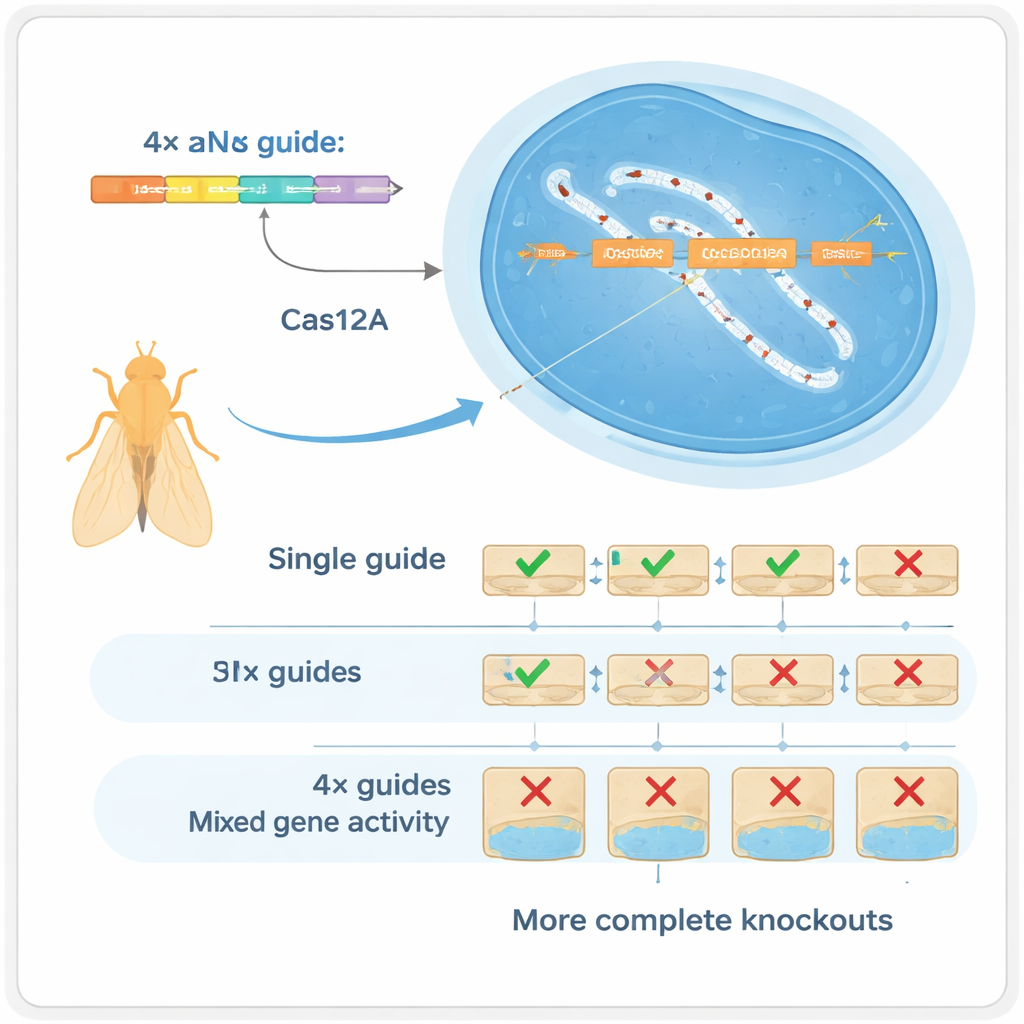
Quatro guias são melhores do que um
Os autores recorreram a outra enzima CRISPR, a Cas12a, que consegue processar arrays compactos de guias muito mais facilmente que o Cas9. Eles construíram um kit para Drosophila em que cada gene é alvo de um array de quatro RNAs-guia, todos codificados em um único pequeno fragmento de DNA que pode ser produzido em massa. Em testes cuidadosamente controlados, mostraram que usar quatro guias por gene remodela dramaticamente os tipos de alterações de DNA produzidas: em vez de principalmente pequenas inserções ou deleções em um único sítio, o sistema frequentemente gera deleções maiores entre sítios de corte que quase sempre destroem a função do gene. Esse “multiplexing” atua de duas formas: se um guia falha, outros ainda podem cumprir a função (redundância), e quando vários cortam ao mesmo tempo podem remover trechos maiores do gene (sinergia).
Alta eficiência sem dano colateral extra
Criar mais quebras de DNA levanta perguntas óbvias de segurança. Cortes múltiplos em uma região poderiam apagar acidentalmente genes vizinhos? Os guias poderiam falhar em outros locais do genoma com mais frequência? Para responder, os pesquisadores mediram morte celular, investigaram efeitos em genes vizinhos e criaram um ensaio inteligente para visualizar eventos de reparo cromossômico chamado perda de heterozigosidade ao longo de grandes trechos de DNA. Eles descobriram que agrupar quatro cortes dentro de um único gene foi bem tolerado: não aumentou a morte celular em comparação com abordagens convencionais com Cas9 e raramente perturbou genes vizinhos, a menos que um guia caísse extremamente próximo a um elemento regulatório. Triagens em larga escala usando mais de 2.000 guias cobrindo um terço do genoma da mosca mostraram que mais de 99% dos arrays de guias estavam ativos no alvo pretendido, enquanto a atividade fora do alvo reproducível ficou abaixo de 1%, indicando especificidade muito alta mesmo em um cenário multiplexado.
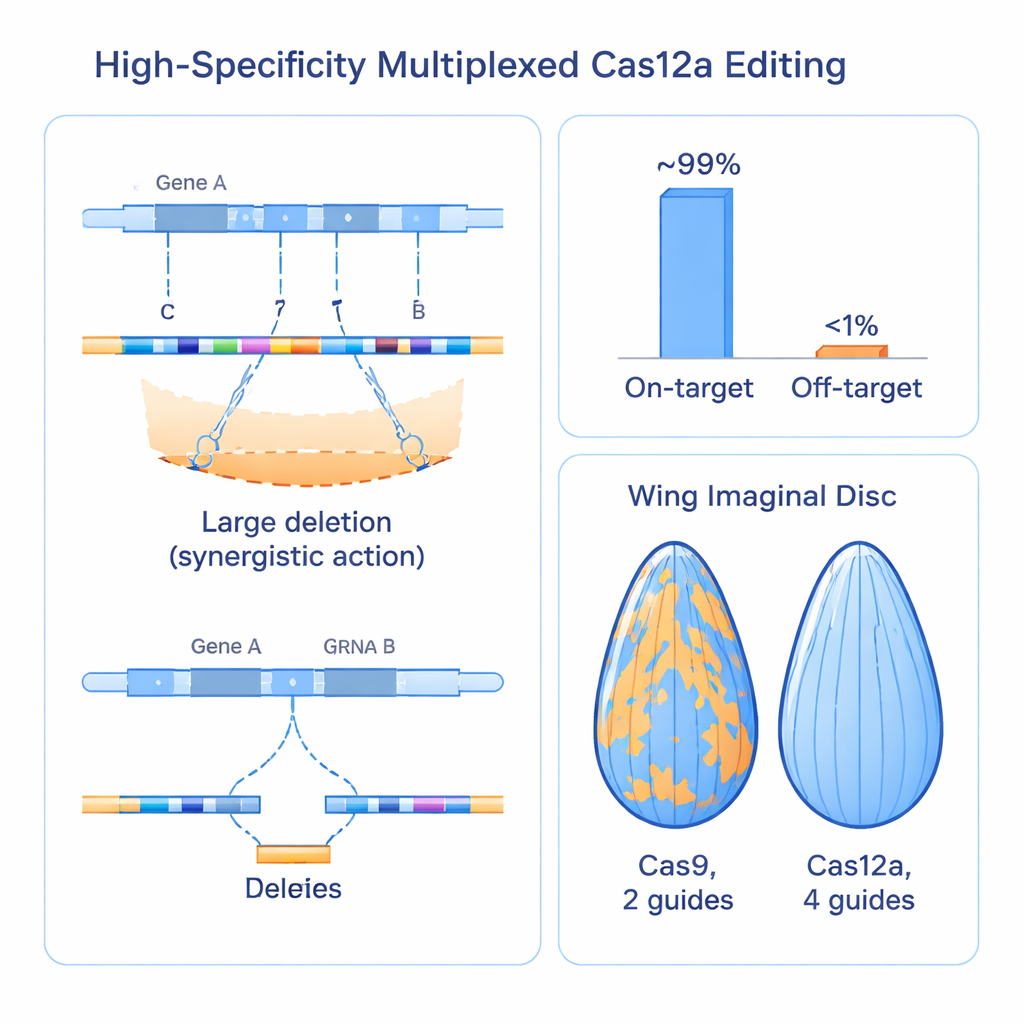
Superando sistemas Cas9 estabelecidos em tecidos reais
Para saber se essas melhorias moleculares se traduzem em biologia mais clara, a equipe comparou seu sistema Cas12a com quatro guias diretamente com recursos amplamente usados baseados em Cas9 visando mais de 100 genes na mosca. Em tecidos como olho, intestino e asa em desenvolvimento, a abordagem Cas12a produziu efeitos de perda de função mais fortes e mais uniformes do que o Cas9, que frequentemente deixou áreas óbvias de tecido não editado e normal. Quando usaram o tamanho da asa como medida quantitativa, o novo sistema gerou de forma consistente defeitos de crescimento maiores e mais reprodutíveis para reguladores conhecidos, revelando que alguns genes anteriormente classificados como fracos ou não essenciais foram, na verdade, perdidos porque as ferramentas antigas não os inativavam com profundidade suficiente. O poder aumentado do método até revelou um papel essencial previamente desconhecido para um gene chamado trade embargo no desenvolvimento e na sobrevivência da asa.
O que isso significa para o futuro da edição gênica
Em termos simples, este trabalho mostra como transformar o CRISPR de um bisturi às vezes confuso em um interruptor mais decisivo para desligar genes em animais vivos. Ao combinar Cas12a com quatro guias por gene, os autores alcançam nocaute quase completos com efeitos indesejados muito baixos, tudo em um formato prático para escalonar por centenas de genes. Embora desenvolvido em moscas-da-fruta, os princípios subjacentes — usar múltiplos guias para redundância e sinergia, e verificar cuidadosamente efeitos cromossômicos colaterais — são amplamente aplicáveis. Essa estratégia pode melhorar a pesquisa básica, afiar triagens genéticas e informar projetos mais seguros para aplicações médicas e ecológicas futuras da edição gênica.
Citação: Port, F., Buhmann, M.A., Zhou, J. et al. Improved in vivo gene knockout with high specificity using multiplexed Cas12a sgRNAs. Nat Commun 17, 877 (2026). https://doi.org/10.1038/s41467-026-68434-z
Palavras-chave: CRISPR, Cas12a, nocaute gênico, Drosophila, especificidade da edição do genoma