Clear Sky Science · pt
Controle do recrutamento da telomerase e proteção das extremidades por componentes independentes do shelterin
Como as células mantêm as extremidades dos cromossomos seguras
Cada vez que uma célula se divide, as pontas de seus cromossomos — chamadas telômeros — encurtam-se um pouco. Para evitar a perda de informação genética vital, as células usam uma enzima especial, a telomerase, e um conjunto de proteínas protetoras para preservar essas extremidades. Este estudo investiga como duas dessas proteínas, TPP1 e POT1, gerenciam o equilíbrio delicado entre permitir que a telomerase reconstrua os telômeros e manter as extremidades cromossômicas protegidas contra danos.
O problema do envelhecimento das extremidades cromossômicas
Os telômeros atuam como capas plásticas nas pontas dos cadarços, impedindo que os cromossomos se desgastem ou sejam confundidos com DNA danificado. Se a célula interpretar equivocadamente a extremidade de um cromossomo como dano, pode ativar sistemas de reparo de emergência que colam cromossomos entre si ou interrompem a divisão celular. Ao mesmo tempo, os telômeros precisam ocasionalmente se abrir para que a telomerase os alongue, especialmente em células-tronco que se dividem muitas vezes. Biólogos há muito imaginam que os telômeros alternam entre um estado “fechado”, protegido, e um estado “aberto” que permite o acesso da telomerase, mas arrisca sinais temporários de dano. Permanecia em aberto se esses dois estados refletiam diferentes conformações físicas do telômero ou mecanismos de controle verdadeiramente distintos.
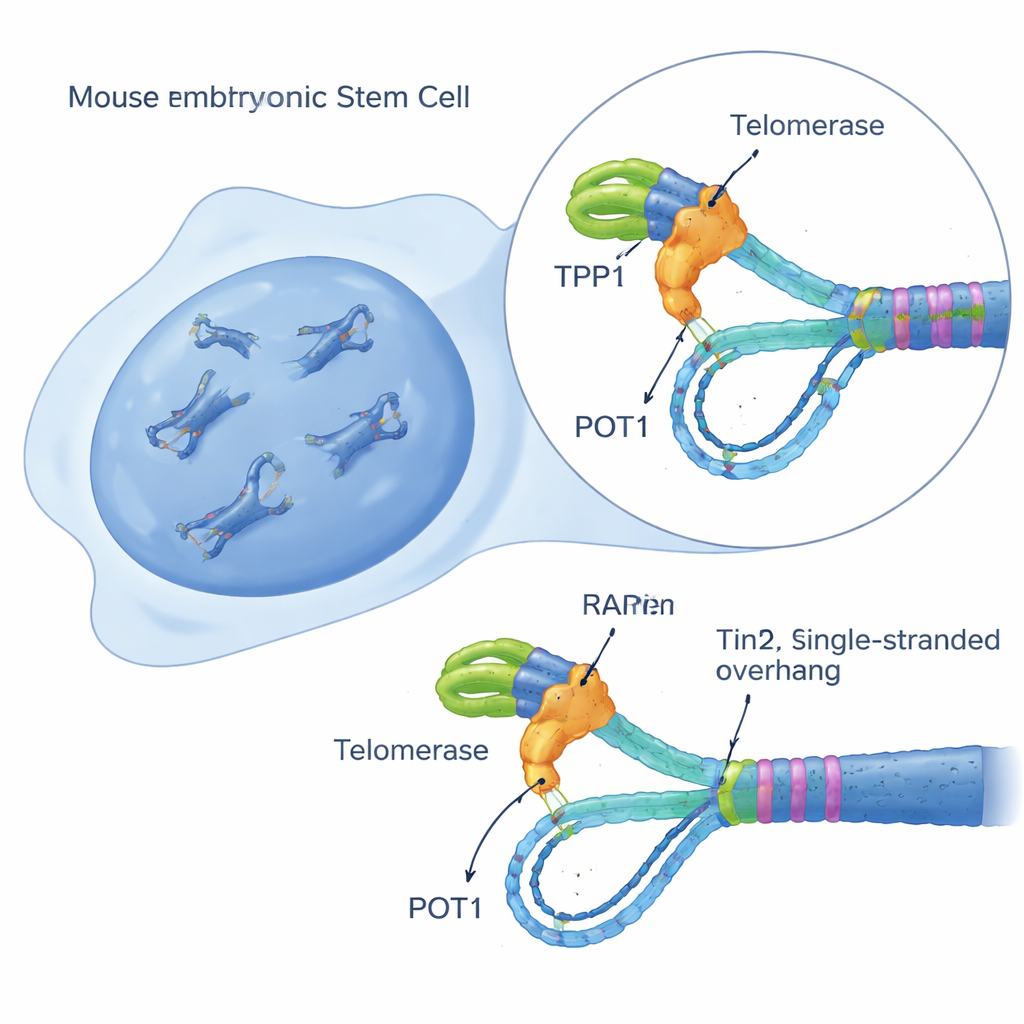
Construindo um sensor de atividade da telomerase em célula única
Para desvendar esse enigma, os pesquisadores criaram um ensaio sensível em células vivas, chamado iTAP (inducible Telomerase Activity Probing), em células-tronco embrionárias de camundongo. Eles modificaram as células para produzir uma versão levemente alterada do RNA modelo da telomerase somente quando expostas ao antibiótico doxiciclina. Esse molde “mutante” faz com que a telomerase adicione uma sequência de DNA modificada aos telômeros, distinguível visualmente do DNA telomérico normal. Usando sondas fluorescentes, blots de DNA e um método de sequenciamento que enriquece fragmentos teloméricos, a equipe pôde ver diretamente, célula a célula, quando e onde a telomerase estava ativa. Crucialmente, esse sistema não prejudicou o crescimento celular nem induziu uma resposta de dano por si só, permitindo medidas limpas do comportamento da telomerase em células essencialmente saudáveis.
TPP1 traz a telomerase; POT1 a contém
Com o iTAP, os autores testaram como duas proteínas teloméricas-chave, TPP1 e POT1, contribuem para a ação da telomerase. Ambas pertencem a um complexo maior conhecido como shelterin, que reveste os telômeros. Quando removeram TPP1 usando ferramentas de edição gênica, as sequências teloméricas mutantes praticamente desapareceram, mesmo com a produção normal do RNA mutante da telomerase. Experimentos adicionais mostraram que TPP1 precisa se ligar fisicamente a outro componente do shelterin, TIN2, para recrutar a telomerase; interromper a conexão entre TPP1 e TIN2 encerrou a atividade da telomerase. Surpreendentemente, romper a interação de TPP1 com POT1 não teve esse efeito, e a deleção de POT1 em si não reduziu a ação da telomerase. De fato, células sem POT1 exibiram um aumento modesto na quantidade de sequência mutante adicionada, sugerindo que POT1 normalmente atua como um freio — limitando com que frequência a telomerase atua nos telômeros, em vez de ajudá-la.
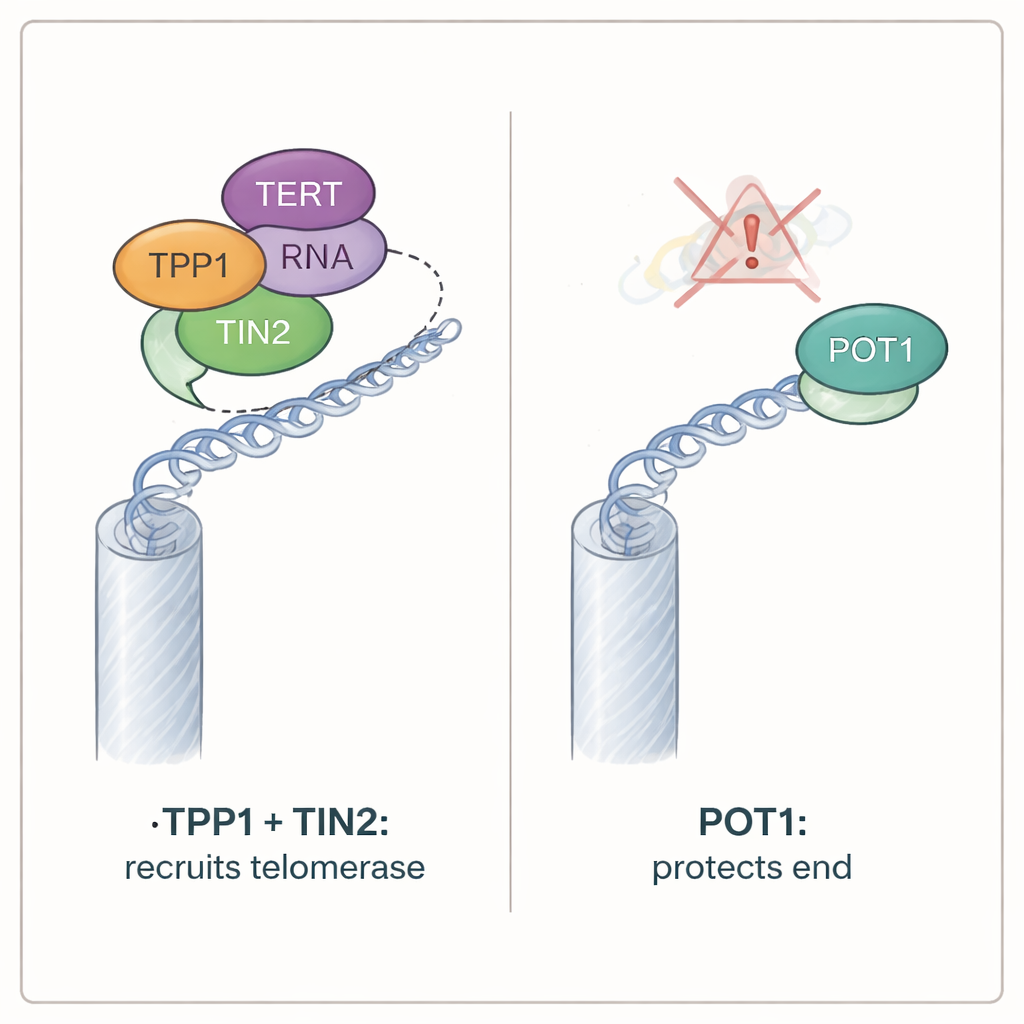
POT1 guarda as extremidades, enquanto TPP1 pode ser dispensável
Embora POT1 não fosse necessária para o recrutamento da telomerase, mostrou-se vital para proteger as extremidades cromossômicas. Células sem ambas as versões de POT1 em camundongos rapidamente pararam de proliferar e exibiram todas as marcas de telômeros expostos: marcadores de dano ao DNA se acumularam nas pontas cromossômicas, uma enzima sensor de dano chamada ATR foi ativada e as extremidades dos cromossomos se fundiram. Em contraste, células sem TPP1 continuaram a crescer e mostraram poucos sinais de estresse telomérico, mesmo tendo perdido a atividade telomerase normal. Testes adicionais mostraram que o papel defensivo de POT1 depende de sua capacidade de se ligar à porção simples fita exposta dos telômeros. Proteínas POT1 mutantes que não conseguiam mais agarrar esse DNA exposto falharam em suprimir os sinais de dano, mesmo que ainda pudessem interagir com TPP1. Por outro lado, versões de POT1 que podiam se ligar à extremidade, mas não se ancoravam ao TPP1, ainda protegiam as pontas cromossômicas.
Uma nova visão modular do controle dos telômeros
Essas descobertas derrubam a visão simplista de que os telômeros alternam entre um único estado “aberto” para a telomerase e um único estado “fechado” para proteção. Em vez disso, o estudo mostra que o recrutamento da telomerase e a proteção das extremidades são controlados por circuitos moleculares separáveis. TPP1, agindo por meio de TIN2, é a principal porta de entrada que traz a telomerase aos telômeros, enquanto POT1 protege de forma independente o DNA exposto nas extremidades cromossômicas e mantém sob controle as respostas de dano. Para o leitor leigo, a conclusão é que as células não dependem de um único interruptor universal nas pontas dos cromossomos. Ao contrário, usam botões separados, porém coordenados — um para permitir a entrada da telomerase e outro para manter as extremidades seguras — para preservar a estabilidade do genoma ao longo da vida.
Citação: Sandhu, R., Tricola, G.M., Lee, S.Y. et al. Control of telomerase recruitment and end protection by independent shelterin components. Nat Commun 17, 1733 (2026). https://doi.org/10.1038/s41467-026-68433-0
Palavras-chave: telômeros, telomerase, células-tronco, danos ao DNA, proteção dos cromossomos