Clear Sky Science · pt
Uso dinâmico de alelos de genes ligados ao X ameniza fenótipos de doenças do neurodesenvolvimento em organoides cerebrais
Como o cromossomo X “silencioso” ajuda a proteger o cérebro
Cada célula de uma mulher carrega dois cromossomos X, mas durante décadas os livros de biologia disseram que um deles fica amplamente desligado—como um livro reserva mantido fechado numa prateleira. Este estudo mostra que, especialmente no cérebro em desenvolvimento, esse X “silencioso” é mais parecido com uma biblioteca de reserva dinâmica. Ele pode ser acionado quando necessário, e essa flexibilidade extra pode ajudar a explicar por que muitos distúrbios do desenvolvimento cerebral afetam mais severamente os homens do que as mulheres.
Um sistema de reserva oculto no cromossomo X
Em mamíferas fêmeas, um cromossomo X em cada célula é desativado cedo no desenvolvimento para evitar uma dose dupla de genes ligados ao X. Ainda assim, os cientistas sabem há muito tempo que alguns genes conseguem escapar dessa desativação. O novo trabalho faz uma pergunta mais profunda: essa fuga é fixa ou pode mudar à medida que as células se desenvolvem? Usando células-tronco humanas e pequenos tecidos cerebrais chamados organoides, os pesquisadores rastrearam qual cópia de cada gene ligado ao X—materna ou paterna—era utilizada à medida que as células amadureciam de células-tronco para neurônios. Eles descobriram que muitos genes no supostamente inativo X ligam-se e desligam-se de forma específica para estágio e tipo celular, em vez de seguir uma regra simples de ligado/desligado.
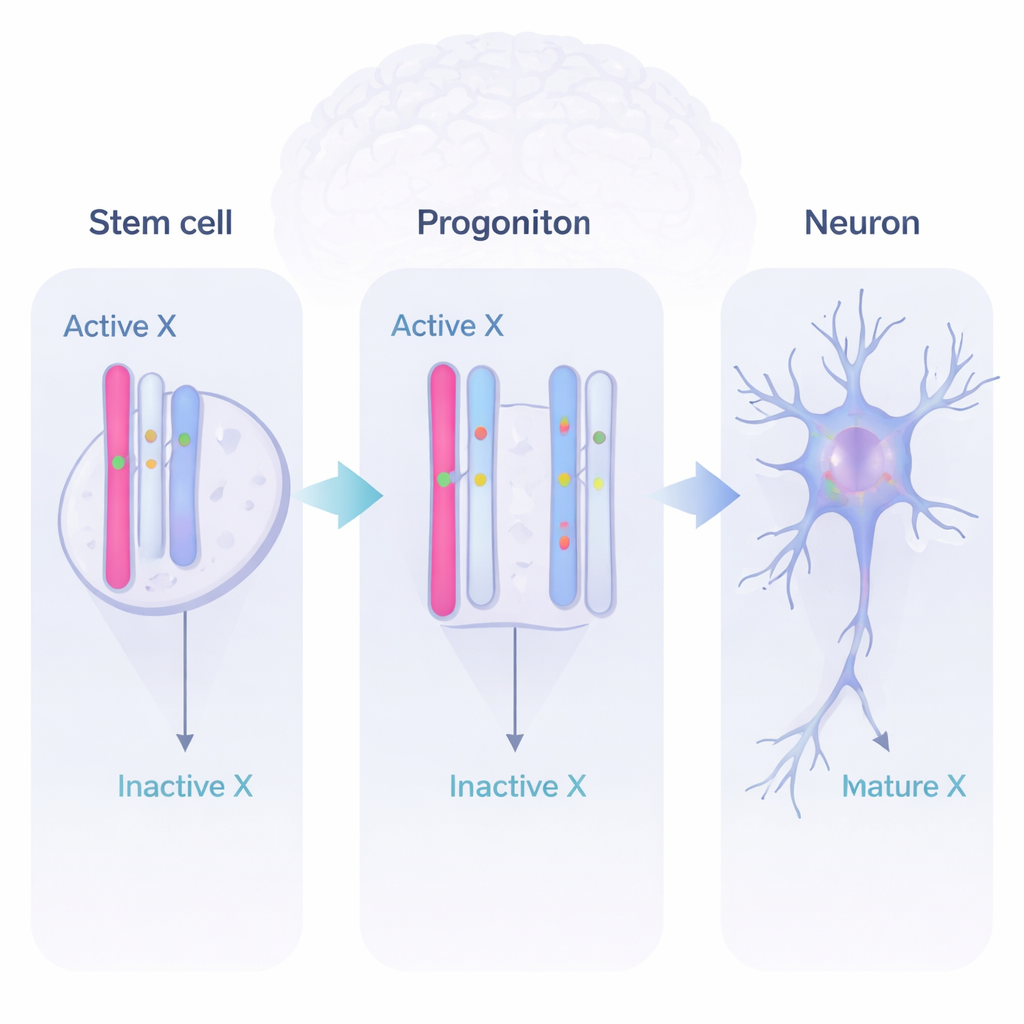
Uso dinâmico de genes durante o desenvolvimento cerebral
Lendo o RNA (as mensagens produzidas a partir dos genes) e distinguindo entre as duas cópias parentais, a equipe descobriu três comportamentos principais. Alguns genes permaneceram majoritariamente desligados no X inativo, como esperado. Outros eram “escapistas completos”, ativos a partir de ambas as cópias do X em todos os estágios. Mais intrigante, um grupo considerável de genes era dinâmico. Esses genes eram silenciosos no X inativo em células-tronco, ativavam-se a partir de ambos os cromossomos X em progenitores neurais e em neurônios iniciais, e depois alguns voltavam a se desligar mais tarde. Isso mostra que o X inativo não é um cemitério estático de genes, mas um reservatório flexível que o cérebro em desenvolvimento pode usar quando atividade gênica extra é útil.
Padrões conservados e vínculos com doenças cerebrais
Quando os pesquisadores compararam seus dados humanos com estudos em camundongos e com marcas químicas no DNA de tecido cerebral fetal, encontraram que essa fuga dinâmica da inativação do X é observada em outros mamíferos e está ligada a estados da cromatina—características do empacotamento do DNA que controlam quão facilmente os genes podem ser ativados. Os genes que se reativavam tendiam a se agrupar em certas regiões do cromossomo X e exibiam assinaturas epigenéticas de DNA ativo especificamente em tecido cerebral feminino. Importante para a medicina, esses genes reativados dinamicamente tinham uma riqueza incomum de genes de risco conhecidos para transtornos do neurodesenvolvimento, como deficiência intelectual e condições do espectro autista, sugerindo que essa flexibilidade evoluiu como um mecanismo protetor.
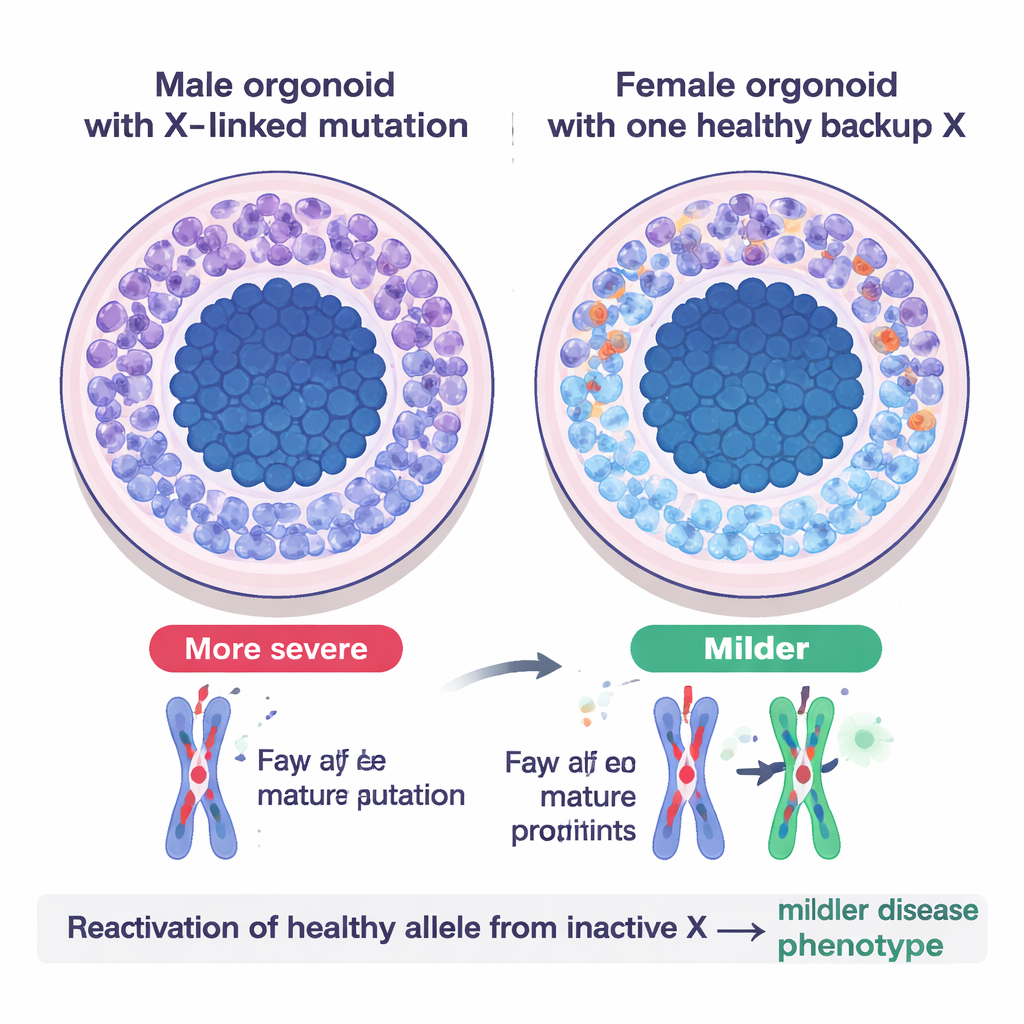
Um teste no mundo real: síndrome Opitz BBB/G
Para ver como esse sistema de reserva se manifesta na doença, a equipe modelou a síndrome Opitz BBB/G, uma condição rara ligada ao X que afeta estruturas médianas do cérebro e frequentemente causa atraso no desenvolvimento. O distúrbio é causado por mutações deletérias em um gene chamado MID1 no cromossomo X. Em organoides cerebrais cultivados a partir de células de pacientes do sexo masculino—onde existe apenas uma cópia do X—os neurônios eram escassos e as células-tronco neurais demoravam demais no estado de divisão, ecoando o subdesenvolvimento cerebral observado em pacientes. Organoides femininos com a mesma mutação no X ativo, mas uma cópia saudável no X inativo, pareciam visivelmente mais saudáveis: produziram mais neurônios e tiveram defeitos mais leves. Quando os cientistas criaram linhagens femininas de modo que ambas as cópias do X carregassem a mutação, os organoides desenvolveram problemas graves, semelhantes aos masculinos, confirmando que o alelo saudável previamente inativo havia sido reativado e estava ajudando a compensar.
O que isso significa para as diferenças sexuais nas doenças cerebrais
O estudo revela que o segundo cromossomo X “silencioso” nas fêmeas não é mero lastro genético. Durante janelas-chave do desenvolvimento cerebral, genes selecionados nesse X inativo ligam-se em tipos celulares específicos, ampliando o conjunto de cópias gênicas funcionais. Para genes como o MID1, que são cruciais para construir o cérebro, essa reativação dinâmica pode atenuar o impacto de mutações deletérias e produzir sintomas mais leves e mais variáveis nas mulheres. Em outras palavras, cérebros femininos possuem um sistema interno de reserva que pode ser ajustado ao longo do tempo, ajudando a explicar por que muitos transtornos do neurodesenvolvimento ligados ao X são menos frequentes ou menos severos em meninas do que em meninos.
Citação: Bertin, M., Todorov, H., Frank, S. et al. Dynamic allele usage of X-linked genes ameliorates neurodevelopmental disease phenotypes in brain organoids. Nat Commun 17, 599 (2026). https://doi.org/10.1038/s41467-026-68428-x
Palavras-chave: inativação do cromossomo X, organoides cerebrais, transtornos do neurodesenvolvimento, dosagem gênica, diferenças sexuais nas doenças