Clear Sky Science · pt
Shigella flexneri evita a imunidade autonômica celular mediada por septinas via ADP-riboxanação de proteínas
Como algumas bactérias intestinais escapam do nosso sistema de segurança interno
A diarreia grave causada por bactérias do gênero Shigella continua sendo um problema importante no mundo todo, especialmente em crianças pequenas. Nossas células não ficam indefesas: elas dispõem de mecanismos embutidos que podem prender e destruir micróbios invasores. Este estudo revela como Shigella flexneri, uma das principais causas de disenteria, usa artifícios moleculares para desmontar uma dessas defesas, ajudando a bactéria a se espalhar de célula a célula no intestino.
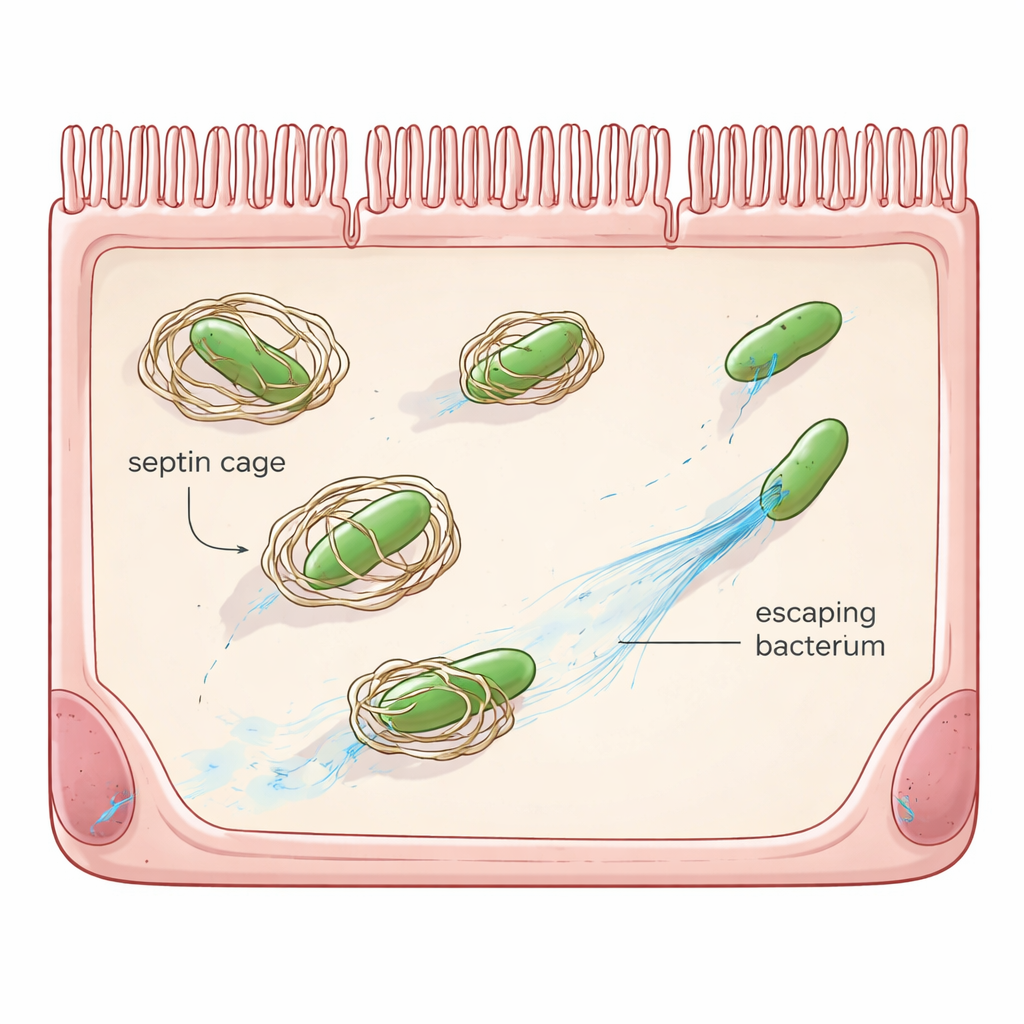
A defesa “faça você mesmo” da célula
Além dos glóbulos brancos e dos anticorpos, muitas células comuns contam com seus próprios sistemas de segurança de emergência, conhecidos como imunidade autonômica celular. Um desses sistemas depende das septinas, uma família de proteínas andaimes que formam anéis e estruturas em forma de gaiola. Quando a Shigella entra numa célula e escapa para o interior gelatinoso, as septinas podem se montar ao redor da bactéria, bloqueando sua capacidade de movimento e sinalizando sua destruição por vias de reciclagem celular. Trabalhos anteriores mostraram que a Shigella já possui uma contramedida, uma proteína chamada OspG, que marca as septinas para eliminação. Ainda assim, mesmo quando OspG está ausente, a maioria das bactérias continua a evitar ser aprisionada, sugerindo que a Shigella dispõe de truques adicionais.
Desmascarando um segundo sabotador bacteriano
Os autores voltaram sua atenção para outro grupo de proteínas da Shigella, conhecido como família OspC. Usando uma abordagem global de mapeamento de proteínas em células humanas, eles procuraram por proteínas hospedeiras que se tornavam quimicamente modificadas na presença das proteínas OspC. Além de alvos já conhecidos envolvidos na síntese proteica, encontraram várias septinas, especialmente uma chamada SEPT9, consistentemente marcadas. Testes bioquímicos detalhados mostraram que três proteínas OspC podem conectar diretamente uma pequena etiqueta rica em energia, derivada da molécula NAD, a muitos sítios nas septinas. Essa alteração química, chamada ADP-riboxanação, é uma variação especial e irreversível de uma modificação proteica mais comum.
Desmontando o andaime proteico por dentro
Para entender como essa etiqueta química enfraquece as defesas da célula, o grupo focou na SEPT9. As septinas normalmente formam cadeias ordenadas de oito subunidades, que então se alinham em filamentos e finalmente em gaiolas ao redor das bactérias. Os pesquisadores descobriram que uma posição particular na SEPT9, um aminoácido chamado arginina 561, é o principal sítio de ADP-riboxanação durante a infecção. Trabalho estrutural e experimentos de reconstituição com proteínas purificadas mostraram que esse sítio se situa numa superfície de contato crítica onde duas unidades de SEPT9 se travam. Quando essa arginina é quimicamente modificada — ou substituída por um resíduo que mimetiza a carga negativa adicionada — as cadeias octaméricas se desfazem em pedaços menores e deixam de formar filamentos estáveis.
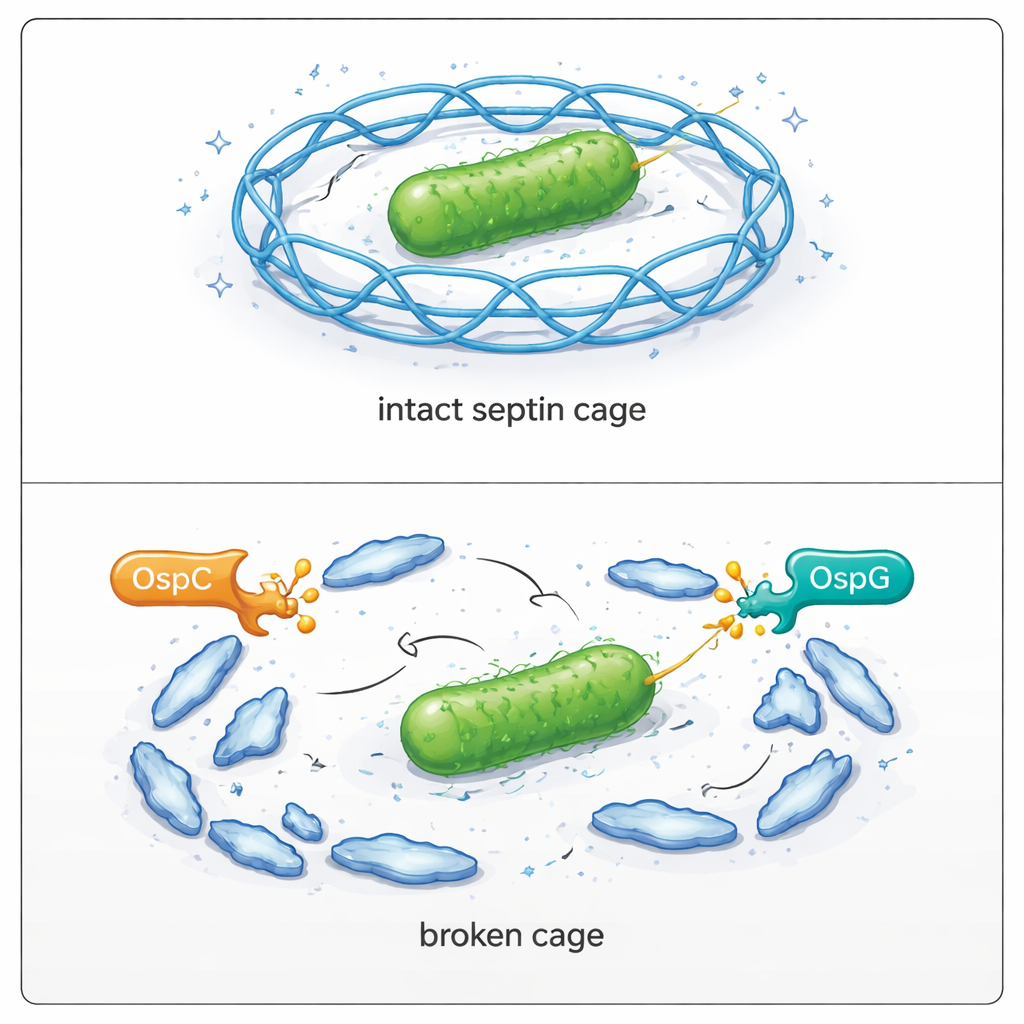
Observando as gaiolas falharem dentro de células infectadas
O grupo então voltou às células vivas para ver as consequências. Em células humanas infectadas por Shigella normal, apenas uma minoria das bactérias acabava dentro de gaiolas de septina. Quando todas as proteínas OspC foram geneticamente deletadas, a fração de bactérias aprisionadas quase dobrou. A remoção de OspG teve efeito semelhante, e a deleção conjunta de OspC e OspG aumentou ainda mais a formação de gaiolas e prejudicou severamente a capacidade das bactérias de se espalhar através de uma camada celular. A reintrodução de OspC ativos nas cepas mutantes restaurou sua capacidade de escapar das gaiolas e de replicar e formar grandes placas. A microscopia confirmou que quando a SEPT9 não pode ser modificada na arginina 561, ela participa de gaiolas de forma eficiente; quando é alterada por OspC, a formação de gaiolas ao redor das bactérias cai acentuadamente.
O que isso significa para combater a Shigella
Em termos acessíveis, este trabalho mostra que a Shigella carrega um par combinado de ferramentas moleculares projetadas para abrir as barras de uma “prisão” intracelular. OspC enfraquece diretamente os blocos de construção proteicos necessários para montar as gaiolas de septina, enquanto OspG promove sua eliminação por outra via química. Juntas, essas estratégias permitem que as bactérias escapem, se movam dentro das células e invadam as vizinhas. Entender esses mecanismos de fuga precisos não apenas aprofunda nossa compreensão de como funciona a imunidade intrínseca das células, mas também aponta para novos ângulos terapêuticos: fármacos que bloqueiem OspC ou protejam contatos cruciais das septinas poderiam ajudar a restaurar a capacidade natural da célula de prender e eliminar esse patógeno perigoso.
Citação: Tang, Z., Xian, W., Özbaykal Güler, G. et al. Shigella flexneri evades septin-mediated cell-autonomous immunity via protein ADP-riboxanation. Nat Commun 17, 1727 (2026). https://doi.org/10.1038/s41467-026-68425-0
Palavras-chave: Shigella, gaiolas de septina, imunidade autonômica celular, fatores de virulência bacteriana, ADP-riboxanação