Clear Sky Science · pt
Produtos naturais peptídicos que têm como alvo ClpC1 desregulam diferencialmente o proteoma de Mycobacterium tuberculosis
Por que atrapalhar as equipes de limpeza bacterianas importa
A tuberculose continua sendo uma das doenças infecciosas mais letais do mundo, e cepas de Mycobacterium tuberculosis resistentes a medicamentos tornam o tratamento mais difícil. A maioria dos antibióticos existentes ataca a parede celular da bactéria ou sua capacidade de gerar energia e copiar material genético. Este estudo explora um ponto fraco muito diferente: a “equipe de limpeza” interna da célula que mantém a saúde das proteínas. Ao entender como novas moléculas derivadas de produtos naturais perturbam esse sistema de limpeza, os cientistas esperam projetar futuros fármacos capazes de matar as bactérias da TB de maneiras novas e mais duradouras.
O centro de cuidados das proteínas da célula
Como todas as células vivas, a bactéria da TB constantemente constrói, dobra, repara e recicla suas proteínas. Um ator central nessa rede de manutenção proteica é uma grande máquina chamada complexo ClpC1–ClpP1P2. Uma parte (ClpC1) atua como chaperona, reconhecendo e puxando proteínas danificadas ou desnecessárias, enquanto a outra parte (ClpP1P2) as corta em pedaços para reciclagem. Esse sistema é essencial para a sobrevivência da bactéria, especialmente sob estresse, como calor ou ataque por antibióticos. Vários compostos peptídicos naturais — ecumicina, ilamicinas (rufomicinas) e ciclomarinas — já são conhecidos por se ligar ao ClpC1 e mostrar forte atividade anti-TB, o que sugere que esse complexo pode ser um alvo farmacológico poderoso. 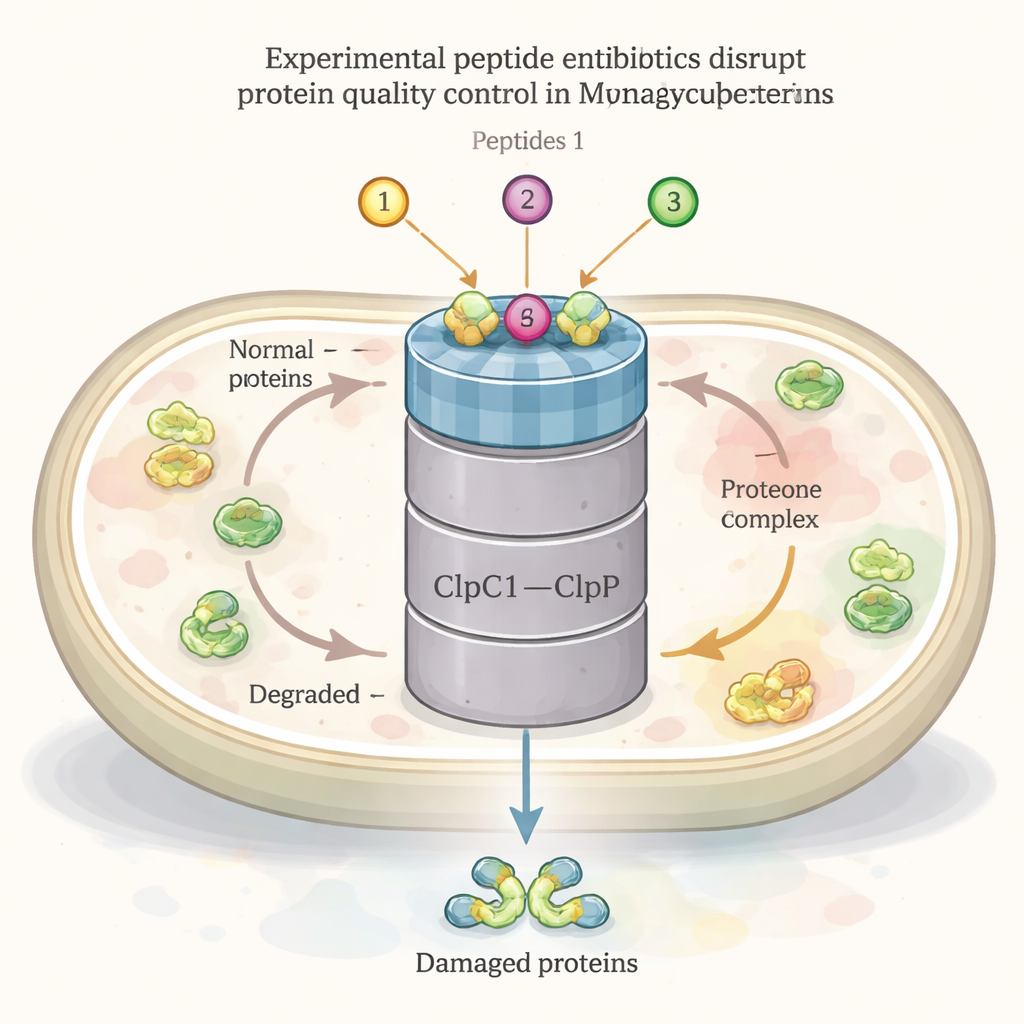
Três drogas relacionadas, três impactos diferentes
Os pesquisadores examinaram um representante de cada uma das três famílias de peptídeos: um análogo de ecumicina (Ecu*), ilamicina E (IlaE) e um derivado da ciclomarina (desoxiciclomarin, dCym). Embora os três se prendam à mesma região do ClpC1, eles não se comportam da mesma forma dentro da célula. Usando proteômica quantitativa — uma abordagem que mede milhares de proteínas de uma só vez —, eles descobriram que Ecu* causou a maior perturbação, alterando significativamente os níveis de quase 17% de todas as proteínas bacterianas. IlaE alterou cerca de 12% e dCym cerca de 7%. Apenas 72 proteínas foram consistentemente afetadas por todos os três compostos, e a maioria dessas teve redução de abundância. Isso mostra que cada molécula empurra a máquina ClpC1 em uma direção diferente, remodelando o panorama proteico da célula de maneiras distintas, em vez de simplesmente “desligar a máquina”.
Entupir o triturador versus cortar a energia
Para contextualizar esses efeitos, a equipe comparou os peptídeos com o bortezomibe, um medicamento contra o câncer que bloqueia de forma ampla enzimas degradoras de proteínas. Nas bactérias da TB, o bortezomibe causou acúmulo geral de muitas proteínas, como esperado quando os trituradores são desligados. Em contraste, os peptídeos produziram padrões mais seletivos: alguns alvos conhecidos do ClpC1 se acumularam, outros foram reduzidos, e não se observou inibição global de toda a degradação proteica. Testes detalhados em laboratório com componentes purificados mostraram que cada peptídeo alterou como substratos específicos eram tratados. Por exemplo, os três interferiram com a destruição de uma proteína regulatória (PanD), mas apenas Ecu* bloqueou a degradação de uma proteína desordenada modelo, e apenas dCym prejudicou a degradação da proteína protetora contra estresse Hsp20. Essas diferenças sugerem que a forma geral e a flexibilidade de cada proteína-alvo influenciam como ela é afetada quando o ClpC1 é “desajustado” por um composto específico. 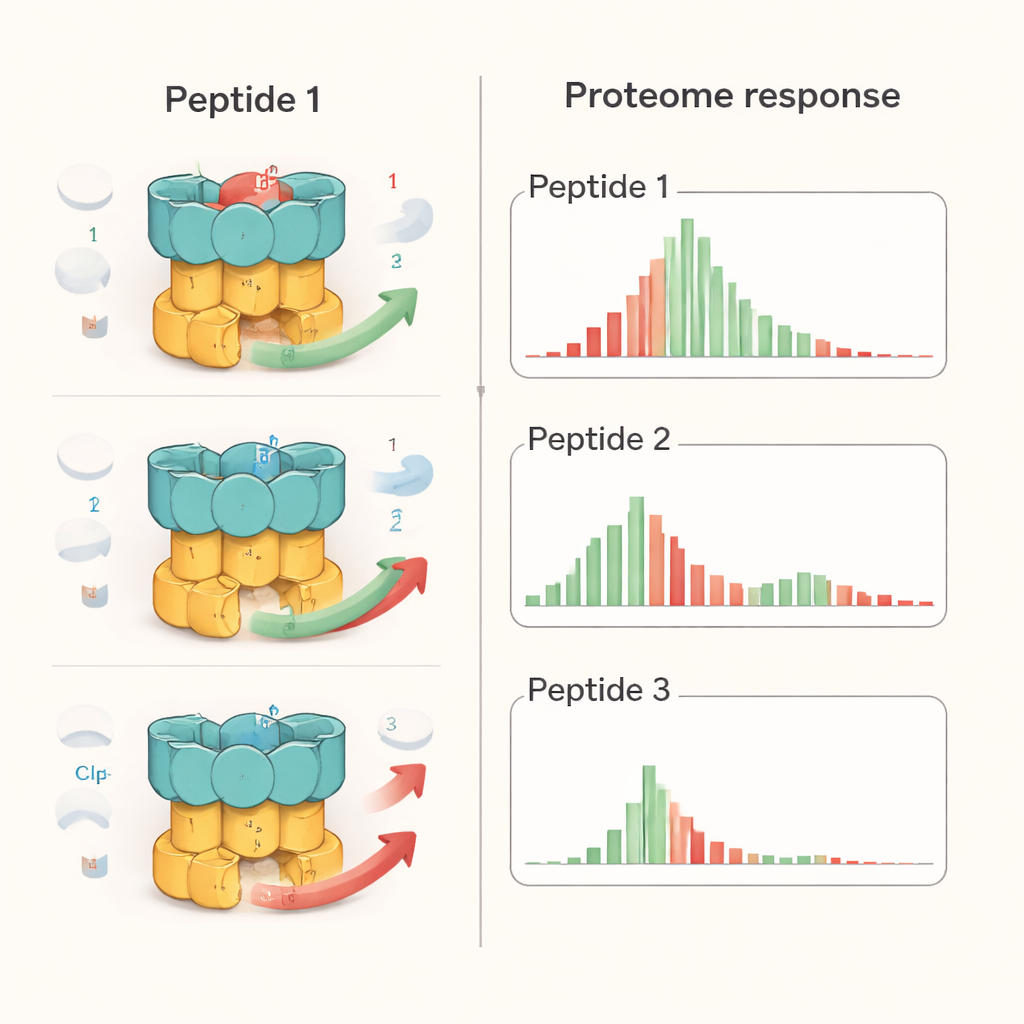
Respondedores ao estresse e o auto-resgate bacteriano
A bactéria da TB possui sistemas de reserva para lidar quando o dano proteico sobrecarrega a máquina principal de limpeza. Um desses sistemas envolve outra chaperona, ClpC2, que pode se ligar a moléculas do tipo ciclomarina e reduzir seu impacto sobre o ClpC1. Este estudo descobriu que, embora os três peptídeos possam se ligar ao ClpC2 em tubo de ensaio, apenas o derivado da ciclomarina (dCym) realmente desencadeou níveis maiores de ClpC2 em bactérias vivas e tornou-se mais potente quando o ClpC2 foi reduzido experimentalmente. Em contraste, Ecu* e IlaE permaneceram eficazes mesmo quando ClpC2 foi suprimido, sugerindo que em grande parte evitam essa rota de auto-resgate. A equipe também descobriu uma forte ligação específica por composto com Hsp20, uma pequena proteína que ajuda a prevenir agregados nocivos: Ecu* (e em menor grau IlaE) causou aumentos dramáticos nos níveis de Hsp20 e Ecu* ligou-se diretamente à Hsp20, revelando uma nova conexão entre esses candidatos a fármacos e a rede de resposta ao estresse da célula.
Transformando estresse em vantagem terapêutica
Como o sistema ClpC1 é especialmente importante sob condições adversas, os pesquisadores testaram os fármacos enquanto as bactérias eram submetidas a um estresse térmico leve, que aumenta a carga de proteínas desnaturadas. Nessas condições, tanto Ecu* quanto dCym tornaram-se muito mais letais, alcançando toxicidade semelhante à do bortezomibe, embora atuem de maneira mais seletiva. Isso demonstra que direcionar cuidadosamente a máquina de controle de qualidade proteica pode ser tão eficaz quanto desligar todas as principais proteases, mas com controle potencialmente mais preciso. O trabalho também mostrou que muitas das alterações causadas por Ecu* nos níveis de proteínas não se refletiram simplesmente em mudanças na atividade gênica, ressaltando que perturbar o ClpC1 afeta principalmente a regulação pós-tradução das proteínas.
O que isso significa para tratamentos futuros contra a TB
Para não especialistas, a mensagem-chave é que as bactérias da TB dependem de um sistema interno de limpeza e resposta ao estresse finamente equilibrado para sobreviver. Os três peptídeos derivados de produtos naturais testados aqui todos atacam a mesma máquina central, mas a empurram para modos diferentes, levando a distorções diversas e altamente específicas na composição proteica da bactéria. Importante, compostos do tipo ecumicina e ilamicina evitam um mecanismo de resgate bacteriano incorporado que pode atenuar o efeito da ciclomarina, e ainda assim debilitam o patógeno sob estresse. Essas propriedades os tornam estruturas promissoras para futuros fármacos contra a tuberculose, incluindo moléculas projetadas que poderiam forçar células de TB a destruir seletivamente suas próprias proteínas vitais ou que poderiam ser incorporadas em “chimeras direcionadoras de proteínas” para direcionar precisamente a autodestruição bacteriana.
Citação: Barter, I.K., Bedding, M.J., Leodolter, J. et al. ClpC1-targeting peptide natural products differentially dysregulate the proteome of Mycobacterium tuberculosis. Nat Commun 17, 1725 (2026). https://doi.org/10.1038/s41467-026-68423-2
Palavras-chave: tuberculose, controle de qualidade de proteínas, ClpC1, resistência a antibióticos, antibióticos de produto natural