Clear Sky Science · pt
Perfilagem epigenômica simultânea e medição da atividade regulatória usando e2MPRA
Lendo os Interruptores Ocultos da Célula
Cada célula do seu corpo carrega essencialmente o mesmo DNA, ainda que uma célula do cérebro e uma do fígado se comportem de forma muito distinta. O segredo está em trechos curtos de DNA que funcionam como dimmers para genes, aumentando, reduzindo ou desligando sua expressão. Este estudo apresenta uma ferramenta poderosa e nova, chamada e2MPRA, que permite aos cientistas testar milhares desses interruptores de uma só vez enquanto também observam como o DNA é embalado e marcado dentro da célula — passos-chave para entender desenvolvimento, risco de doenças e por que algumas variantes genéticas importam enquanto outras não.
De Mapas de DNA à Função do DNA
Ao longo da última década, os pesquisadores traçaram enormes mapas de “candidatos” a elementos regulatórios, conhecidos como elementos cis-regulatórios. Eles usam métodos que mostram onde o DNA está frouxamente empacotado (cromatina aberta), quais proteínas estão ligadas e quais marcas de histonas decoram o DNA ao redor. Esses mapas são impressionantes, mas em grande parte descritivos: o fato de uma proteína se ligar ou de uma marca aparecer não prova que uma sequência realmente controla a atividade gênica. Ensaios tradicionais de repórter em escala massiva (MPRAs) podem testar se milhares de fragmentos de DNA aumentam ou silenciam um gene repórter, mas não revelam quais proteínas se ligam ali nem quais mudanças epigenéticas acompanham essa atividade.
Um Ensaio Dois-em-Um para Atividade e Marcas Epigenéticas
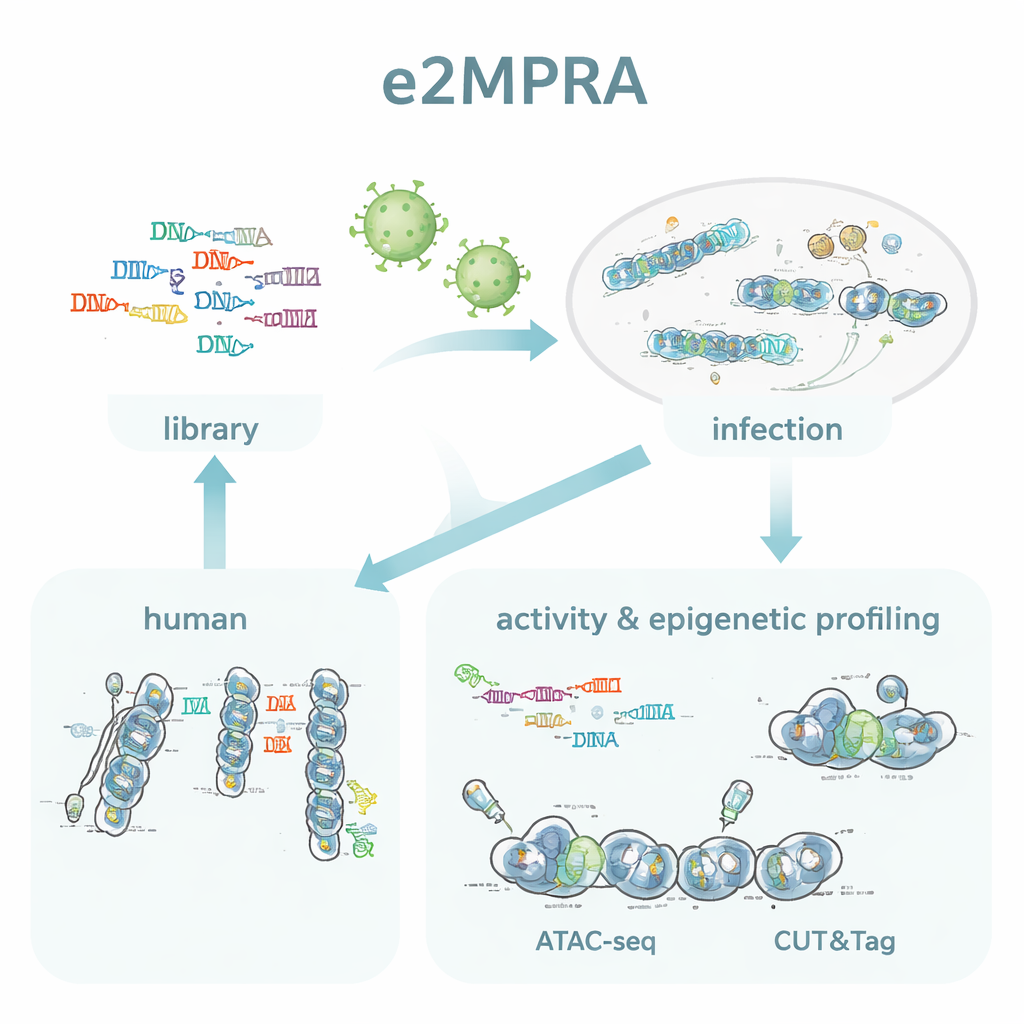
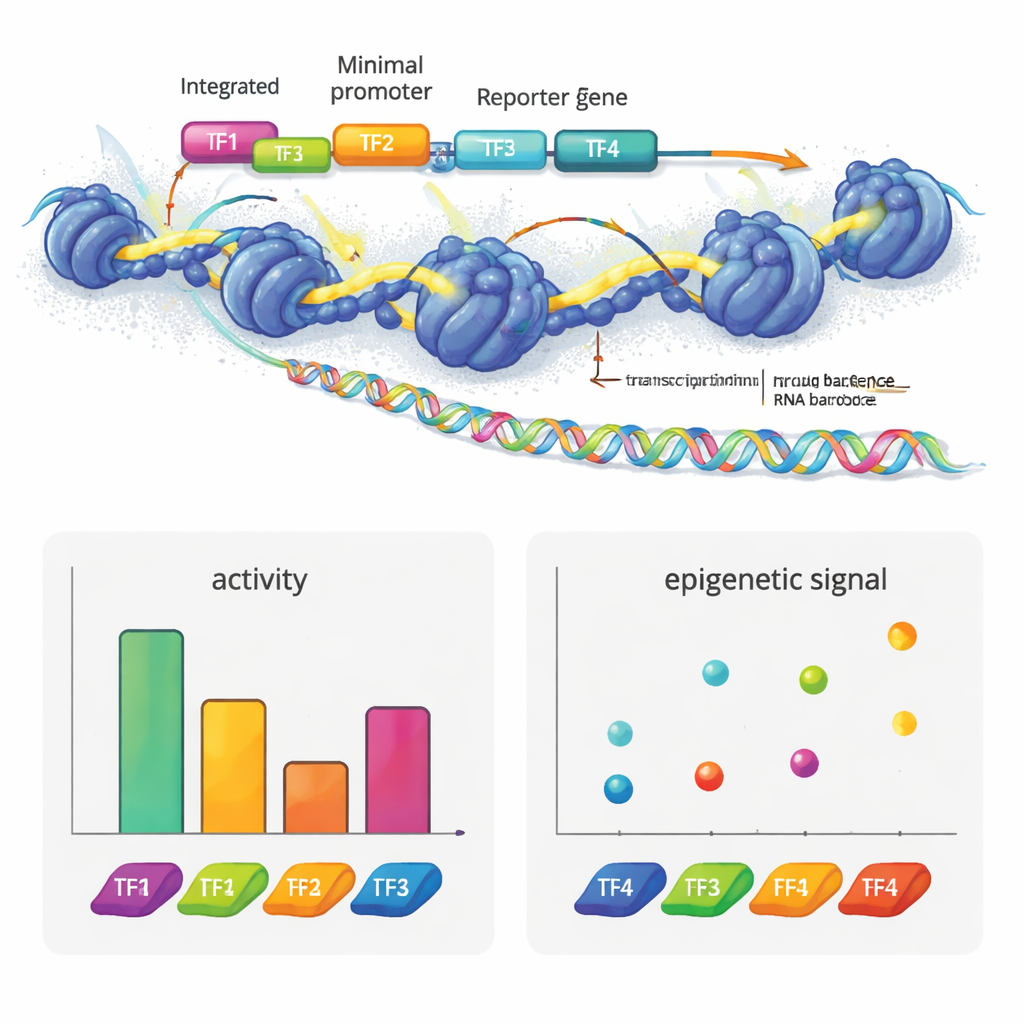
Os autores criaram o e2MPRA ao combinar um MPRA lentiviral com duas técnicas epigenômicas, ATAC-seq e CUT&Tag. Primeiro, eles constroem uma biblioteca de DNA na qual cada sequência regulatória candidata está ligada a um código de barras curto e posicionada ao lado de um promotor minimal e de um gene repórter. Essa biblioteca é então empacotada em lentivírus e integrada muitas vezes nos genomas de células humanas em cultura. Do mesmo conjunto de células, eles leem os códigos de barras no RNA para medir a atividade regulatória, e usam ATAC-seq e CUT&Tag para medir a abertura da cromatina e uma marca de histona chave (H3K27ac) especificamente nas sequências inseridas. Ao normalizar esses sinais pela frequência com que cada sequência realmente se integra, obtêm medições lado a lado da “força ligado/desligado” e do estado epigenético de milhares de elementos em um único experimento.
Decodificando Como Motivos de Fatores de Transcrição Trabalham em Conjunto
Para ver o que essa tecnologia pode revelar, a equipe construiu enhancers sintéticos a partir de motivos de fatores de transcrição conhecidos usados em células do fígado. Eles arranjaram esses motivos em diferentes números e ordens sobre moldes de DNA neutros. Alguns fatores, como HNF1A e XBP1, comportaram-se como ativadores clássicos: adicionar mais cópias aumentou a saída do repórter. Outros, como HNF1A e ONECUT1, sobretudo aumentaram a acessibilidade da cromatina, coerente com seu papel como fatores “pioneiros” que abrem DNA fechado. PPARA mostrou um padrão distinto, alterando fortemente cromatina e marcas de histona, mas não ativando a transcrição por si só, embora cooperasse com outros fatores para elevar a atividade gênica. REST, um represssor conhecido, reduziu a atividade quando colocado próximo a ativadores. De forma notável, simplesmente reordenar quatro motivos pôde mudar substancialmente a força do enhancer, e os ativadores tendiam a funcionar melhor quando mais próximos ao promotor, revelando uma espécie de estrutura gramatical na disposição desses motivos.
Localizando Bases Sensíveis em Enhancers de Pluripotência
Os pesquisadores então se voltaram a enhancers importantes para a identidade de células-tronco, focando em regiões ligadas pelos fatores de pluripotência POU5F1 (também chamado OCT4) e SOX2. Eles criaram bibliotecas densas de mutação nas quais cada base de enhancers de 100 pares de bases foi sistematicamente alterada, junto com janelas pequenas de seis bases que foram embaralhadas aleatoriamente. Usando e2MPRA em células-tronco pluripotentes induzidas, puderam ver quais mutações enfraqueciam ou fortaleciam a atividade do repórter e como afetavam abertura da cromatina e acetilação. A interrupção do motivo de ligação POU5F1::SOX2 frequentemente reduziu tanto a atividade gênica quanto as marcas epigenéticas, confirmando seu papel central. Em um enhancer bem estudado próximo ao gene POU5F1, eles também encontraram que mudar um motivo YY1 aumentou a transcrição, mas reduziu a abertura da cromatina, sugerindo que alguns fatores podem promover um estado mais aberto enquanto ainda restringem a expressão.
O Que Isso Significa para Genes e Doenças
e2MPRA não reproduz perfeitamente todas as sutilezas da arquitetura 3D natural do genoma, mas oferece uma maneira prática de comparar milhares de sequências regulatórias e variantes nas mesmas condições. Ao acoplar uma leitura funcional (o quão fortemente um segmento de DNA dirige um gene) com leituras epigenéticas (como esse DNA é embalado e marcado), esse método ajuda a revelar por que certos motivos de fatores de transcrição, combinações e posições são tão cruciais. A longo prazo, ferramentas como o e2MPRA podem facilitar a interpretação de variantes genéticas não codificantes associadas a doenças, o desenho de enhancers sintéticos para terapia gênica e a construção de um “código regulatório” mais completo que conecte sequência de DNA ao comportamento celular.
Citação: Zhang, Z., Georgakopoulos-Soares, I., Bourque, G. et al. Simultaneous epigenomic profiling and regulatory activity measurement using e2MPRA. Nat Commun 17, 1724 (2026). https://doi.org/10.1038/s41467-026-68422-3
Palavras-chave: regulação gênica, enhancers, epigenética, fatores de transcrição, genômica funcional