Clear Sky Science · pt
Ligases E3 ubiquitina guardiãs direcionam desaminases APOBEC3 associadas ao câncer para degradação para promover a integridade do genoma humano
Protegendo nosso DNA de fogo amigo
Nossas células utilizam enzimas poderosas para danificar DNA viral, ajudando a nos defender de infecções. Mas algumas dessas mesmas enzimas, se não forem controladas, podem acidentalmente marcar nosso próprio genoma e contribuir para o câncer. Este estudo revela como as células humanas fiscalizam essas enzimas arriscadas, mostrando um sistema interno de “controle de qualidade” que marca versões perigosas para destruição antes que possam reescrever nosso DNA.
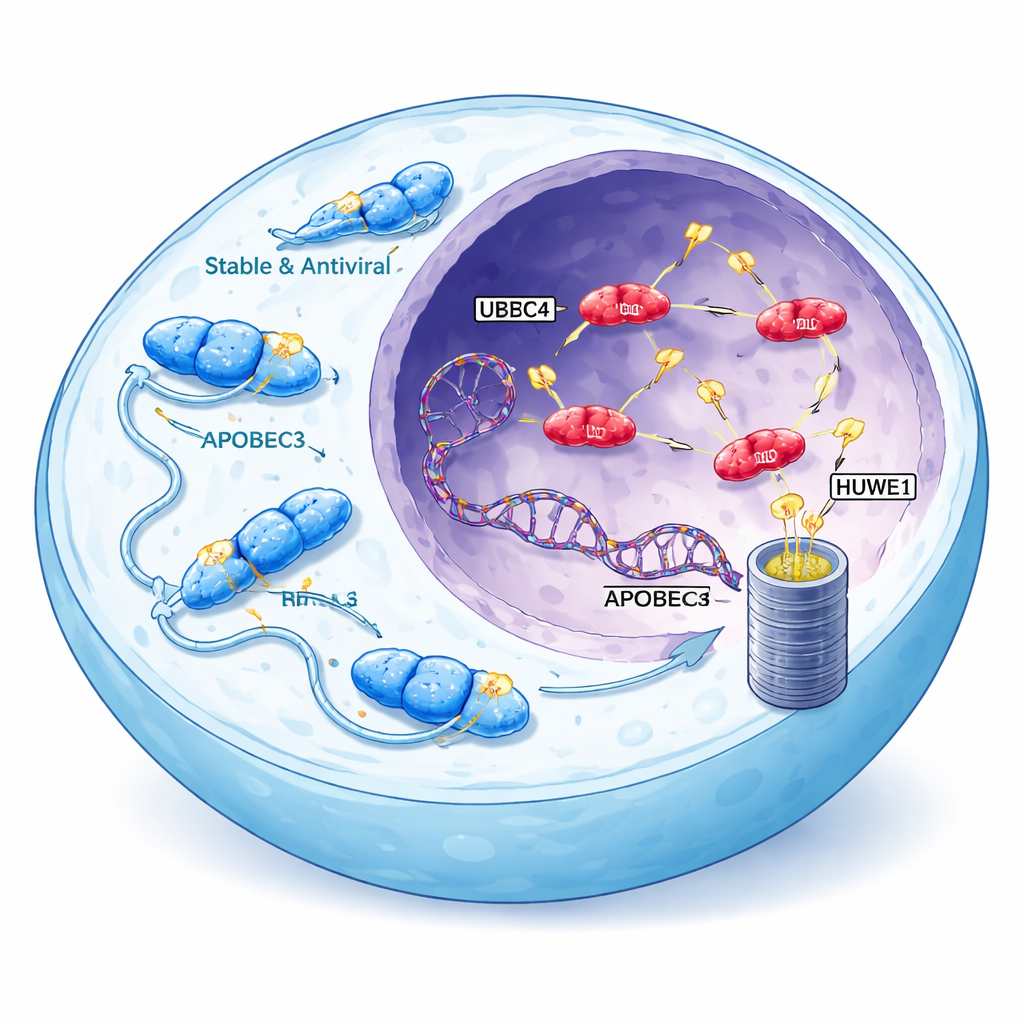
Combatentes virais que podem se voltar contra nós
A família de enzimas APOBEC3 normalmente ajuda a defender contra vírus como o HIV ao alterar quimicamente o DNA viral, provocando erros letais. Humanos carregam sete variantes de APOBEC3, e três delas — A3A, A3B e uma forma de A3H chamada haplótipo I (A3H-I) — estão fortemente ligadas a padrões de mutação observados em muitos cânceres. Essas enzimas específicas podem translocar para o núcleo celular, onde residem nossos cromossomos, e introduzir aglomerados característicos de mutações no genoma. Assinaturas ligadas a APOBEC aparecem em mais da metade de todos os cânceres humanos, especialmente em tumores de mama, pulmão e bexiga, onde ampliam o conjunto de alterações genéticas que os tumores podem usar para se adaptar e resistir ao tratamento.
Por que as formas mais perigosas são estranhamente instáveis
Curiosamente, as enzimas APOBEC3 mais fortemente associadas ao câncer também são as menos estáveis. Ao contrário de suas congêneres citoplasmáticas, que se acumulam em níveis elevados e bloqueiam vírus de forma eficiente, A3A, A3B e A3H-I são rapidamente degradadas e geralmente estão presentes em baixas concentrações no núcleo. Os pesquisadores cogitaram que essa instabilidade poderia ser deliberada: se as células limitam ativamente os níveis de proteínas APOBEC3 nucleares, qualquer falha nesse controle poderia desencadear surtos de mutagênese. Usando A3H-I como modelo, mostraram que as APOBEC3 associadas ao câncer são destruídas principalmente pelo proteassoma, o triturador de proteínas da célula, depois de serem marcadas com pequenos “sinais” moleculares chamados ubiquitina em múltiplos sítios de aminoácidos.
Encontrando os guardiões celulares
Para identificar a maquinaria responsável por marcar A3H-I e A3B, a equipe combinou triagem CRISPR com mapeamento de proximidade proteica. Eles projetaram células que brilham de modo diferente dependendo de quão estável é A3H-I e sua variante inofensiva A3H-II, e então interromperam sistematicamente genes envolvidos na degradação de proteínas. Três ligases de ubiquitina — UBR4, UBR5 e HUWE1 — se destacaram. A inativação de qualquer uma dessas ligases aumentou seletivamente os níveis da instável, nuclear A3H-I sem afetar a estável, citoplasmática A3H-II. As mesmas ligases também elevaram independentemente os níveis de A3B endógeno em linhagens de células do cólon e do sistema imune, e a deleção simultânea das três produziu um aumento aditivo na abundância de A3B. Experimentos bioquímicos mostraram ainda que UBR5 e HUWE1 se ligam fisicamente a A3B e A3H-I e anexam diretamente cadeias de ubiquitina, enquanto UBR4 parece se especializar em alongar essas cadeias para tornar as proteínas mais facilmente descartáveis.
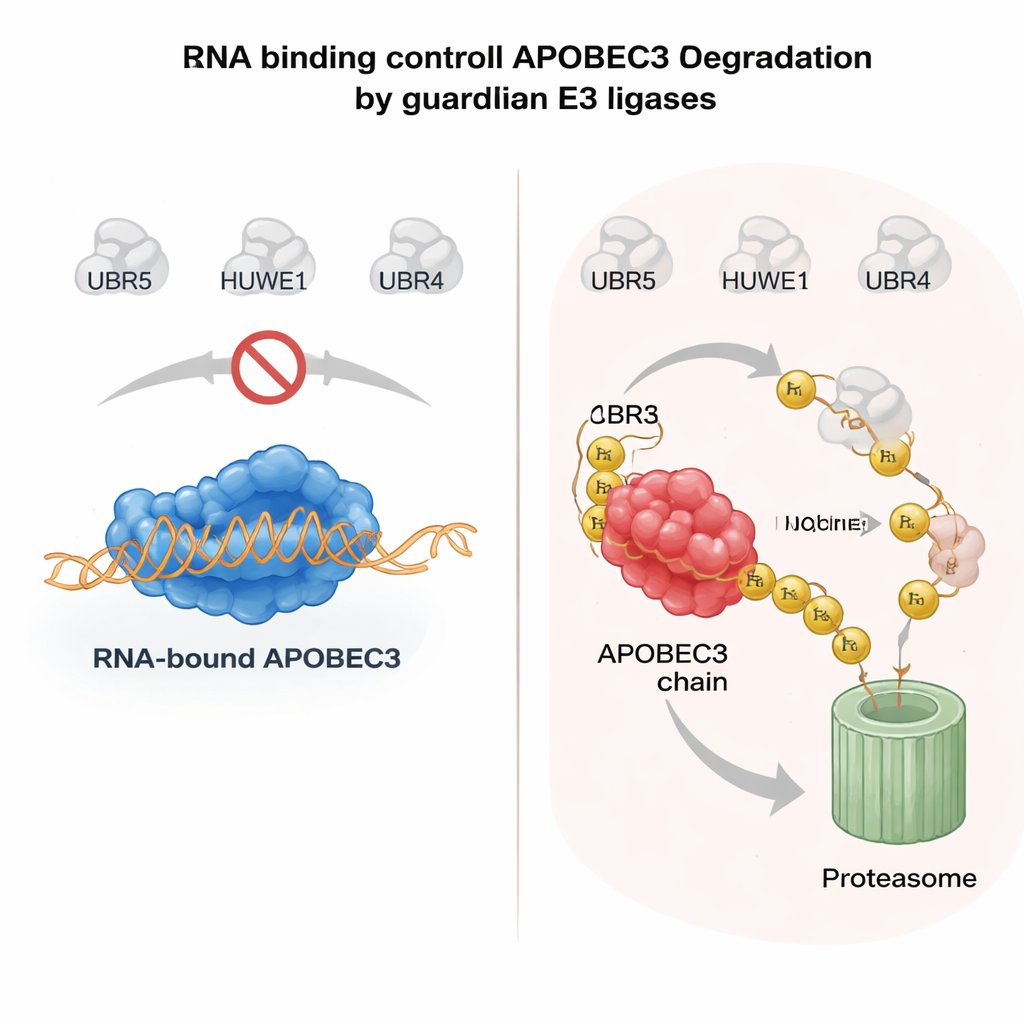
RNA como cinto de segurança para enzimas arriscadas
O que determina se uma enzima APOBEC3 é poupada ou destruída? Uma pista importante veio da forma como proteínas APOBEC3 se ligam a moléculas de RNA no citoplasma. Quando A3H ou outro membro da família, A3G, se liga ao RNA, tende a permanecer em grandes complexos no citossol e é relativamente estável. Mutações que enfraquecem a ligação ao RNA fazem com que essas enzimas migrem para o núcleo, percam seus parceiros protetores e se tornem altamente instáveis. Os autores mostraram que, quando proteínas APOBEC3 não estão ligadas ao RNA, UBR5 e HUWE1 reconhecem superfícies expostas na enzima, as decoram com ubiquitina e as direcionam para degradação nuclear. Em sistemas purificados, a adição de RNase para remover o RNA aumentou muito a capacidade dessas ligases de se ligar e ubiquitinar APOBEC3, confirmando que a ligação ao RNA atua como um escudo molecular. Esse mecanismo permite que as células mantenham APOBEC3 antivirais ativos no citoplasma enquanto eliminam rapidamente qualquer pool desencapacitado e ameaçador ao genoma no núcleo.
Quando os guardiões falham: ligações com mutações cancerígenas
Se UBR4, UBR5 e HUWE1 agem como guardiões, sua perda deveria incrementar os níveis de mutação. Os pesquisadores testaram isso desativando cada ligase em células de câncer de cólon e acompanhando alterações no DNA ao longo do tempo usando um método de sequenciamento sensível que lê “assinaturas” mutacionais. Remover essas ligases, particularmente em células que expressam A3H-I, amplificou padrões de mutação específicos de APOBEC — exatamente o tipo encontrado em tumores humanos. Ampliando para dados de pacientes, eles analisaram milhares de genomas tumorais e descobriram que tumores com mutações em UBR5 ou HUWE1 apresentavam uma fração significativamente maior de assinaturas de mutação vinculadas à APOBEC do que tumores com ligases intactas, mesmo após ajustar pela carga total de mutação. Isso sugere que ligases guardiãs defeituosas em pacientes podem permitir que APOBEC3s associadas ao câncer atuem livremente e reconfigurem o genoma tumoral.
O que isso significa para o cuidado futuro do câncer
Para um não especialista, a conclusão é que nossas células possuem um sistema sofisticado de fiscalização para evitar que enzimas antivirais úteis saboteiem inadvertidamente nosso próprio DNA. UBR4, UBR5 e HUWE1 atuam como guardiões que detectam quando as APOBEC3s não estão mais ligadas com segurança ao RNA e, especialmente no núcleo, as enviam para o triturador celular. Quando esse sistema de controle é enfraquecido — por mutações nas ligases ou por drogas que bloqueiam a degradação de proteínas — a atividade das APOBEC3s pode alimentar o caos genético que impulsiona a evolução tumoral e a resistência ao tratamento. Compreender essa rede de guardiões abre portas para novos marcadores diagnósticos, como mutações nas ligases ou níveis de proteínas APOBEC, e sugere que modular com cuidado essa via pode um dia ajudar a limitar surtos de mutação prejudiciais em tumores sem comprometer nossas defesas antivirais.
Citação: Schwartz, I., Budroni, V., Meyenberg, M. et al. Guardian ubiquitin E3 ligases target cancer-associated APOBEC3 deaminases for degradation to promote human genome integrity. Nat Commun 17, 1723 (2026). https://doi.org/10.1038/s41467-026-68420-5
Palavras-chave: APOBEC3, estabilidade do genoma, ligase ubiquitina, mutagênese no câncer, degradação de proteína