Clear Sky Science · pt
Padrões espaciais de contratilidade por um gradiente de atividade mecanógeno auto-organizado sustentam a gastrulação em Drosophila
Como os tecidos se esculpem
Embriões precoces de algum modo transformam folhas simples de células em formas tridimensionais complexas. Este estudo investiga uma pergunta fundamental por trás desse truque: como as células coordenam onde contrair e dobrar para que um tecido se dobre no local e na direção corretos? Ao observar embriões de mosca com alta resolução, os autores identificam um sinal químico que se comporta como um “morfógeno mecânico”, padronizando diretamente onde as células se tensionam para impulsionar um evento crucial de dobra durante o desenvolvimento.
Uma onda que dobra o embrião
No moscardo Drosophila, uma etapa-chave do início do desenvolvimento é a gastrulação, quando uma camada plana de células se dobra para dentro para começar a formar o intestino. Na parte posterior do embrião, um grupo de células chamado primórdio do endoderma posterior inicia esse processo contraindo seus lados superiores (ápices). Essa dobra inicial lança uma onda viajante de invaginação tecidual que avança pelas células vizinhas. Os autores mostram que essa onda depende de um sinal chamado Fog, uma molécula secretada que ativa uma família de receptores conhecidos como GPCRs, os quais, por sua vez, ligam a máquina contrátil da célula composta pela proteína motora Miosina-II.
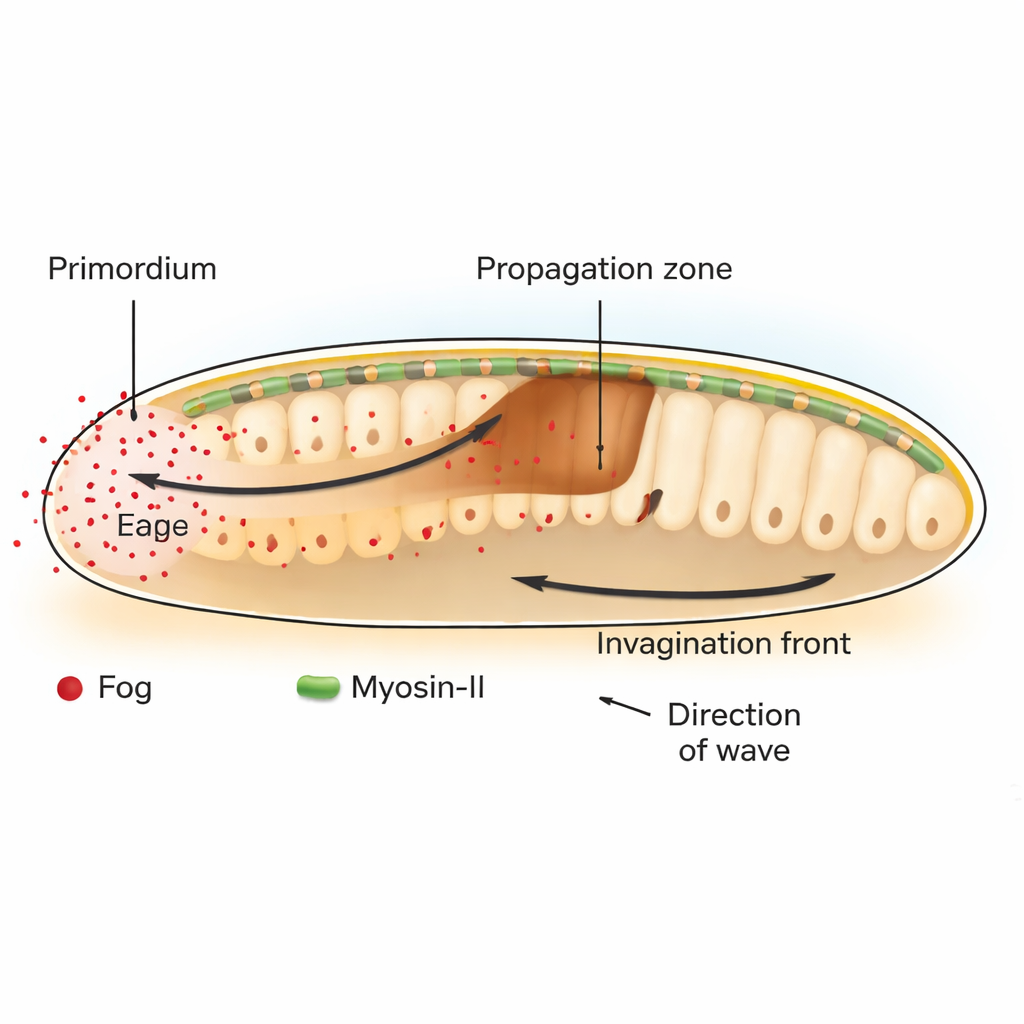
Um químico que padroniza força, não destino
Classicamente, biólogos do desenvolvimento têm se concentrado em “morfógenos”, moléculas que se difundem e cujos gradientes de concentração dizem às células que identidade adotar. Aqui, Fog se comporta de forma diferente. Em vez de alterar o tipo celular que uma região se tornará, Fog ajusta diretamente quão fortemente as células se contraem. Ao restaurar ou bloquear seletivamente Fog e seu mensageiro a jusante Gα apenas em certas regiões, os pesquisadores demonstram que Fog produzido no primórdio é tanto necessário quanto suficiente para desencadear a ativação da Miosina-II e a dobra do tecido à distância na zona de propagação adjacente. Quando Fog é retido de modo que não possa se espalhar, somente as células produtoras se contraem e a onda de invaginação estagna após uma ou duas fileiras de células.
Um gradiente oculto na superfície celular
Uma ideia natural é que Fog possa formar um gradiente de concentração clássico no meio extracelular. Usando uma versão fluorescente marcada de Fog e medições de fluorescência sensíveis, a equipe encontra o oposto: na fina camada fluida entre o tecido e sua envoltura (a membrana vitelínica), Fog é notavelmente uniforme. Ainda assim, a atividade da Miosina-II forma claramente um gradiente viajante acentuado, mais forte bem à frente da dobra em avanço e enfraquecendo a alguns diâmetros celulares de distância. A peça que faltava é que Fog não atua como um simples indicador de concentração em massa; em vez disso, uma pequena fração de Fog fica temporariamente aprisionada na superfície celular, ligando-se aos seus receptores GPCR e formando um gradiente de atividade ligado à superfície mesmo que as moléculas livres de Fog permaneçam homogeneamente distribuídas no fluido.
Receptores, endocitose e adesão moldam a onda
Os autores mostram que esse Fog ligado à superfície, junto com seus receptores, se auto-organiza em um padrão. Onde Fog encontra repetidamente receptores, ele promove o agrupamento e a ativação dos receptores, o que recruta mais Miosina-II. Um processo celular de “limpeza”—a endocitose dos GPCRs—então remove complexos ativos, prevenindo ativações descontroladas e ajudando a ajustar até onde o sinal se propaga. Quando essa endocitose é geneticamente retardada, o gradiente de Miosina-II torna-se mais alto e mais amplo. Um segundo ator chave é um conjunto de moléculas de adesão chamadas integrinas. À medida que o tecido se dobra, as células à frente da dobra pressionam contra a membrana vitelínica; esse contato ativa localmente as integrinas, que por sua vez aumentam a eficácia da sinalização Fog–GPCR. A região de forte engajamento de integrinas coincide com a extensão do gradiente de Miosina-II, e sem integrinas a onda torna-se fraca e de curto alcance mesmo que a sinalização Fog esteja, de outra forma, reforçada.
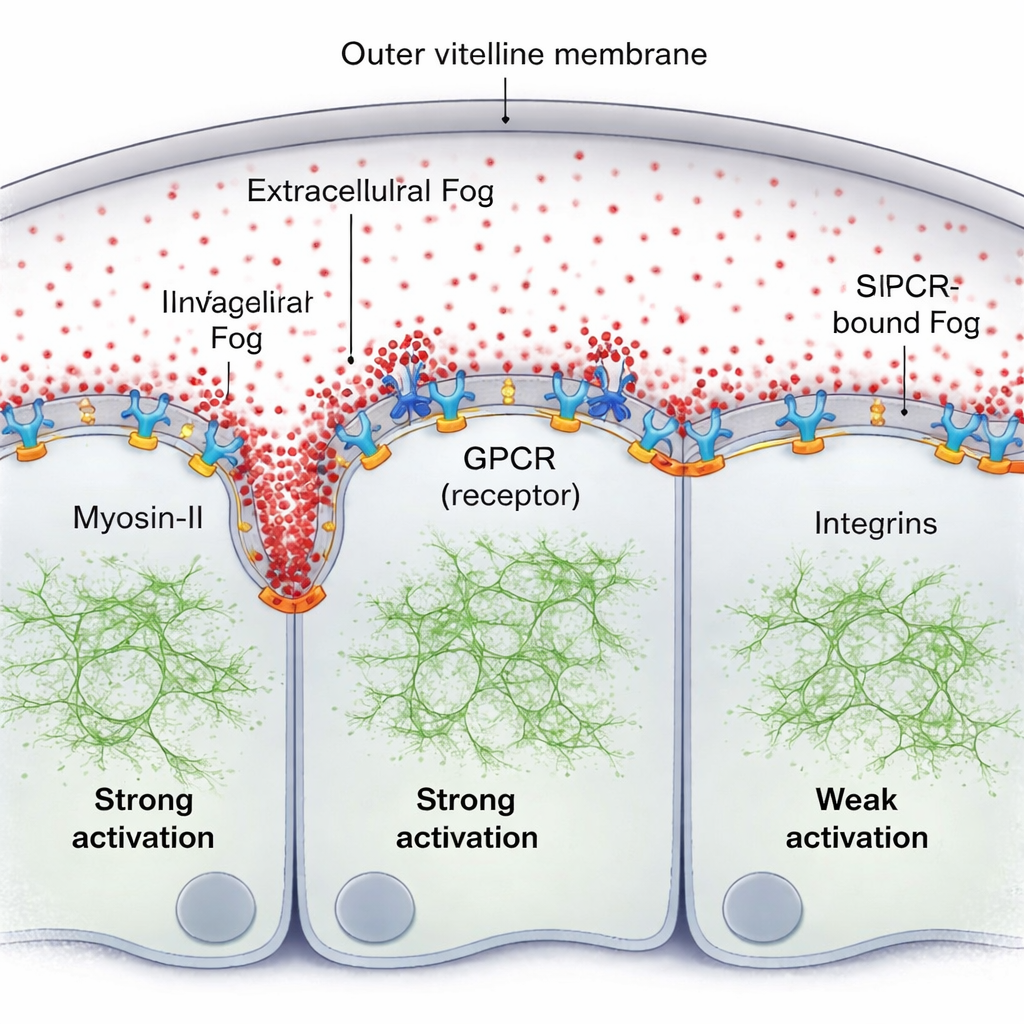
Um padrão mecânico auto-renovável
Para um leigo, a mensagem principal é que o embrião não depende apenas de mapas químicos predefinidos para decidir onde dobrar. Em vez disso, ele constrói um padrão móvel de atividade mecânica em tempo real. Fog se espalha de forma uniforme, mas sua ação efetiva é esculpida na superfície celular pelo agrupamento de receptores, remoção de receptores e pela mudança na geometria tecidual conforme as células pressionam contra o entorno. Isso cria um gradiente viajante auto-organizado de força contrátil que puxa o tecido para dentro em uma onda coordenada. O trabalho oferece um exemplo concreto do teoricamente proposto “mecanógeno”: uma molécula difusível que padroniza diretamente as forças físicas em um tecido, ajudando a explicar como os organismos vivos esculpem-se com tanta confiabilidade durante o desenvolvimento.
Citação: Mundhe, G., Dunsing-Eichenauer, V., Philippe, JM. et al. Spatial patterning of contractility by a self-organized mechanogen activity gradient underlies Drosophila gastrulation. Nat Commun 17, 1721 (2026). https://doi.org/10.1038/s41467-026-68418-z
Palavras-chave: gastrulação, mecanógeno, embrião de Drosophila, mecânica tecidual, Sinalização Fog