Clear Sky Science · pt
A configuração das extremidades do DNA determina a formação do complexo sináptico durante a ponte de extremidades mediada por NHEJ
Quando o DNA se rompe, a célula precisa agir rápido
Todos os dias, o DNA em nossas células é riscado, cortado e danificado pelo metabolismo normal e por estresses ambientais. Entre as lesões mais perigosas estão as quebras de fita dupla, nas quais ambas as fitas da hélice de DNA se rompem. Se essas quebras não forem reparadas rápida e precisamente, as células podem morrer ou, pior, evoluir para o câncer. Este estudo investiga como a forma e a química exatas das extremidades quebradas do DNA ajudam a determinar se uma via de reparo chave, chamada junção de extremidades não homólogas (NHEJ), aproxima essas extremidades de forma eficiente e com o mínimo possível de erros.
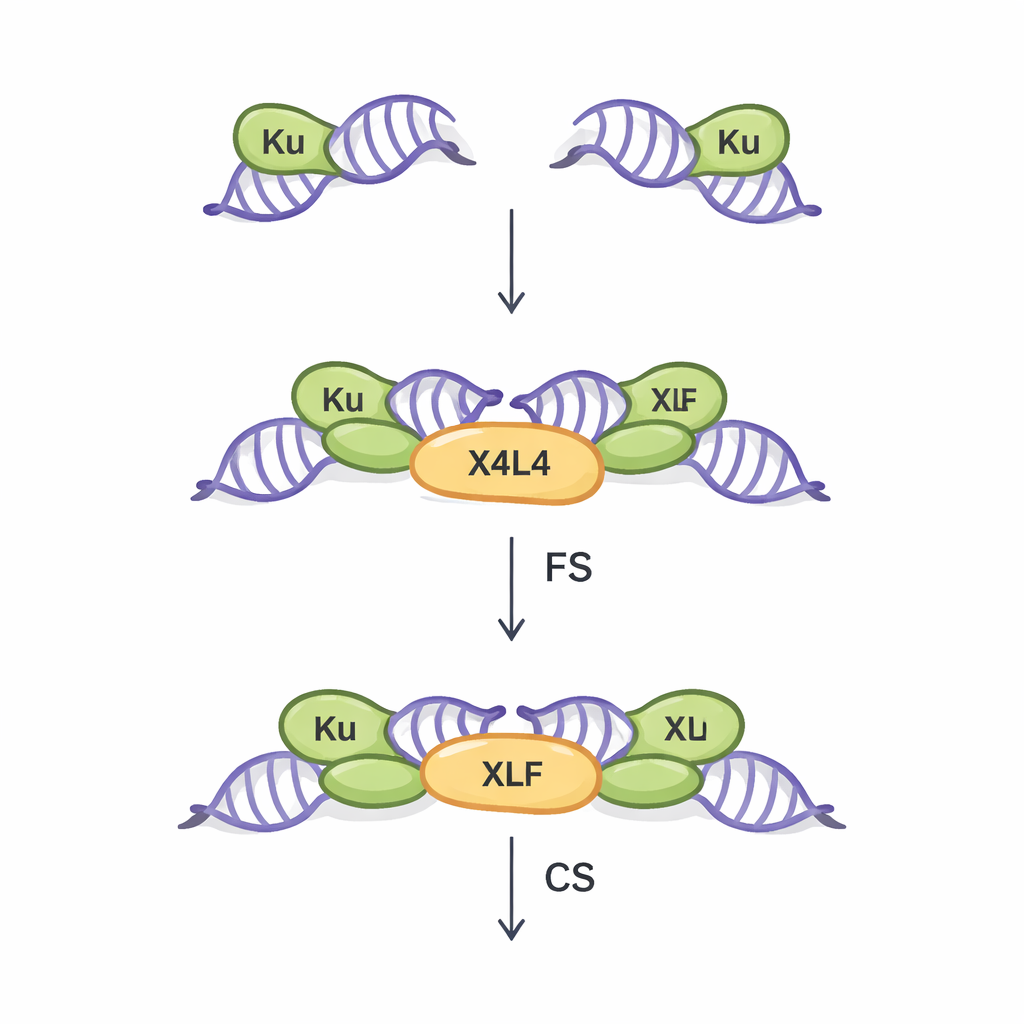
Duas maneiras de aproximar as extremidades do DNA
A NHEJ é a principal via de reparo para quebras de fita dupla na maior parte das células do nosso corpo. Ela funciona sem precisar de um molde correspondente de DNA, o que a torna rápida, porém algo suscetível a erros. O primeiro passo crucial nessa via é chamado sinapse: a ponte física entre as duas extremidades quebradas do DNA para que possam depois ser unidas. Trabalhos anteriores, em sua maioria usando extremidades de DNA perfeitamente alinhadas (bluntas), revelaram dois tipos de montagens sinápticas. No estado “sináptico flexível” (SF), as extremidades são mantidas próximas e podem se mover, procurando maneiras de emparelhar. No estado “sináptico fechado” (SC), as extremidades se alinham ponta a ponta e ficam prontas para serem seladas por uma ligase. Três proteínas centrais — Ku, XRCC4–Ligase IV (conjuntamente chamadas X4L4) e XLF — já eram conhecidas por coordenar esse processo, mas como extremidades de DNA mais irregulares influenciam qual estado sináptico se forma permaneceu pouco compreendido.
Forma das extremidades e curtos emparelhamentos direcionam a rota de reparo
Os pesquisadores usaram FRET de molécula única, uma técnica baseada em fluorescência que monitora distâncias na escala nanométrica, para observar moléculas de DNA individuais sendo aproximadas por proteínas da NHEJ. Compararam extremidades simples e bluntas com extremidades mais realistas que carregavam pequenos saliências — minúsculas caudas de fita simples que podem potencialmente emparelhar entre si. Constatou-se que, quando as saliências são complementares, mesmo por apenas algumas bases, a probabilidade de formar um complexo sináptico fechado aumenta dramaticamente. De fato, três bases correspondentes de “microhomologia” na quebra foram suficientes para que Ku e X4L4 sozinhos criassem um complexo SC estável, sem precisar de XLF. Isso mostra que o próprio DNA pode fornecer parte da energia e da orientação normalmente oferecidas por proteínas auxiliares.
Como pequenas abas de DNA ajudam a estabilizar a ponte
Ao analisar assinaturas FRET distintas, a equipe descobriu pelo menos duas configurações estruturais do estado sináptico fechado para extremidades com saliência. Em uma, as próprias pontas das saliências emparelham entre si, formando uma junção com um nick ou um gap. Na outra, as junções onde o DNA de fita dupla encontra as saliências de fita simples pressionam-se em linha, enquanto as saliências se viram para fora como pequenas abas. Essas abas ainda permitem o pareamento de bases e mantêm as extremidades muito próximas, o que provavelmente estabiliza o complexo e dá às enzimas espaço para aparar ou estender o DNA conforme necessário antes da selagem final. Curiosamente, danos oxidativos comuns nas saliências, como a 8-oxoguanina, afetaram esse processo apenas modestamente, ressaltando quão robusta a NHEJ é frente a certas formas de dano.
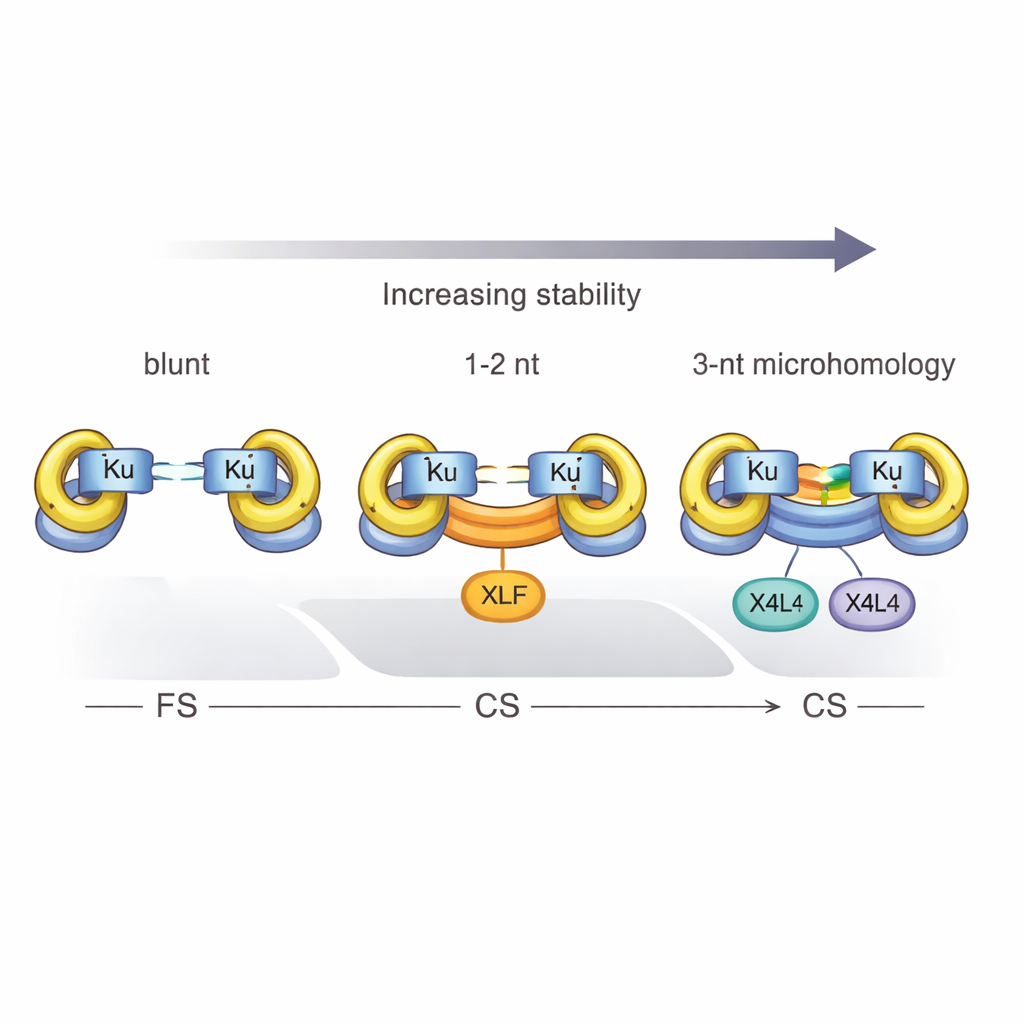
Proteínas, fosfatos e o poder do três
O estudo também definiu um limiar rígido: são necessárias pelo menos três bases emparelhadas complementares para que Ku e X4L4 convertam de forma confiável um complexo flexível em um fechado. Com apenas uma ou duas correspondências, o sistema geralmente fica preso no estado flexível, a menos que XLF entre em cena para ajudar a prender as extremidades. Detalhes químicos também importam. Quando o DNA quebrado carrega um grupo fosfato na posição 5′ — uma característica normal de muitas quebras fisiológicas — a sinapse torna-se mais eficiente, e complexos fechados têm maior probabilidade de serem efetivamente ligados, transformando uma ponte temporária em um reparo permanente. No entanto, esse impulso dado pelo fosfato não pode substituir totalmente o efeito estabilizador do pareamento de bases na quebra.
Por que isso importa para a saúde e a edição do genoma
Em linguagem mais direta, este trabalho mostra que as extremidades quebradas do DNA não são vítimas passivas esperando para serem consertadas. Suas formas exatas, pequenos trechos de sequência combinante e marcas químicas guiam ativamente como as proteínas de reparo agarram, alinham e reconectam essas extremidades. Quando três ou mais bases correspondentes estão presentes, as próprias extremidades do DNA ajudam a travar a quebra em uma configuração pronta para reparo, tornando às vezes certas proteínas auxiliares opcionais. Quando tais correspondências são escassas, fatores proteicos adicionais tornam-se essenciais. Esses achados ajudam a explicar por que algumas quebras são consertadas com precisão, enquanto outras levam a pequenas mutações ou rearranjos. Eles também oferecem pistas para aprimorar ferramentas de edição do genoma, como o CRISPR, onde quebras deliberadamente criadas no DNA são reparadas pela mesma maquinaria da NHEJ. Ao ajustar as extremidades dessas quebras, cientistas podem controlar melhor como o genoma é remodelado.
Citação: Zhang, C., Jin, W., Jiang, Y. et al. DNA end configurations dictate synaptic complex formation during NHEJ-mediated end bridging. Nat Commun 17, 1720 (2026). https://doi.org/10.1038/s41467-026-68417-0
Palavras-chave: reparo de quebras de fita dupla do DNA, junção de extremidades não homólogas, sinapse de DNA, microhomologia, estabilidade do genoma