Clear Sky Science · pt
Uma única troca de valina por leucina interrompe a ligação ao DNA do AP2-G de Plasmodium falciparum e revela o papel do GDV1 na ativação de ap2-g
Como os parasitas da malária fazem uma escolha crítica de vida ou morte
Parasitas da malária que vivem em nosso sangue enfrentam constantemente uma decisão que muda suas vidas: continuar se multiplicando dentro de um hospedeiro ou transformar-se numa forma capaz de saltar para o próximo hospedeiro por meio da picada de um mosquito. Este estudo revela como uma única alteração minúscula em uma proteína do parasita pode encerrar completamente essa fase infecciosa, pronta para o mosquito, oferecendo novas possibilidades para bloquear a transmissão da malária.
A encruzilhada do parasita
No sangue, os parasitas Plasmodium falciparum concentram-se majoritariamente no crescimento rápido, que causa a doença. Mas uma pequena minoria se transforma em formas sexuais chamadas gametócitos, os únicos estágios que os mosquitos podem captar e transmitir. Por que apenas alguns parasitas em uma população fazem essa mudança tem sido um mistério de longa data. Trabalhos anteriores mostraram que duas proteínas do parasita, GDV1 e uma proteína de ligação ao DNA chamada AP2-G, estão no centro dessa decisão. O GDV1 ajuda a despertar o gene ap2-g, normalmente silencioso, e o AP2-G por sua vez liga um conjunto de genes que impulsionam o desenvolvimento sexual. O estudo atual partiu para investigar outra proteína, uma quinase chamada STK2, mas acabou esbarrando numa descoberta muito mais dramática no próprio AP2-G.
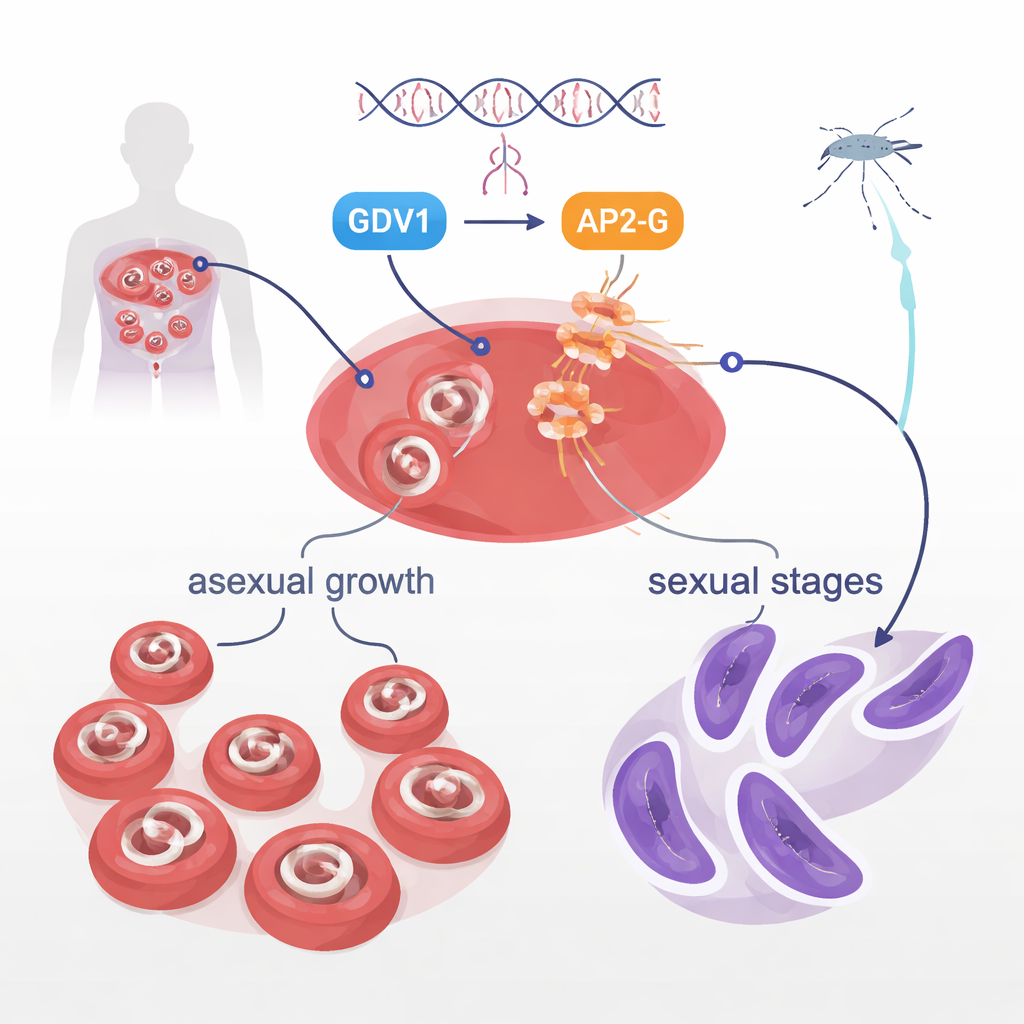
Um único aminoácido que impede a transmissão
Ao deletar o gene stk2 em uma linhagem de laboratório, os pesquisadores notaram que esses parasitas perderam completamente a capacidade de produzir gametócitos, embora ainda crescessem assexuadamente sem problema. Surpreendentemente, quando repetiram manipulações semelhantes em outra linhagem, os gametócitos se formaram normalmente. O sequenciamento do genoma inteiro revelou o culpado oculto: uma única mudança de “letra” no gene ap2-g, trocando um aminoácido, valina, por outro muito semelhante, leucina, na posição 2163. Essa posição fica no início da região de ligação ao DNA do AP2-G, a parte que agarra fisicamente motivos de DNA específicos para ativar genes. Essa troca minúscula de valina por leucina foi suficiente para abolir a formação de gametócitos. Quando os cientistas introduziram essa mutação em parasitas por outro modo normais, os gametócitos desapareceram; quando a reverteram de volta para valina, o desenvolvimento sexual foi completamente restaurado.
Como a troca quebra a fechadura molecular
Para entender por que essa alteração sutil é tão devastadora, a equipe combinou modelagem computacional com experimentos de laboratório. As previsões de estrutura sugeriram que substituir valina por leucina desloca e desestabiliza a forma precisa do domínio de ligação ao DNA AP2. Em ensaios de bancada usando proteínas purificadas, o AP2-G normal ligou-se fortemente à sua sequência de DNA preferida, um código curto contendo o motivo “GnGTAC”. Em contraste, o AP2-G mutante com leucina na posição 2163 não conseguiu ligar-se a essa sequência. Sem ligação estável ao DNA, o AP2-G não podia mais ativar seu próprio gene (um circuito de retroalimentação positiva conhecido como autorregulação) nem ativar dezenas de genes a jusante necessários para empurrar os parasitas para a via sexual. Funcionalmente, os parasitas mutantes tornaram-se “estéreis”: não conseguiam formar as fases que infectam mosquitos, mesmo prosperando dentro de glóbulos vermelhos.
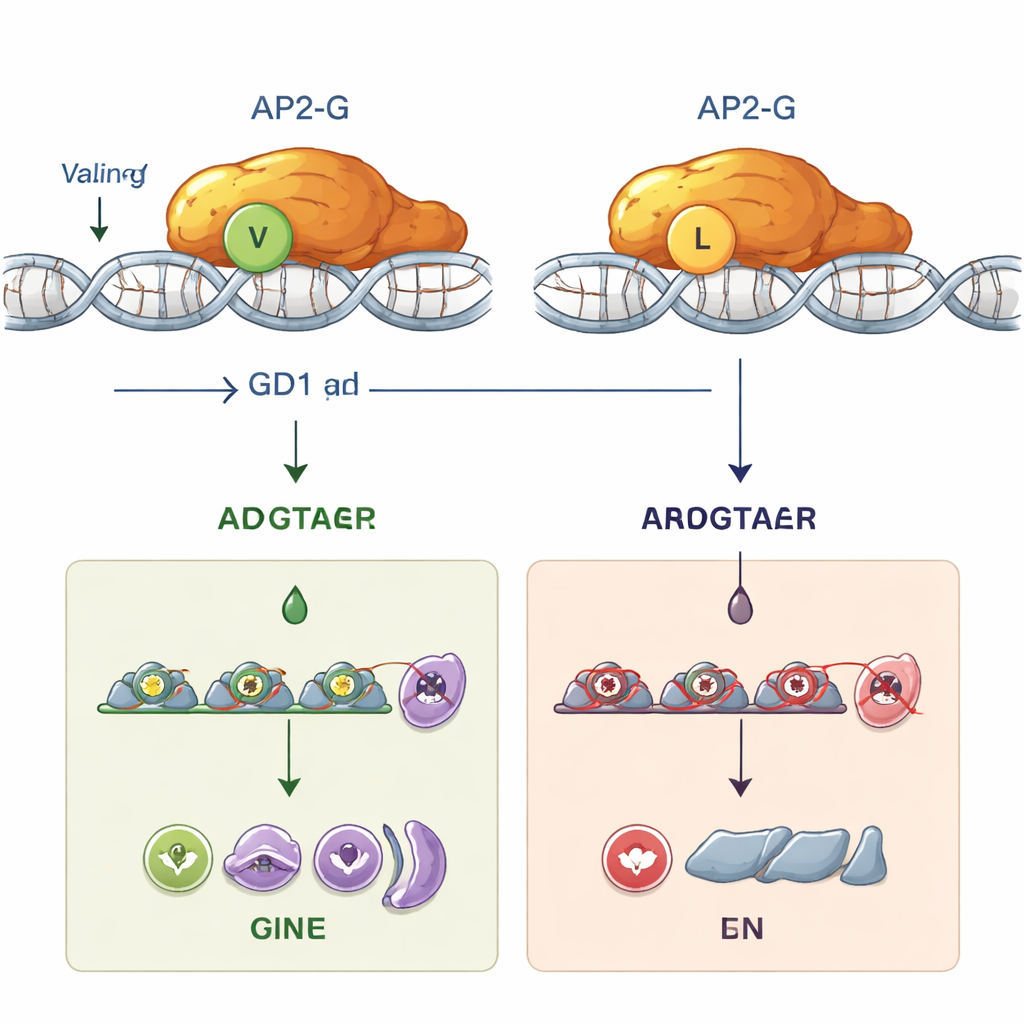
O papel oculto do GDV1 antes do AP2-G assumir
A mutação também deu aos pesquisadores uma ferramenta única: parasitas nos quais o gene ap2-g pode ser ligado, mas o AP2-G não consegue ligar-se ao DNA. Usando repórteres fluorescentes e bioluminescentes, eles acompanharam quando diferentes atores atuam durante o ciclo de 48 horas do parasita nos glóbulos vermelhos. Descobriram que a proteína GDV1 aparece primeiro, cedo em um estágio chamado esquizogonia, e é essencial para dar o pontapé inicial na expressão de ap2-g a partir de seu estado silenciado. Essa ativação inicial ocorreu tanto quando ap2-g codificava o AP2-G normal quanto a versão mutante. Só mais tarde, quando quantidade suficiente de AP2-G funcional se acumulava, é que o forte circuito de autoamplificação e a ativação de outros genes “sexuais” aconteciam. Um marcador chave, uma proteína chamada MSRP1, acendeu apenas em parasitas com AP2-G funcional, fornecendo um meio prático de distinguir parasitas comprometidos com o sexo em estágios iniciais e tardios. Nas linhagens mutantes com a troca para leucina, o GDV1 ainda conseguia despertar o ap2-g, mas a proteína AP2-G defeituosa não conseguia conduzir o processo adiante, de modo que o desenvolvimento sexual parava.
Implicações para interromper a disseminação da malária
Para o leitor geral, a conclusão é simples: os parasitas da malária dependem de uma fechadura molecular extremamente sensível para decidir se serão transmissíveis. Este estudo mostra que mudar apenas um “dente” dessa fechadura — uma única valina na região que agarra o DNA do AP2-G — impede o parasita de formar estágios infecciosos para mosquitos. Ao mesmo tempo, esclarece que outra proteína, o GDV1, atua antes como a chave que primeiro destranca o gene ap2-g silenciado, antes que o AP2-G fortaleça sua própria produção e ligue um programa sexual mais amplo. Ao mapear essa sequência de eventos e criar linhagens de parasitas repórter que brilham quando cada etapa ocorre, o trabalho fornece ferramentas poderosas para rastrear drogas ou fatores humanos que interfiram no comprometimento sexual. A longo prazo, mirar a região de ligação ao DNA do AP2-G ou a etapa de ativação dirigida pelo GDV1 pode formar a base de novas estratégias que não apenas curam a malária em um paciente, mas cortam por completo a cadeia de transmissão.
Citação: Prajapati, S.K., Dong, J.X., Morahan, B.J. et al. A single valine to leucine switch disrupts Plasmodium falciparum AP2-G DNA binding and reveals GDV1’s role in ap2-g activation. Nat Commun 17, 1719 (2026). https://doi.org/10.1038/s41467-026-68416-1
Palavras-chave: transmissão da malária, Plasmodium falciparum, desenvolvimento de gametócitos, AP2-G, GDV1