Clear Sky Science · pt
Mecanismos hierárquicos controlam a remoção da RNA polimerase II bloqueada por lesões no DNA
Quando as máquinas copiadoras de genes encontram um obstáculo
Cada segundo, milhões de pequenas máquinas moleculares chamadas RNA polimerase II percorrem nosso DNA, copiando genes em RNA. Mas quando o DNA é danificado — por exemplo pela luz ultravioleta (UV) do sol — essas máquinas podem parar. Se cópias paradas se acumularem, as células deixam de ler seus genes adequadamente, o que é especialmente perigoso para células cerebrais e pode levar a doenças raras como a síndrome de Cockayne. Este estudo revela, em detalhes, como nossas células detectam essas máquinas bloqueadas e as reiniciam ou removem antes que causem danos duradouros.
Uma nova forma de observar engarrafamentos celulares
Para entender como as células eliminam as polimerases bloqueadas, os pesquisadores construíram uma “câmera de trânsito” temporal para a transcrição. Eles usaram um fármaco que permite que as moléculas de RNA polimerase II já presentes continuem em movimento, mas impede que novas iniciem a jornada, e então criaram um pequeno ponto de dano por UV dentro de cada núcleo celular. Ao seguir uma marca química específica na forma ativa da polimerase, puderam observar com que rapidez ela desaparecia da zona danificada em comparação com o restante do genoma. Em paralelo, desenvolveram um ensaio complementar que analisava a quantidade total de polimerase ativa em extratos celulares, revelando não apenas quando as polimerases deixavam o DNA, mas quando eram degradadas pelo sistema de eliminação da célula.
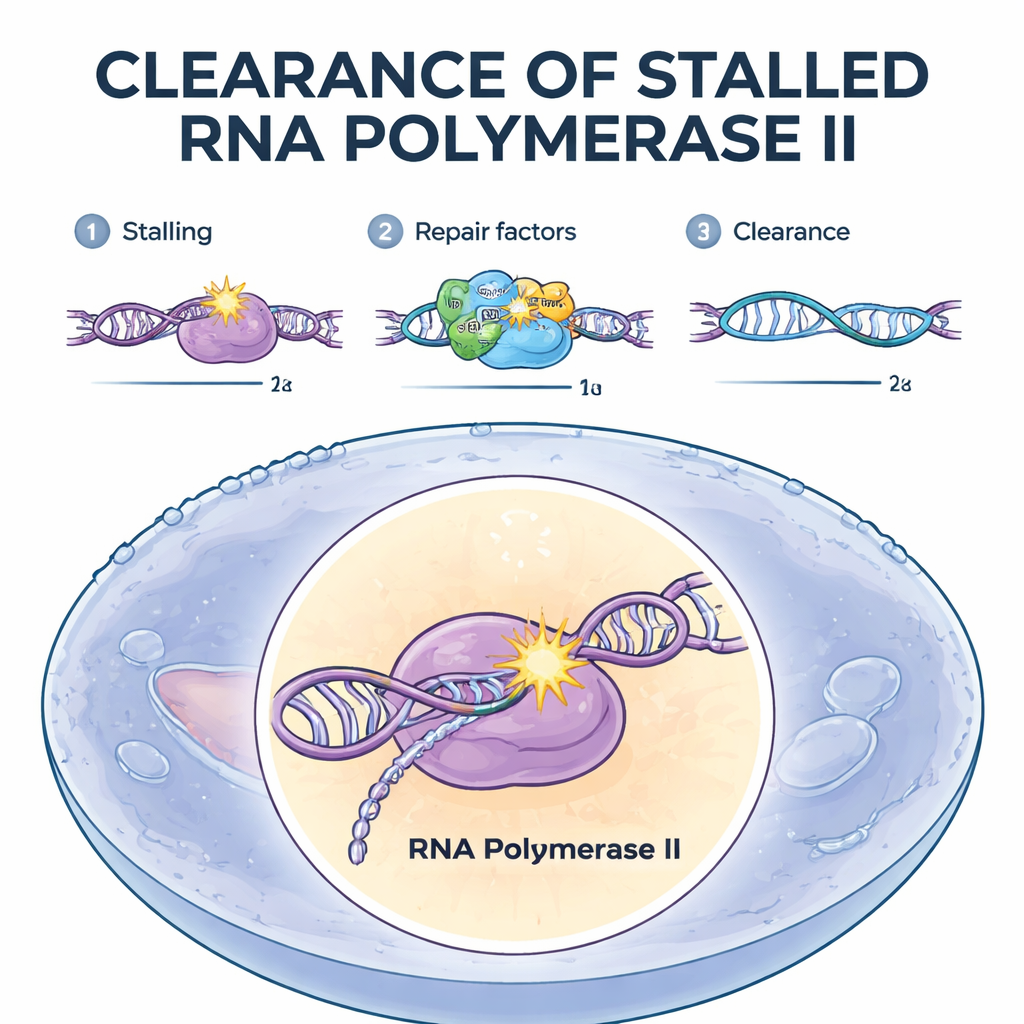
Marcando as máquinas paradas para remoção
O grupo concentrou-se na reparação acoplada à transcrição, um sistema especializado que corrige lesões em genes que estão sendo lidos ativamente. Eles usaram um conjunto pareado de linhagens celulares humanas, cada uma faltando um fator de reparo diferente. Duas proteínas, CSB e CSA, emergiram como guardiãs decisivas. Quando qualquer uma delas estava ausente, a RNA polimerase II se acumulava e permanecia teimosamente nos locais de dano, e a célula falhava em degradá‑la. Bioquimicamente, essas células também não conseguiam ligar pequenas etiquetas de ubiquitina a um sítio chave na polimerase. Em contraste, células sem proteínas de reparo tardias — aquelas que recortam e substituem o DNA danificado — ainda removiam a polimerase normalmente. Isso mostrou que a marcação inicial por ubiquitina da polimerase parada é o gatilho crítico para decidir seu destino.
Duplas equipes de limpeza: uma rápida e outra como reserva
Uma vez marcada, a célula pode escolher entre duas vias para removê‑la. A rota principal e rápida depende de um grande complexo de reparo chamado TFIIH, e em particular da sua subunidade helicase XPD, que usa energia para desenrolar o DNA. Proteínas auxiliares, incluindo ELOF1, UVSSA e STK19, trazem o TFIIH até a polimerase parada e posicionam XPD no DNA logo à frente dela. Usando novos testes em células de pacientes que carregam uma mutação que torna XPD incapaz de desenrolar DNA, os autores mostraram que quando XPD não consegue desenrolar o DNA, a remoção da polimerase desacelera dramaticamente, mesmo que o restante da maquinaria de reparo esteja presente. Isso indica que a ação mecânica de tração de XPD é o que normalmente “solta” a polimerase da lesão para que as enzimas de reparo alcancem o local danificado.
Um plano B lento, porém essencial
O estudo também revelou uma via de emergência mais lenta para remover a polimerase parada. Essa via depende de VCP (também conhecido como p97), uma proteína que reconhece marcas de ubiquitina e pode extrair proteínas da cromatina à força. Em células saudáveis com TFIIH plenamente funcional, bloquear VCP teve apenas um efeito menor. Mas em células onde o TFIIH estava ausente, mal posicionado ou com a helicase inativa, a remoção da polimerase tornou‑se quase totalmente dependente de VCP. Nesses casos, o VCP ainda conseguia puxar a polimerase marcada para longe do DNA, mesmo quando o reparo normal não podia prosseguir. Crucialmente, essa via de reserva ainda exigia alguma marcação por ubiquitina, explicando por que células sem CSB ou CSA — e portanto sem marcas de ubiquitina — falhavam tanto na via principal quanto na de backup.
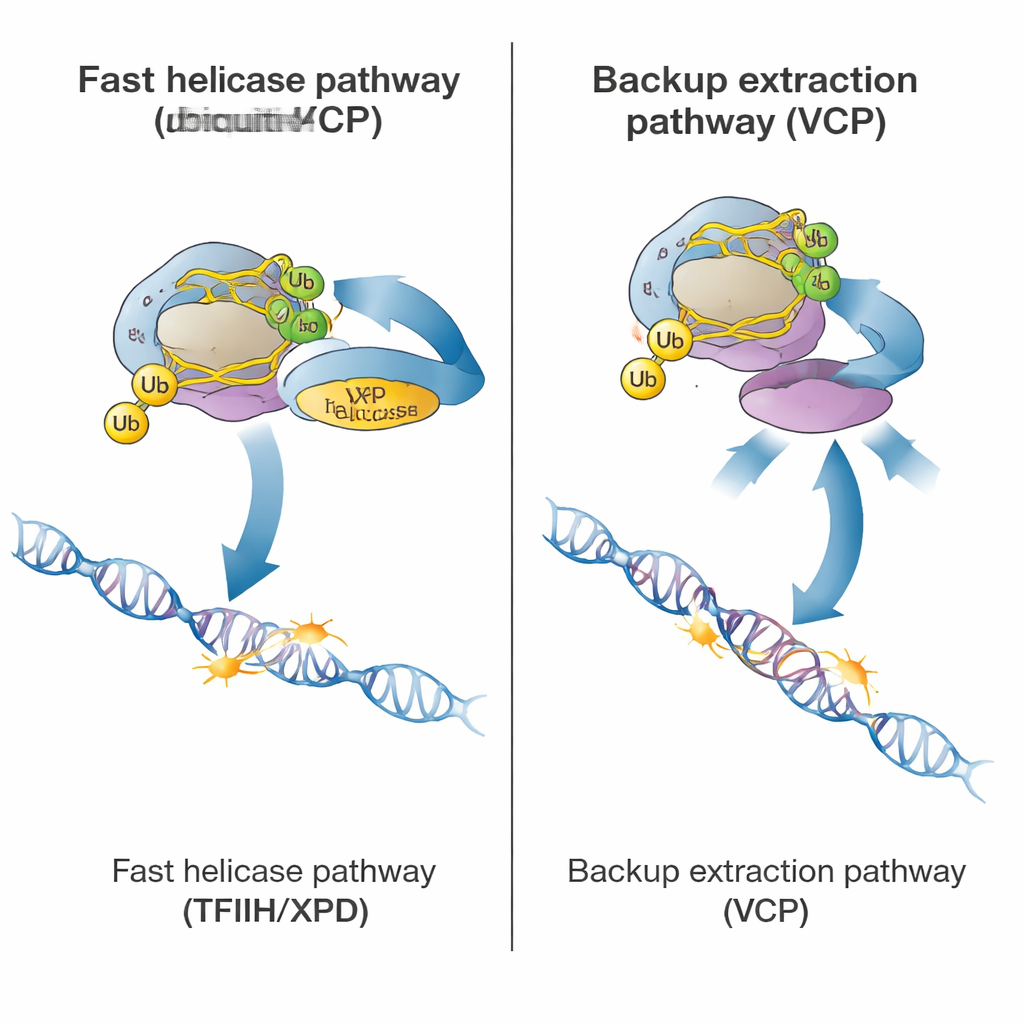
Por que isso importa para saúde e doença
Em conjunto, o trabalho delineia um programa hierárquico de segurança que as células usam sempre que a RNA polimerase II encontra um dano no DNA. Primeiro, CSB e CSA sinalizam a máquina parada com ubiquitina. Se tudo estiver funcionando corretamente, TFIIH e sua helicase XPD desaloja rapidamente a polimerase para que a lesão seja recortada e reparada. Se o TFIIH não puder cumprir sua função, o VCP intervém para extrair a polimerase e enviá‑la para degradação, impedindo que ela entupa a expressão gênica mesmo que o dano no DNA permaneça. Esse quadro ajuda a explicar por que defeitos hereditários em CSB ou CSA causam problemas neurológicos particularmente graves: sem a marcação por ubiquitina, as células perdem tanto a via principal dirigida pelo reparo quanto a via de extração de reserva, deixando polimerases presas em genes danificados e a transcrição cronicamente bloqueada.
Citação: van der Meer, P.J., Yakoub, G., Tsukada, K. et al. Hierarchical mechanisms control the clearance of DNA lesion–stalled RNA polymerase II. Nat Commun 17, 1647 (2026). https://doi.org/10.1038/s41467-026-68413-4
Palavras-chave: reparação do DNA acoplada à transcrição, RNA polimerase II, danos no DNA induzidos por UV, ubiquitilação de proteínas, síndrome de Cockayne