Clear Sky Science · pt
Visualização in situ da heterogeneidade fenotípica de Clostridioides difficile e morfologia celular individual durante infecção intestinal
Por que os microrganismos intestinais não se comportam todos da mesma forma
Clostridioides difficile, frequentemente chamado de C. diff, é um microrganismo hospitalar notório que pode causar diarreia grave e às vezes com risco de vida após antibióticos perturbarem as bactérias normais do intestino. Ainda assim, mesmo quando essas bactérias são geneticamente idênticas e compartilham o mesmo ambiente, células individuais podem se comportar de maneira muito diferente. Este estudo revela, com detalhe sem precedentes, como células únicas de C. diff ligam ou desligam a produção de toxinas e até mudam de forma enquanto infectam o intestino de camundongos, oferecendo pistas sobre por que a doença pode ser tão persistente e difícil de tratar.
Rastreando um invasor intestinal perigoso em tempo real
Para entender como células individuais de C. diff atuam dentro do corpo, os pesquisadores precisavam de uma forma de vê‑las claramente em meio à comunidade densa e diversa de micróbios intestinais. Eles engenheiraram cepas de C. diff que brilham continuamente em cores intensas ao microscópio, usando proteínas fluorescentes especiais que não interferem na capacidade das bactérias de crescer ou causar doença. Ao infectar camundongos tratados com antibióticos com essas cepas fluorescentes e então fatiar e corar o cólon, puderam localizar as posições e comportamentos exatos de milhares de células bacterianas individuais dentro do tecido intestinal intacto. 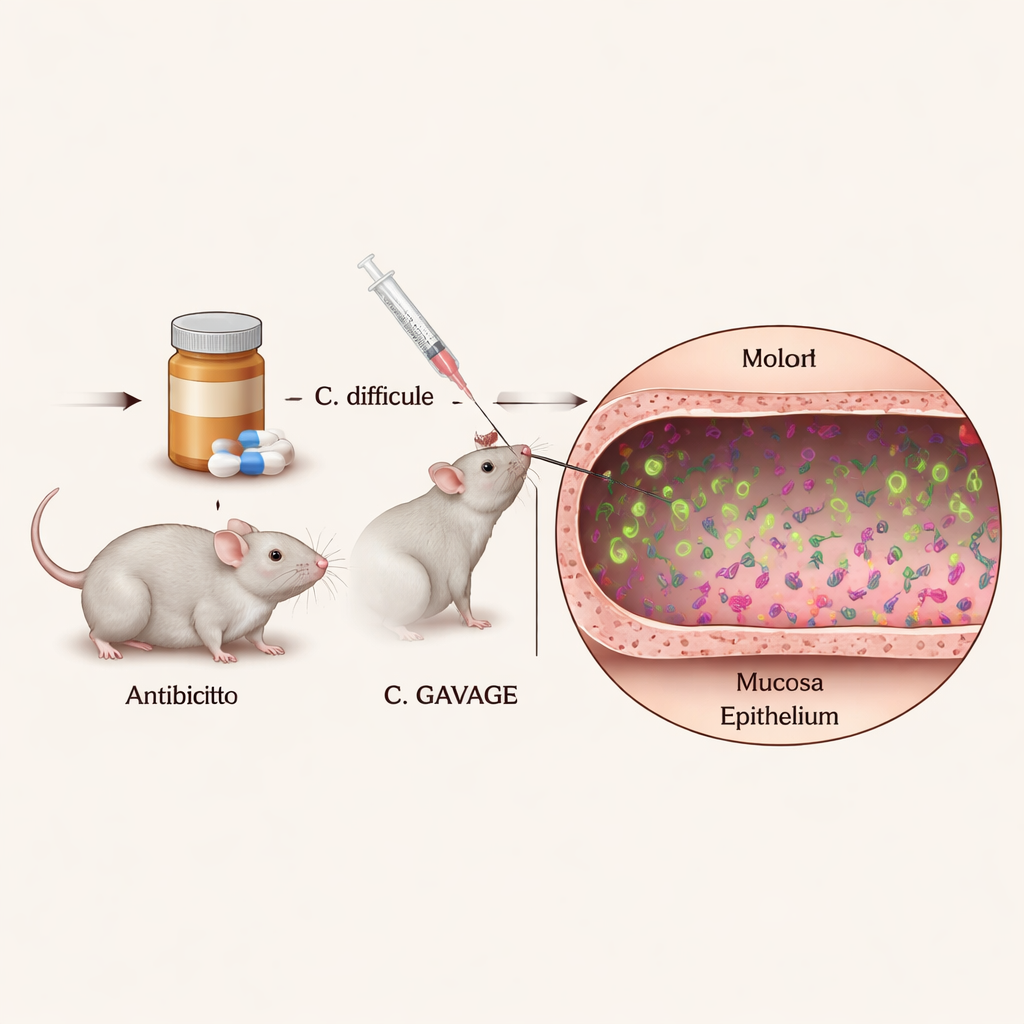
Onde as bactérias vivem no cólon
As imagens mostraram que a maioria das células de C. diff vive no centro do conteúdo do cólon, conhecido como lúmen, confirmando que o organismo é principalmente um patógeno “lúmenal” livre‑flutuante. Contudo, uma minoria notável de células apareceu de forma consistente próxima à camada de muco e diretamente ao lado da superfície epitelial — a fina camada de células que reveste o cólon e atua como barreira para o mundo externo. Essa subpopulação de contato próximo não havia sido claramente vista antes em camundongos convencionais com sistemas imunes normais. Importante, as etiquetas fluorescentes engenheiradas não enfraqueceram as bactérias de forma perceptível nos animais, o que indica que as imagens provavelmente refletem o comportamento de C. diff em uma infecção realista.
Quem produz toxina, e onde?
A equipe então adicionou um segundo sinal fluorescente que se ativa apenas quando C. diff ativa seus genes de toxina. As toxinas são as proteínas danosas que lesionam o revestimento intestinal e provocam os sintomas da doença, e são também o que os médicos medem em testes de fezes para diagnosticar a infecção. Surpreendentemente, as bactérias não produziram toxinas todas ao mesmo tempo. Em vez disso, apenas uma fração das células acendeu como “toxina‑ON” a qualquer momento, tanto no início quanto em estágios avançados da infecção. Essa fração foi maior em uma cepa mutante geneticamente programada para superproduzir toxina, mas mesmo ali nem toda célula participava. Igualmente notável, a posição de uma célula — flutuando no lúmen, assentada no muco ou tocando o epitélio — não alterou fortemente nem a frequência com que a toxina era produzida nem a intensidade com que esses genes eram ativados. 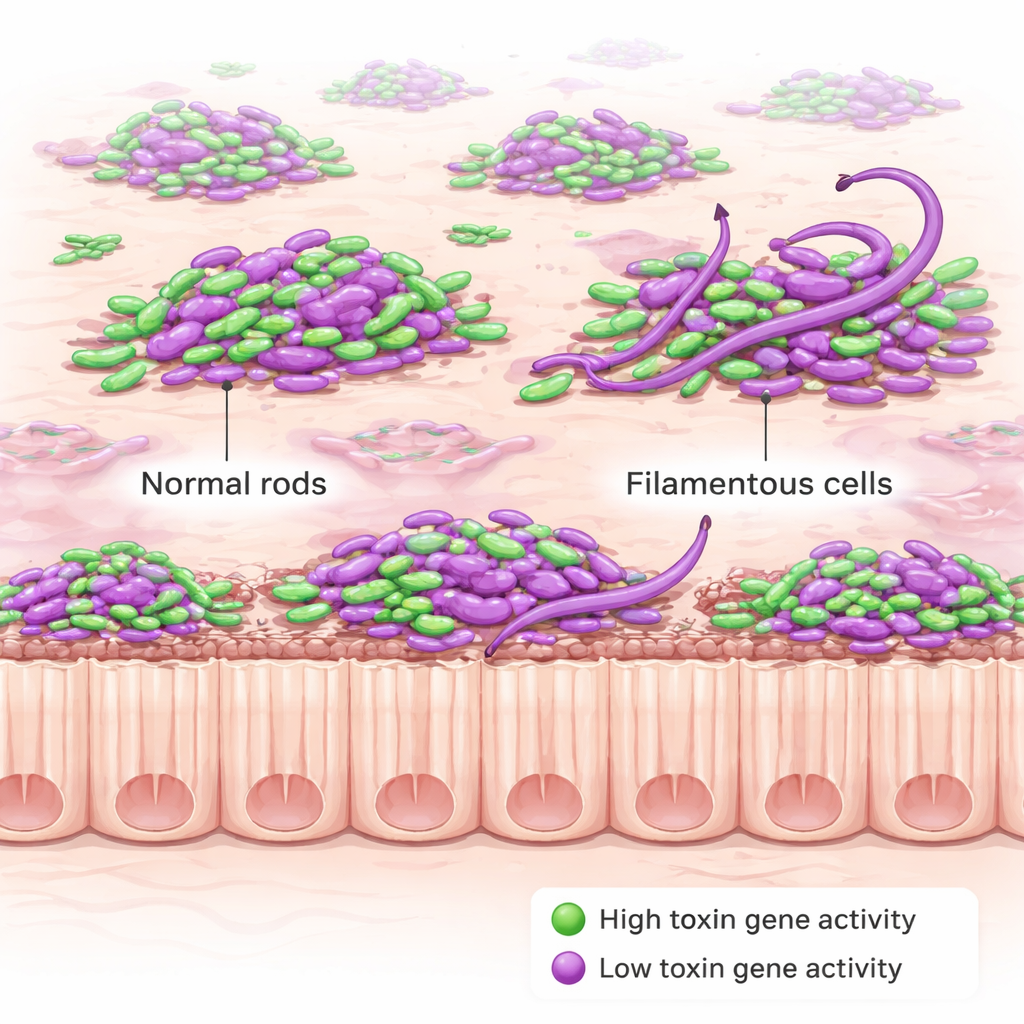
Células que mudam de forma sob estresse
Enquanto mapeavam a produção de toxina, os pesquisadores encontraram um comportamento novo e surpreendente. Em camundongos infectados com a cepa mutante que superproduz toxina, muitas células de C. diff durante a fase aguda da doença tornaram‑se filamentos incomumente longos e curvos, alguns com mais de dez vezes o comprimento dos bacilos curtos normais. Essa morfologia “em forma de fio” apareceu principalmente durante a infecção inicial e grave e diminuiu mais tarde, e não ocorreu quando a mesma cepa foi cultivada em caldo de laboratório. Isso sugere que as condições estressantes dentro do intestino inflamado — e não apenas as mudanças genéticas isoladas — desencadeiam essa remodelação dramática. Experimentos de seguimento mostraram que a perda de uma proteína reguladora chamada RstA, que controla tanto genes de toxina quanto outras respostas ao estresse, contribui para a formação desses filamentos.
O que isso significa para a doença por C. diff
Para não especialistas, a mensagem principal é que mesmo uma única cepa de C. diff se comporta como uma força de trabalho dividida. Algumas células arcam com o custo energético de produzir toxina e danificar o intestino, liberando nutrientes que vizinhas livres de toxina podem explorar. Essa “divisão de trabalho” compartilhada pode ajudar a infecção a persistir e a retornar, porque nem toda célula é igualmente vulnerável a tratamentos que miram toxina ou bactérias em rápido crescimento. O sistema repórter fluorescente recém‑desenvolvido oferece aos cientistas uma forma poderosa de observar, célula por célula, como C. diff e micróbios intestinais relacionados se adaptam ao longo do tempo e do espaço dentro do corpo. Esse conhecimento pode, em última instância, orientar terapias voltadas não apenas para matar bactérias, mas para perturbar os papéis prejudiciais de subpopulações específicas que impulsionam a doença e a recorrência.
Citação: DiBenedetto, N.V., Donnelly-Morell, M.L., Kumamoto, C.A. et al. In situ visualization of Clostridioides difficile phenotypic heterogeneity and single-cell morphology during gut infection. Nat Commun 17, 1716 (2026). https://doi.org/10.1038/s41467-026-68411-6
Palavras-chave: Clostridioides difficile, microbioma intestinal, toxinas bacterianas, heterogeneidade fenotípica, imagem fluorescente