Clear Sky Science · pt
Modelagem do metabolismo específico de tecidos em Drosophila identifica desregulação metabólica induzida por dieta rica em açúcar no músculo em níveis de reação e via
Por que este estudo com moscas-da-fruta interessa à saúde humana
A ingestão excessiva de açúcar pode sobrecarregar a capacidade do corpo de gerir combustíveis, contribuindo ao longo do tempo para o desenvolvimento de diabetes tipo 2. Este estudo usa moscas-da-fruta para revelar, com notável detalhe, como tecidos diferentes lidam com o metabolismo e como uma dieta rica em açúcar perturba a função muscular. Como as moscas compartilham muitos genes metabólicos e sistemas de órgãos com os humanos, essas descobertas ajudam a explicar o que pode dar errado em nossos próprios músculos sob uma sobrecarga prolongada de açúcar.
Mapeando o metabolismo tecido a tecido
Nossos corpos, como os das moscas, são constituídos por tecidos que desempenham papéis metabólicos muito diferentes: o músculo queima combustível, o tecido adiposo o armazena, o intestino processa alimentos, e assim por diante. Em vez de medir cada enzima diretamente, os pesquisadores construíram “mapas” de grande escala do metabolismo — chamados modelos metabólicos em escala genômica — para 32 tecidos distintos das moscas. Eles combinaram uma rede de reações químicas já curada com dados de expressão gênica de célula única, que indicam quais genes metabólicos estão ativados em cada tecido. Isso permitiu comparar quantas reações, metabólitos e genes estão ativos em cada rede específica de tecido e ver quais vias são enfatizadas no músculo, no corpo adiposo, no intestino e em vários tipos de células nervosas.
Funções distintas de combustível para diferentes órgãos
A comparação revelou “personalidades” metabólicas claras entre os tecidos. O corpo adiposo e as oenócitos — contrapartes das moscas para o tecido adiposo e o fígado humanos — continham o conjunto mais rico de reações, especialmente aquelas que queimam gorduras por beta-oxidação. O músculo, em contraste, não tinha a maior rede, mas possuía a maior fração de reações que transportam substâncias para dentro e fora das células, sugerindo que o músculo é um centro importante de troca de combustíveis e blocos de construção com o resto do corpo. Os cientistas também verificaram se as vias previstas correspondiam aos padrões reais de metabólitos medidos em diferentes regiões do corpo. Usando metabolômica direcionada, analisaram centenas de pequenas moléculas de cabeças, tórax, intestinos e abdômens de moscas e, em seguida, checaram se as vias enriquecidas nos dados se sobrepunham às previstas pelos modelos. No músculo e no corpo adiposo, a correspondência foi forte, dando confiança de que os modelos específicos de tecido capturaram biologia real melhor do que apenas a expressão gênica.
O que uma dieta rica em açúcar faz ao fluxo de combustível do músculo
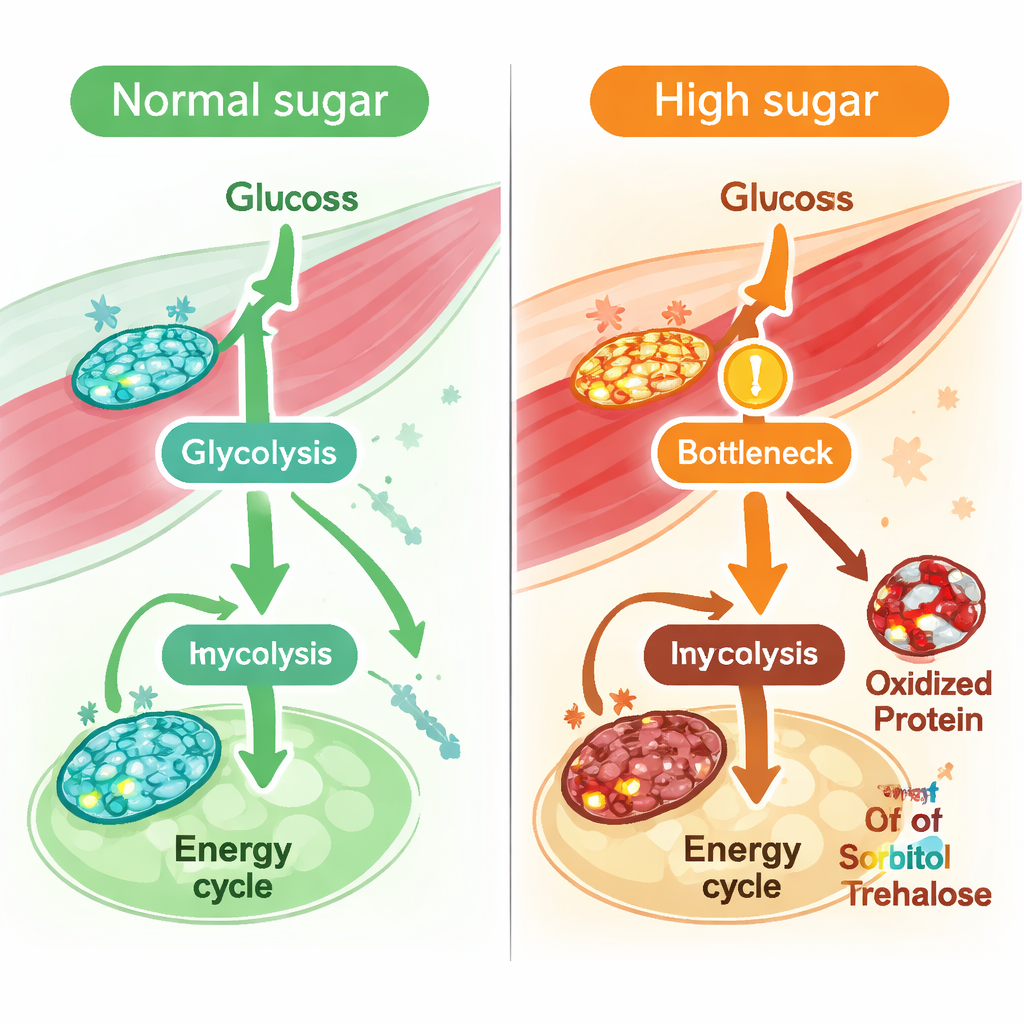
Com um modelo muscular validado em mãos, a equipe simulou o que acontece quando as moscas são alimentadas com uma dieta rica em açúcar a longo prazo, um modelo bem estabelecido de diabetes tipo 2. Eles restringiram o modelo usando características conhecidas do músculo diabético, como redução da captação de glicose e atividade lenta no ciclo central de energia mitocondrial. Análises computacionais de “fluxo” — cálculos da velocidade máxima das reações — mostraram reduções amplas em reações que dependem do par redox NAD/NADH, moléculas que transportam elétrons e são essenciais para a produção de energia. Em particular, reações na via central de queima de açúcar, a glicólise, desaceleraram, incluindo as catalisadas pela enzima GAPDH. O modelo também previu uma queda de cerca de um quarto na capacidade geral do músculo de produzir NADH, sugerindo um equilíbrio redox comprometido. Medições diretas no músculo torácico das moscas confirmaram que a razão NAD/NADH de fato diminuiu sob dieta rica em açúcar.
Rastreando açúcar marcado e proteínas oxidadas
Para verificar se esses gargalos preditos realmente ocorriam em animais vivos, os pesquisadores alimentaram moscas com dieta rica em açúcar contendo glicose uniformemente marcada com carbono-13 e então rastrearam para onde o carbono marcado foi. Eles encontraram acúmulo de intermediários glicolíticos iniciais a montante da GAPDH, enquanto produtos a jusante e suas frações marcadas caíram, sinalizando uma desaceleração real nesse ponto e abaixo dele. De forma similar, as contribuições do carbono da glicose para o ciclo central de energia foram reduzidas. Ao mesmo tempo, a proteômica redox — um método que detecta alterações oxidativas em aminoácidos específicos de proteínas — mostrou aumento da oxidação de muitas enzimas glicolíticas, incluindo múltiplos sítios na GAPDH. Ao longo da glicólise, enzimas que exibiram mais modificações oxidativas tenderam a mostrar quedas maiores no fluxo previsto, embora seus níveis proteicos gerais permanecessem em sua maioria inalterados. Isso sugere que o dano químico por estresse oxidativo, em vez da perda de abundância das enzimas, é um fator chave na redução do processamento de açúcar no músculo.
Problemas ocultos no manuseio de frutose e sacarose
Olhando além de reações isoladas, a equipe fez a média dos fluxos ao longo de vias inteiras para ver quais eram mais perturbadas pelo açúcar em excesso. Glicólise, o ciclo de energia e a fosforilação oxidativa apresentaram declínios, mas uma das maiores reduções previstas foi no metabolismo da frutose. O perfil de metabólitos do músculo sustentou essa ideia: níveis de sorbitol e trealose/sacarose aumentaram, e uma enzima chave que converte trealose em glicose, a trealase, mostrou tanto atividade prevista reduzida quanto aumento da oxidação em um resíduo de metionina sensível. Em conjunto, essas descobertas apontam para uma perturbação mais ampla em como o músculo processa açúcares alimentares — especialmente combustíveis derivados de frutose e sacarose — sob sobrecarga crônica de açúcar.
O que isso significa para entender o diabetes
Em termos simples, este trabalho mostra que o excesso de açúcar não apenas sobrecarrega a corrente sanguínea; também remodela silenciosamente como as células musculares direcionam e queimam combustíveis. Ao construir mapas metabólicos detalhados e específicos de tecido para a mosca-da-fruta e confrontá‑los com metabolômica, rastreamento isotópico e proteômica redox, os pesquisadores revelam que o açúcar em excesso induz estresse redox, oxida enzimas glicolíticas chave como a GAPDH, desacelera a quebra do açúcar e perturba vias relacionadas à frutose. Essas percepções, obtidas em um organismo-modelo altamente manejável, oferecem um quadro poderoso para identificar quais reações e vias podem ser mais importantes proteger ou restaurar no músculo humano para prevenir ou tratar o diabetes tipo 2.
Citação: Moon, S.J., Hu, Y., Dzieciatkowska, M. et al. Modeling tissue-specific Drosophila metabolism identifies high sugar diet-induced metabolic dysregulation in muscle at reaction and pathway levels. Nat Commun 17, 1692 (2026). https://doi.org/10.1038/s41467-026-68395-3
Palavras-chave: metabolismo de Drosophila, modelos metabólicos específicos de tecido, dieta rica em açúcar, glicólise muscular, regulação redox