Clear Sky Science · pt
Excisão precisa de repetições ampliadas GGC em NOTCH2NLC via CRISPR/Cas9 para tratar a doença de inclusão intranuclear neuronal
Editando o DNA para enfrentar um distúrbio cerebral misterioso
A doença de inclusão intranuclear neuronal (NIID) é uma condição cerebral rara, porém devastadora, que pode causar demência, problemas de movimento e até morte precoce. Atualmente não há cura. Este estudo investiga se uma poderosa ferramenta de edição gênica, o CRISPR, pode ser usada para recortar um trecho minúsculo, porém tóxico, de DNA que conduz a NIID, oferecendo uma visão de como tratamentos futuros poderiam reescrever nossos genes para combater doenças cerebrais. 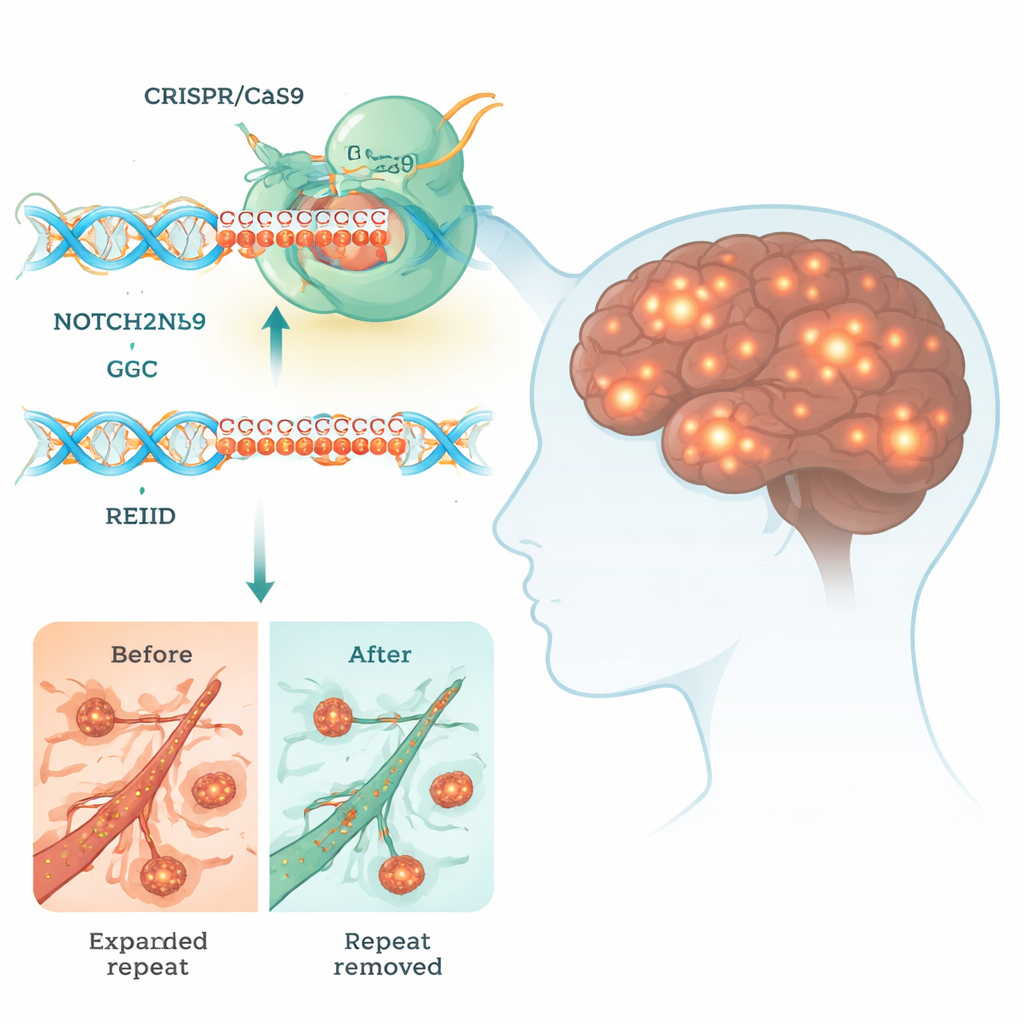
Um culpado genético oculto
Muitos distúrbios hereditários do cérebro são causados por curtas sequências de DNA que cresceram muito além do tamanho normal. Na NIID, o problema é uma corrida ampliada de unidades de três letras de DNA, "GGC", em um gene chamado NOTCH2NLC. Embora esse trecho esteja em uma região que não codifica diretamente uma proteína clássica, ele ainda pode ser lido pela maquinaria celular para produzir cadeias anômalas de poliglicina (polyG). Essas cadeias pegajosas se agregam em grumos dentro do núcleo de neurônios e de outros tecidos, perturbando processos vitais como produção de energia, processamento de RNA e o tráfego de moléculas entre núcleo e citoplasma.
O desafio da cirurgia gênica precisa
Projetar um tratamento de edição gênica para NIID é incomumente difícil porque NOTCH2NLC tem várias genes irmãos quase idênticos que são importantes para o desenvolvimento cerebral humano. Se o CRISPR cortar o gene errado, pode causar mais danos do que benefícios. Os pesquisadores examinaram cuidadosamente o DNA ao redor da repetição GGC e encontraram pequenas diferenças de sequência que distinguem NOTCH2NLC de seus parentes. Em seguida, desenharam pares de RNAs guia do CRISPR que direcionam a proteína Cas9 — as "tesouras moleculares" — para cortar logo antes e depois da repetição expandida. Essa estratégia de cortes duplos permite que o sistema de reparo da célula remova o segmento tóxico enquanto preserva o restante da família gênica.
De células em cultura a neurônios derivados de pacientes
A equipe primeiro testou seu desenho de CRISPR em células humanas padrão e em células modificadas para carregar uma grande repetição de NOTCH2NLC. Nesses modelos, o editor cortou eficientemente a repetição, e os níveis de aglomerados de polyG caíram cerca de metade ou mais. Em seguida, avançaram para células-tronco pluripotentes induzidas (iPSCs) derivadas de um paciente com NIID e converteram essas células em células progenitoras neurais, um estágio inicial de células cerebrais. Usando CRISPR, eles ou deletaram a repetição expandida ou a substituiram por uma versão de comprimento normal. Sequenciamento detalhado do DNA e do genoma inteiro mostrou que a edição foi altamente precisa, com poucas evidências de cortes indesejados, e as células editadas continuaram a se dividir e maturar normalmente. 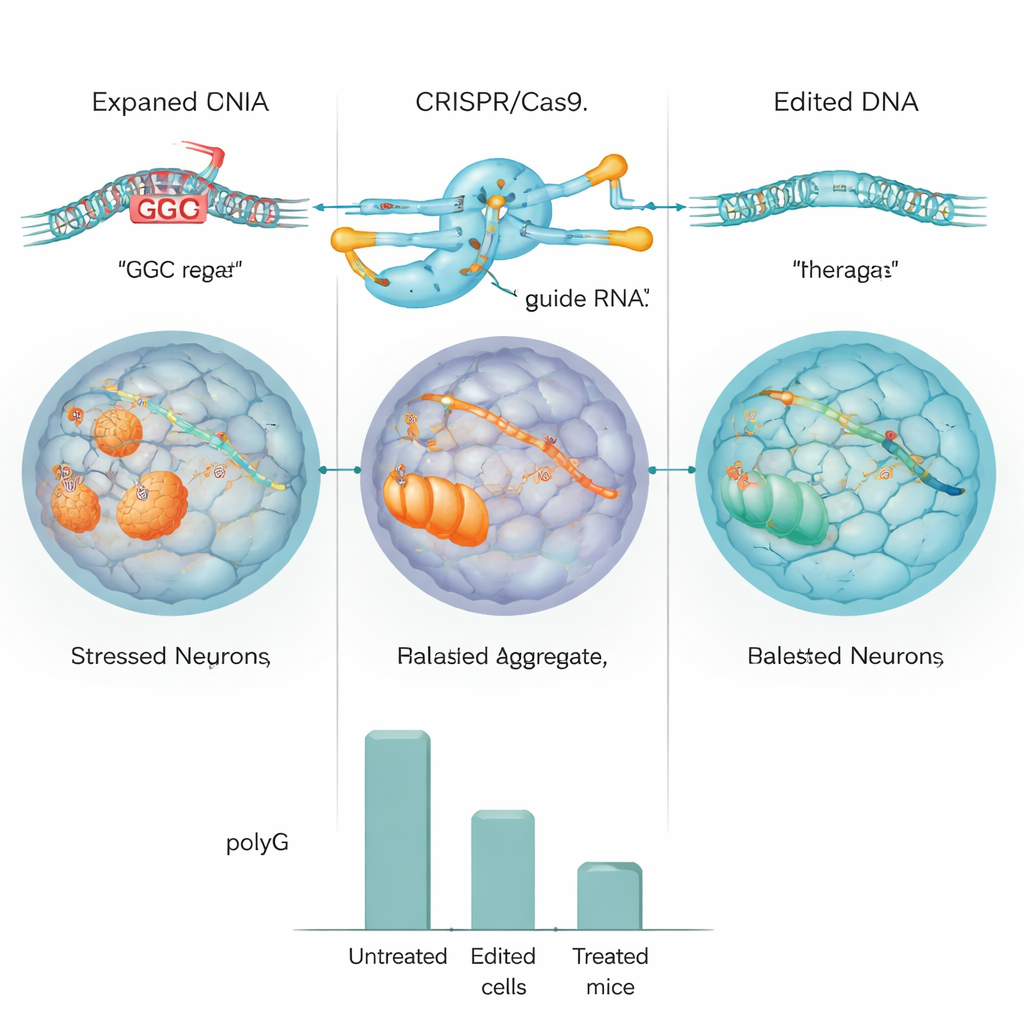
Resgatando cérebro e corpo em um modelo de camundongo
Para ver se essa abordagem poderia realmente melhorar a doença, os pesquisadores recorreram a camundongos engenharia dos para carregar a repetição humana de NOTCH2NLC e desenvolver características semelhantes à NIID, incluindo inclusões nucleares, problemas de movimento e vida útil encurtada. Eles empacotaram o sistema CRISPR em um vírus modificado que pode se espalhar pelo cérebro após uma simples injeção na corrente sanguínea de filhotes recém-nascidos. Em animais tratados, a repetição expandida foi removida com sucesso no tecido cerebral. Como resultado, os níveis tóxicos de polyG caíram acentuadamente, marcadores de saúde dos neurônios melhoraram e a ativação anormal das células de suporte do cérebro diminuiu. Testes comportamentais mostraram que os camundongos tratados se moviam mais, equilibravam-se melhor e sobreviveram por mais tempo do que seus irmãos não tratados. Benefícios semelhantes foram observados no coração, que também acumula polyG nesse modelo.
O que isso pode significar para tratamentos futuros
Para o público leigo, a mensagem principal é que a NIID parece ser impulsionada em grande parte por uma repetição de DNA específica e ampliada, e remover essa repetição com precisão pode reverter muitos sinais da doença em células e em camundongos. Este trabalho ainda não se traduz em uma terapia pronta para uso em humanos: os pesquisadores precisam refinar a segurança a longo prazo, melhorar os métodos de entrega e testar em animais maiores e mais semelhantes aos humanos. Mas o estudo oferece uma forte prova de conceito de que a edição gênica cuidadosamente direcionada pode silenciar com segurança uma repetição tóxica enquanto poupa genes estreitamente relacionados. Essa estratégia pode um dia ser adaptada não só para NIID, mas também para outras doenças do cérebro e do músculo causadas por expansões de repetições semelhantes.
Citação: Xie, N., Pan, Y., Tong, H. et al. Precise excision of expanded GGC repeats in NOTCH2NLC via CRISPR/Cas9 for treating neuronal intranuclear inclusion disease. Nat Commun 17, 1683 (2026). https://doi.org/10.1038/s41467-026-68385-5
Palavras-chave: Edição gênica CRISPR, doença de inclusão intranuclear neuronal, doenças por expansão de repetições, NOTCH2NLC, neurodegeneração