Clear Sky Science · pt
Design generativo de IA baseado em sequência de sintases de triptofano versáteis
Ensinando novas habilidades às enzimas com IA
A sociedade moderna depende de moléculas — medicamentos, materiais e produtos químicos especiais — que costumam ser fabricadas por processos que consomem muita energia e poluem. Os catalisadores da natureza, as enzimas, podem realizar trabalhos semelhantes de forma limpa e eficiente, mas encontrar ou construir a enzima certa para uma nova aplicação industrial é lento e incerto. Este estudo mostra que a inteligência artificial generativa, a mesma classe de tecnologia por trás de chatbots que escrevem texto, pode ser usada para projetar enzimas totalmente novas que não apenas funcionam bem em laboratório, mas às vezes superam os melhores resultados que a evolução e anos de engenharia já produziram.
Por que as enzimas importam no dia a dia
Enzimas são pequenas máquinas proteicas que aceleram reações químicas em células vivas. Químicos aprenderam a reaproveitá‑las para fabricar medicamentos, ingredientes alimentares e outros produtos valiosos usando menos energia e reagentes tóxicos do que a química tradicional. O problema é que cada nova aplicação costuma exigir uma enzima com desempenho sob medida — capaz de aceitar materiais iniciais específicos, resistir às condições de processamento e produzir altos rendimentos. A “evolução dirigida” convencional melhora enzimas gerando e testando muitas versões mutantes, geração após geração. Isso funciona bem, mas depende de uma enzima inicial razoável e pode levar meses ou anos de tentativa e erro, deixando muitas reações úteis inexploradas.
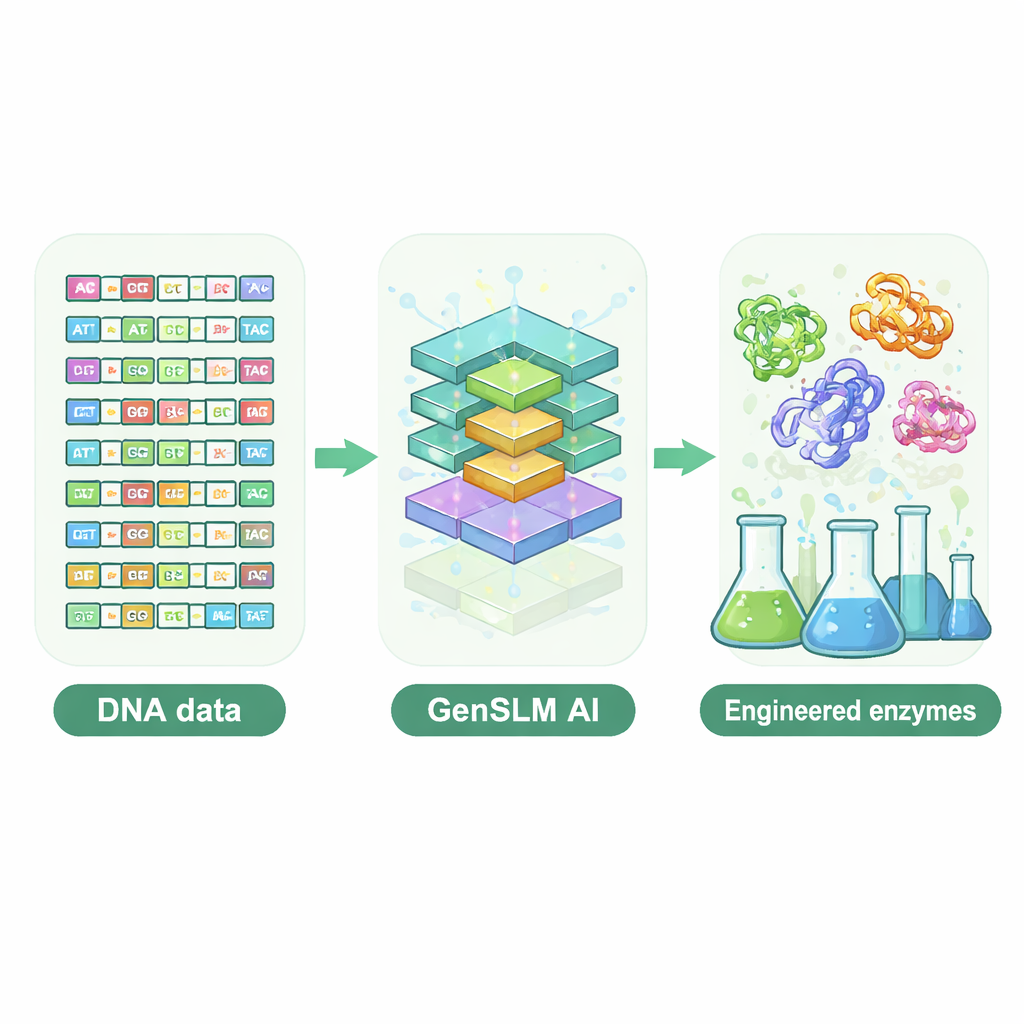
Deixando um modelo de linguagem escrever DNA
Os pesquisadores recorreram a um modelo de linguagem em escala genômica chamado GenSLM, que aprende padrões no DNA da mesma forma que um modelo de linguagem aprende gramática e estilo no texto. Em vez de trabalhar com sequências de proteínas prontas, o GenSLM lê e escreve DNA em códons de três letras, espelhando como as células traduzem genes em proteínas. A equipe primeiro afinou o GenSLM com dezenas de milhares de genes naturais para uma subunidade enzimática particularmente complexa, chamada TrpB, que ajuda a construir o aminoácido triptofano. Em seguida, pediram ao modelo que gerasse milhares de genes trpB inteiramente novos. Filtros computacionais simples eliminaram sequências que eram muito curtas ou muito longas, improváveis de dobrar corretamente ou quase idênticas a enzimas naturais conhecidas, deixando 105 candidatos diversos para testes experimentais em bactérias.
Dos designs computacionais a catalisadores funcionais
Quando essas 105 enzimas TrpB projetadas por IA foram produzidas em E. coli, muitas se dobraram bem e foram expressas em altas quantidades. Dezenas conseguiram realizar sua função principal: converter indol e o aminoácido parceiro natural, serina, em triptofano. Algumas funcionaram de forma robusta mesmo em temperaturas elevadas, apesar de não terem sido projetadas explicitamente para resistência ao calor. Em testes comparativos, um subconjunto das TrpB‑GenSLM igualou ou superou uma enzima de referência que havia sido evoluída em laboratório ao longo de anos para funcionar de forma autônoma a 75 °C. Um design de destaque, rotulado 230, produziu mais triptofano do que essa referência usada industrialmente tanto em temperatura ambiente quanto em alta temperatura, mostrando que um modelo treinado apenas em dados de sequência pode alcançar desempenho de alto nível diretamente.
Nova flexibilidade além do que a natureza construiu
A equipe então desafiou as enzimas com um painel de substratos não naturais — derivados de indol, um parceiro tipo álcool diferente e um composto fluorado usado na fabricação de fármacos. Versões naturais de TrpB geralmente são exigentes: favorecem fortemente seus substratos nativos e apresentam pouca atividade com alternativas. Notavelmente, as enzimas geradas pela IA foram frequentemente mais aventureiras. Para cada substrato não natural testado, pelo menos um design do GenSLM mostrou atividade mensurável, e muitos tiveram desempenho superior ao das enzimas naturais. Novamente, a variante 230 se destacou, convertendo todos os sete substratos alternativos com rendimentos que variaram de modestos a quase completos, uma amplitude de “promiscuidade” não vista antes nesta família enzimática. Ainda assim, quando os pesquisadores compararam 230 com seu parente natural mais próximo — diferindo em apenas 78 de 400 posições de aminoácidos — descobriram que a enzima natural não apresentava essa versatilidade, apesar de sua estrutura geral e resíduos-chave do sítio ativo serem quase idênticos.
O que isso significa para a química verde futura
Para um não especialista, a mensagem principal é que um modelo de IA treinado apenas em sequências de DNA existentes pode imaginar novas enzimas realistas que a natureza nunca tentou, algumas das quais são ferramentas melhores para a química do que as que usamos atualmente. Essas variantes de TrpB projetadas por IA mantêm a forma e a função essenciais de suas congêneres naturais, mas ganham uma habilidade incomum de lidar com muitos materiais iniciais diferentes. Essa flexibilidade poderia reduzir dramaticamente a quantidade de trabalho de laboratório necessária para descobrir rotas enzimáticas para novos medicamentos e outros produtos. À medida que o projeto, a síntese de DNA e os testes se tornarem mais rápidos e baratos, modelos generativos semelhantes podem transformar a descoberta de enzimas de uma caça ao tesouro lenta em uma tarefa de design rápida e rotineira, ajudando a deslocar mais da química industrial para processos mais limpos e movidos por enzimas.
Citação: Lambert, T., Tavakoli, A., Dharuman, G. et al. Sequence-based generative AI design of versatile tryptophan synthases. Nat Commun 17, 1680 (2026). https://doi.org/10.1038/s41467-026-68384-6
Palavras-chave: engenharia de enzimas, IA generativa, projeto de proteínas, sintase de triptofano, biocatálise