Clear Sky Science · pt
Tmem110 regula a conformação do TRPML1 para manter a homeostase endolisossomal e prevenir vazamento de DNA mitocondrial e processamento patológico de DNA próprio
Por que o vazamento de DNA após a lesão importa
Quando sofremos um trauma severo, como um forte impacto na cabeça, o dano não se limita ao local da lesão. Muitos pacientes desenvolvem uma reação sistêmica perigosa na qual pulmões, fígado, rins e outros órgãos começam a falhar. Este estudo revela como estruturas minúsculas dentro das células — lisossomos, mitocôndrias e detectores imunológicos — se comunicam para decidir se o corpo limpa silenciosamente os destroços ou entra em uma resposta imune dirigida a si mesmo. Entender esse sistema oculto de limpeza pode abrir novas formas de prevenir insuficiência orgânica após traumas e de tratar doenças autoimunes e inflamatórias.
Da lesão na cabeça à crise em todo o corpo
A lesão cerebral traumática (TBI) pode desencadear uma poderosa tempestade inflamatória chamada síndrome da disfunção múltipla de órgãos (MODS), mas como o dano no cérebro se espalha para órgãos distantes tem sido obscuro. Os autores focam em monócitos e macrófagos, células imunes que patrulham o sangue e os tecidos e atuam como coletores profissionais de lixo. Após TBI, células morrem de forma descontrolada e liberam mitocôndrias inteiras — pequenas usinas de energia que carregam seu próprio DNA — para a circulação. Esse DNA mitocondrial (mtDNA) se parece suspeitosamente com DNA bacteriano para o sistema imune e pode ativar defesas potentes no estilo antiviral se não for removido rapidamente. Normalmente, as células internalizam essas mitocôndrias errantes em compartimentos ácidos chamados lisossomos, onde enzimas digerem o DNA antes que ele vaze para o citosol. 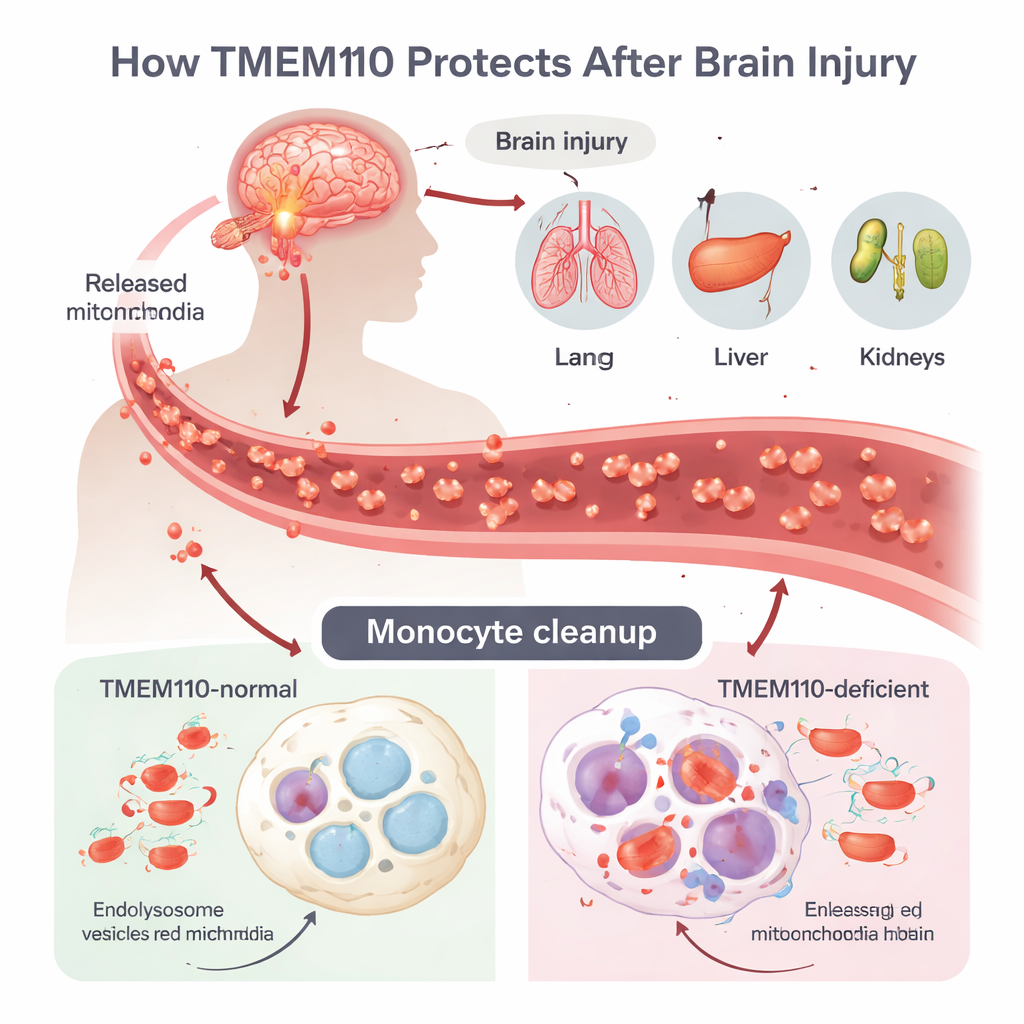
Uma proteína porteira que mantém os lisossomos estáveis
A equipe identificou TMEM110, uma proteína que atravessa a membrana do retículo endoplasmático (uma grande rede de membranas intracelulares), como uma porteira crucial nesse processo. Usando camundongos geneticamente modificados que careciam de TMEM110 apenas em monócitos e macrófagos, eles criaram um modelo controlado de lesão cerebral. Comparados com camundongos normais, os animais deficientes em TMEM110 desenvolveram níveis muito mais altos de interferons tipo I — potentes moléculas de sinalização antiviral — no sangue e no líquido cefalorraquidiano. Seus pulmões, fígado, rins e linfonodos apresentaram danos mais severos, e a sobrevida a longo prazo após TBI foi marcadamente pior. Quando os pesquisadores bloquearam o receptor de interferon tipo I, ou substituíram a medula óssea mutante por células normais, as taxas de lesão orgânica e morte caíram, mostrando que sinalização excessiva por interferon a partir de monócitos periféricos é um motor chave da MODS nesse contexto.
Como o manejo iônico defeituoso permite que o DNA escape
Ao investigar essas células imunes, os autores descobriram que os lisossomos deficientes em TMEM110 estavam quimicamente desequilibrados: eram menos ácidos e sobrecarregados de cálcio. Nessas condições, a enzima DNase II — que normalmente fragmenta DNA nos lisossomos — perdeu atividade, as membranas lisossomais ficaram frágeis e o mtDNA escapou para o citosol circundante. Experimentos de laboratório com monócitos humanos engolfando mitocôndrias doadoras marcadas confirmaram que, sem TMEM110, mais mtDNA vazou para o citosol e desencadeou uma onda de genes estimulados por interferon. O estudo mostra que TMEM110 atua controlando outra proteína, o canal iônico lisossomal TRPML1. Quando TMEM110 está presente, ele faz contato físico com TRPML1 e o desloca para uma conformação “aberta” que cria minúsculos pontos de liberação de cálcio na superfície do lisossomo. Esses fluxos controlados de cálcio ajudam a manter a acidez adequada, sustentam a reparação da membrana e mantêm o mtDNA preso e degradado no interior. 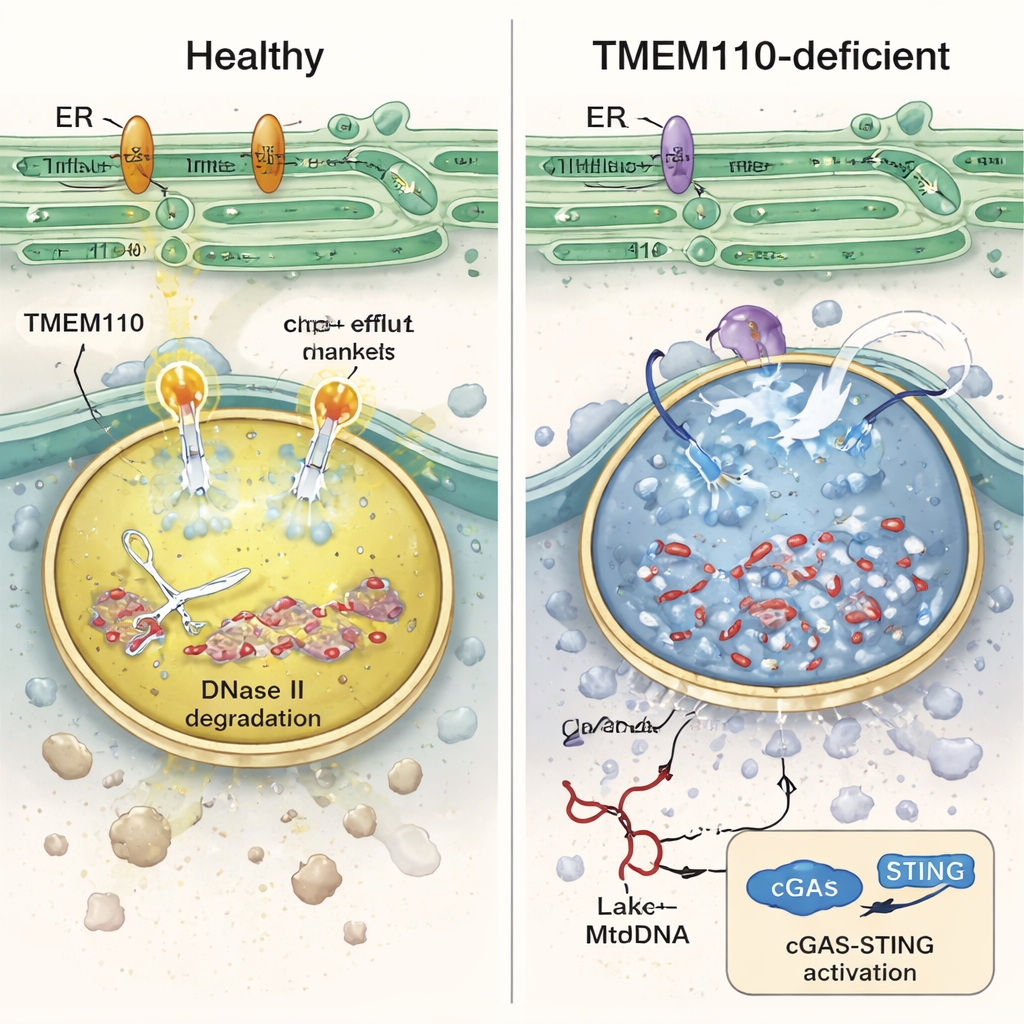
Um circuito de realimentação com o sistema de alarme de DNA da célula
Uma vez que o mtDNA vaza para o citosol, ele é reconhecido pela via cGAS–STING, o principal sistema de alarme da célula para DNA errante. Curiosamente, TMEM110 também se liga ao STING em repouso e o mantém sequestrado no retículo endoplasmático, prevenindo alarmes desnecessários. Quando DNA citossólico se acumula, o STING é ativado e afrouxa sua ligação com TMEM110. Isso, por sua vez, expõe uma região diferente de TMEM110 que interage com TRPML1 e aumenta o efluxo de cálcio lisossomal, criando um circuito de retroalimentação: a detecção de DNA próprio ativa um mecanismo que melhora a remoção do DNA. Mutações em STING associadas a doenças humanas autoinflamatórias perturbam essa transferência, prendendo TMEM110 em um estado inibido e contribuindo para ativação crônica de interferon. Em camundongos portadores de tal mutação em STING, TBI levou a danos orgânicos piores e maior mortalidade, mas a entrega de um pequeno fragmento de TMEM110 aos lisossomos usando uma terapia de nanopartícula lipídica de mRNA restaurou parcialmente o controle do mtDNA e melhorou a sobrevida.
Pistas de pacientes e caminhos para novos tratamentos
Os autores então analisaram uma coorte clínica de 143 pessoas com lesão cerebral relacionada a trauma e MODS. Pacientes cujos monócitos apresentavam níveis mais altos de TMEM110 logo após a lesão tinham maior probabilidade de recuperar a função orgânica e sobreviver. Aqueles com menor TMEM110 mostraram mais mtDNA circulante e mitocôndrias descelularizadas, respostas de interferon mais intensas, pontuações maiores de falência orgânica e perfis mais amplos de autoanticorpos, incluindo anticorpos contra DNA e proteínas nucleares. Esses padrões espelharam de perto os achados em camundongos, apoiando a ideia de que o controle da estabilidade lisossomal e da eliminação do mtDNA conduzido por TMEM110 é um mecanismo compartilhado na doença humana.
O que isso significa para pacientes com trauma severo
Em termos práticos, este trabalho sugere que após um grande ferimento nosso sistema imune enfrenta uma escolha delicada: digerir silenciosamente a enxurrada de DNA próprio liberado por células moribundas, ou interpretá‑la como uma invasão viral e desencadear um ataque total que pode danificar nossos próprios órgãos. TMEM110, ao ajustar um canal iônico lisossomal e coordenar‑se com o sensor de DNA STING, ajuda as células a escolherem o caminho mais seguro. Quando esse sistema falha — porque TMEM110 está ausente, STING é mutado ou os lisossomos estão sobrecarregados — o mtDNA escapa, o alarme continua tocando e o dano multiorgânico segue. Alvejar esse eixo TMEM110–TRPML1–STING, por exemplo com terapias de mRNA direcionadas aos lisossomos, pode oferecer uma nova maneira de prevenir ou tratar a falência de órgãos e complicações tipo autoimune após trauma severo.
Citação: Feng, Z., Pan, Y., Zhou, J. et al. Tmem110 regulates the conformation of TRPML1 to maintain endolysosomal homeostasis and prevent mitochondrial DNA leakage and pathological self-DNA processing. Nat Commun 17, 1678 (2026). https://doi.org/10.1038/s41467-026-68382-8
Palavras-chave: lesão cerebral traumática, DNA mitocondrial, lisossomos, interferon tipo I, via cGAS‑STING