Clear Sky Science · pt
Estrutura por criomicroscopia eletrônica do complexo ubiquitina ligase humano COP1-DET1
Como as células decidem quais proteínas destruir
Dentro de cada célula, milhares de proteínas precisam ser continuamente construídas, remodeladas ou destruídas no momento certo. Este artigo examina uma das principais máquinas de “controle de qualidade” da célula, um fragmentador molecular que decide quando remover reguladores gênicos potentes ligados ao câncer e ao desenvolvimento. Ao revelar sua estrutura tridimensional em detalhe quase atômico, os autores mostram como essa máquina pode alternar entre um estado empilhado e inativo e uma forma ativa que processa substratos — um insight que pode, eventualmente, ajudar a projetar drogas para ativá‑la ou inibi‑la.
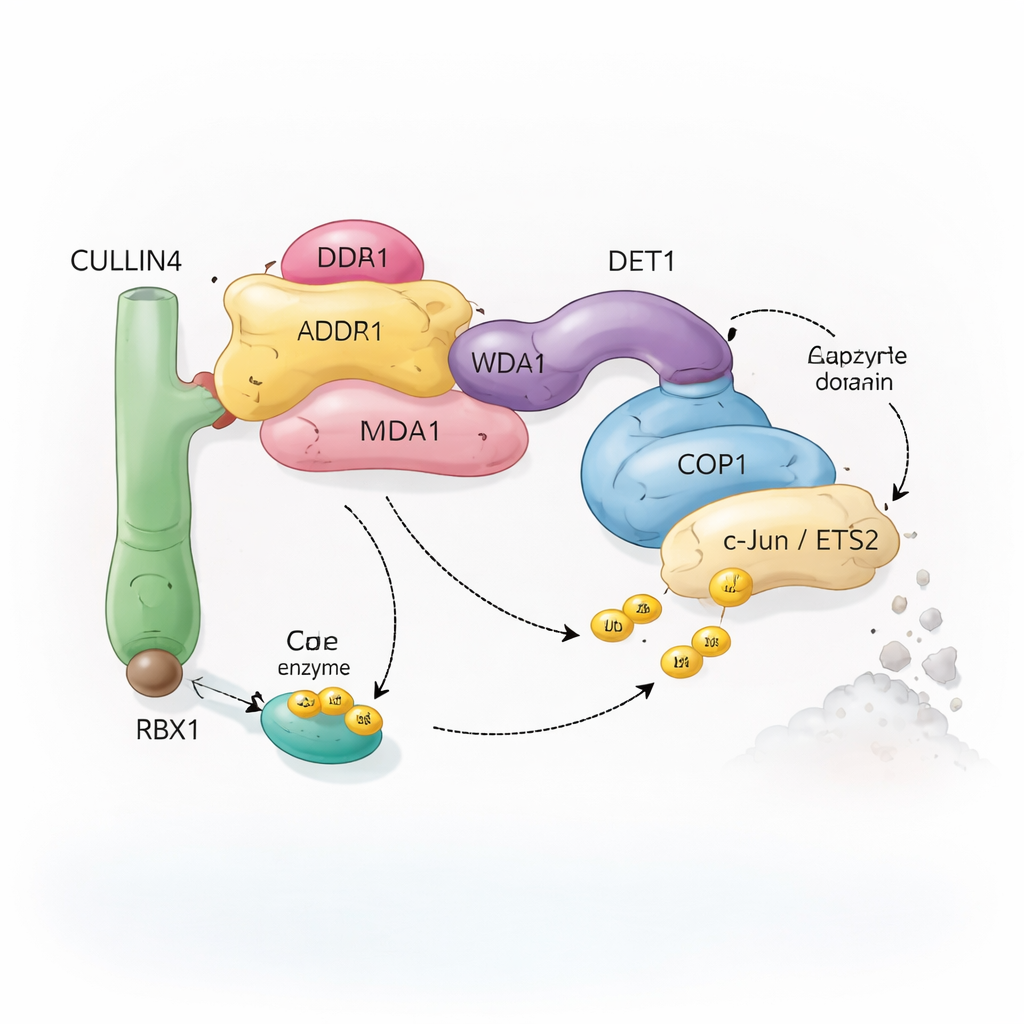
Uma equipe molecular de reciclagem com muitas peças
As células dependem de um sistema chamado ubiquitinação para marcar proteínas para reciclagem. Pequenas moléculas de ubiquitina atuam como bandeiras removíveis que indicam à célula se uma proteína deve ser modificada, realocada ou destruída. Complexos enzimáticos especiais, conhecidos como ligases de ubiquitina, anexam essas bandeiras a alvos selecionados. O complexo estudado aqui tem como centro o COP1, uma proteína encontrada de plantas a humanos, que ajuda a marcar importantes fatores de transcrição — proteínas que controlam quais genes são ativados ou desativados. O COP1 não age sozinho: pode se conectar a um conjunto maior montado em torno de uma proteína andaime chamada CULLIN4, além de vários adaptadores nomeados DDB1, DDA1 e DET1. Juntos, esses componentes formam uma “equipe de reciclagem” flexível que reconhece fatores de transcrição específicos como c‑Jun e ETS2, muitos dos quais estão envolvidos no crescimento celular e no câncer.
Capturando o complexo em 3D
Para entender como essa equipe opera, os pesquisadores usaram criomicroscopia eletrônica de partícula isolada, uma técnica que imagina proteínas congeladas rapidamente e reconstrói suas formas em alta resolução. Eles recriaram o sistema humano COP1–DET1 em células cultivadas, purificaram os complexos e visualizaram vários estados estruturais distintos. Primeiro, resolveram a estrutura do módulo DDB1–DDA1–DET1, que atua como um núcleo central. O DET1 adota uma forma incomum e parcialmente flexível, em vez de um disco rígido, com uma “garra” protuberante que pode agarrar enzimas parceiras. Em seguida, ao adicionar COP1 e uma classe de enzimas auxiliares conhecidas como E2s, capturaram montagens maiores que mostram como todas as peças se encaixam, revelando tanto pilhas compactas quanto arranjos dimerizados mais abertos (com dois COP1).
Uma pilha inativa e um dímero ativo
Uma das descobertas mais marcantes é uma estrutura empilhada, em forma de filamento, composta por camadas repetidas do complexo. Em cada camada, oito moléculas de COP1 entrelaçam‑se por seus segmentos de coiled‑coil, formando um anel em forma de losango. Suas regiões de reconhecimento de substrato, chamadas domínios WD40, estão todas orientadas para a mesma direção e ficam parcialmente protegidas pelas camadas vizinhas. Esse empacotamento apertado provavelmente representa um estado “desligado” no qual o acesso para proteínas‑alvo é limitado. Em contraste, quando a equipe examinou complexos coexpressos com substratos do COP1, como c‑Jun ou ETS2, observaram uma forma dimerizada diferente: dois COP1 dispostos lado a lado, com seus domínios WD40 voltados para fora e disponíveis para se ligar aos curtos motivos “VP” encontrados em muitos fatores de transcrição. Testes bioquímicos confirmaram que apenas esse estado dimerizado suporta eficientemente a construção de cadeias longas de ubiquitina sobre c‑Jun.
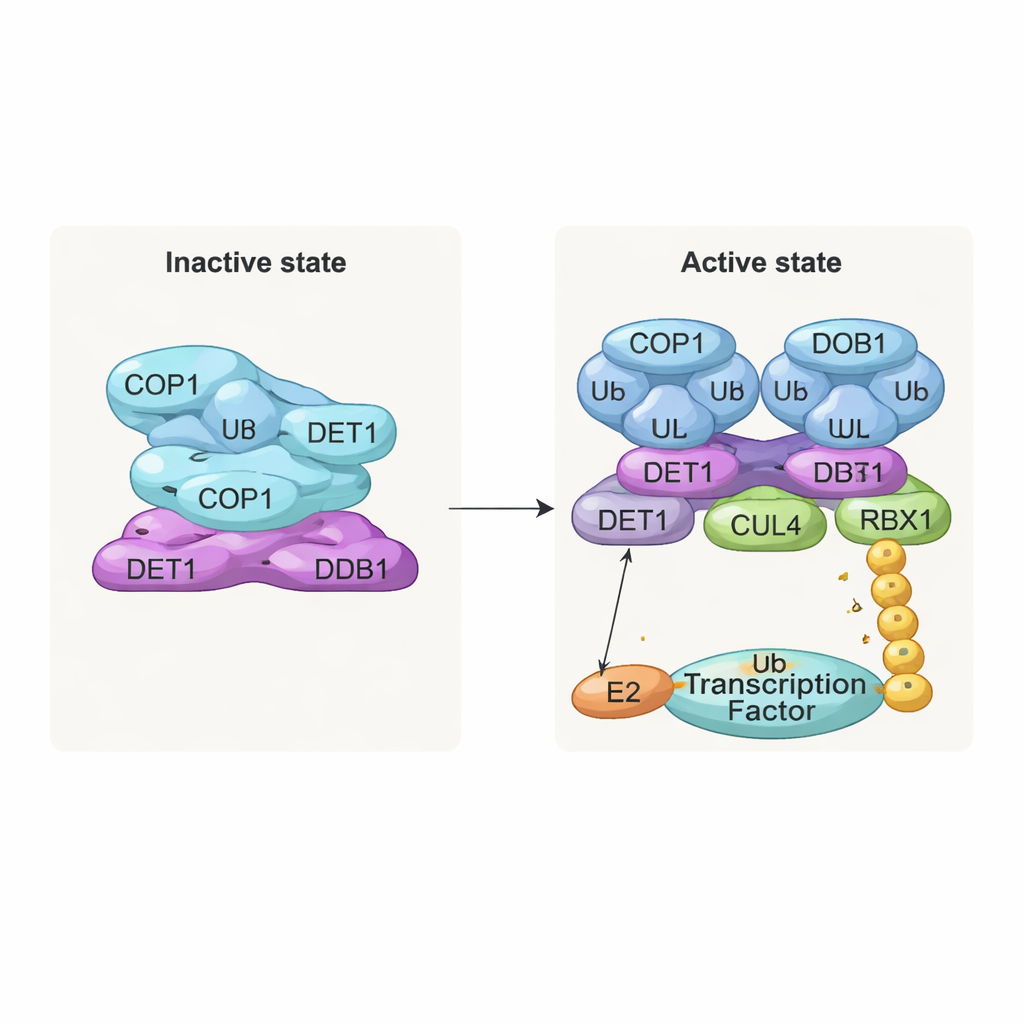
DET1 como ponte flexível e diretor de tráfego
O DET1 surge como o organizador chave que liga todas as partes da máquina. Sua região N‑terminal encaixa‑se em DDB1, ancorando o complexo ao andaime CULLIN4, enquanto sua região de garra envolve uma família de enzimas E2 chamada Ube2e. Experimentos mutacionais detalhados mostram que o DET1, e não o COP1, é o que agarra diretamente esses E2s, posicionando‑os próximo à região catalítica RING do COP1. Nessa configuração, a Ube2e parece ajudar a colocar as primeiras etiquetas de ubiquitina no substrato. Uma segunda enzima E2, Ube2d3, é então recrutada pela haste CULLIN4–RBX1 para alongar essas etiquetas em cadeias mais longas que sinalizam a degradação completa. Em outras palavras, o DET1 age como uma ponte flexível que apresenta um E2 ao COP1, enquanto o andaime maior traz um segundo E2 para finalizar o trabalho.
Por que isto importa para saúde e doença
Ao mapear esses estados estruturais e suas atividades, o estudo explica como o mesmo conjunto de proteínas pode alternar entre uma forma inativa empilhada e um dímero ativo que direciona fatores de transcrição para a destruição. Essa alternância é especialmente importante para fatores como o c‑Jun, que impulsionam a divisão celular e estão fortemente ligados ao câncer quando desregulados. Entender como COP1 e DET1 cooperam — como a garra do DET1 seleciona E2s específicos, como a superfície WD40 do COP1 reconhece substratos contendo VP, e como o dímero ativo se forma — fornece um roteiro para trabalhos futuros. Em longo prazo, drogas que estabilizem a pilha inativa ou favoreçam o dímero ativo poderiam oferecer novas formas de modular vias de controle gênico no câncer e em outras doenças em que a degradação de proteínas se altera.
Citação: Wang, S., Teng, F., Stjepanovic, G. et al. Cryo-EM structure of the human COP1-DET1 ubiquitin ligase complex. Nat Commun 17, 543 (2026). https://doi.org/10.1038/s41467-026-68375-7
Palavras-chave: ligase de ubiquitina, COP1, degradação de proteínas, estrutura por criomicroscopia eletrônica, c-Jun