Clear Sky Science · pt
INCENP e CDCA8 prevêem resposta à quimioterapia neoadjuvante e desfechos no carcinoma espinocelular esofágico
Por que esta pesquisa importa para pacientes com câncer
Muitas pessoas com cânceres do esôfago, mama ou pulmão recebem quimioterapia intensa antes da cirurgia para reduzir os tumores. Ainda assim, apenas cerca de metade desses pacientes obtém benefício real; para os demais, os fármacos causam efeitos colaterais sem deter o câncer. Este estudo faz uma pergunta simples, porém crucial: podemos prever com antecedência quem responderá à quimioterapia e podemos tornar o tratamento mais eficaz para aqueles que atualmente não respondem?
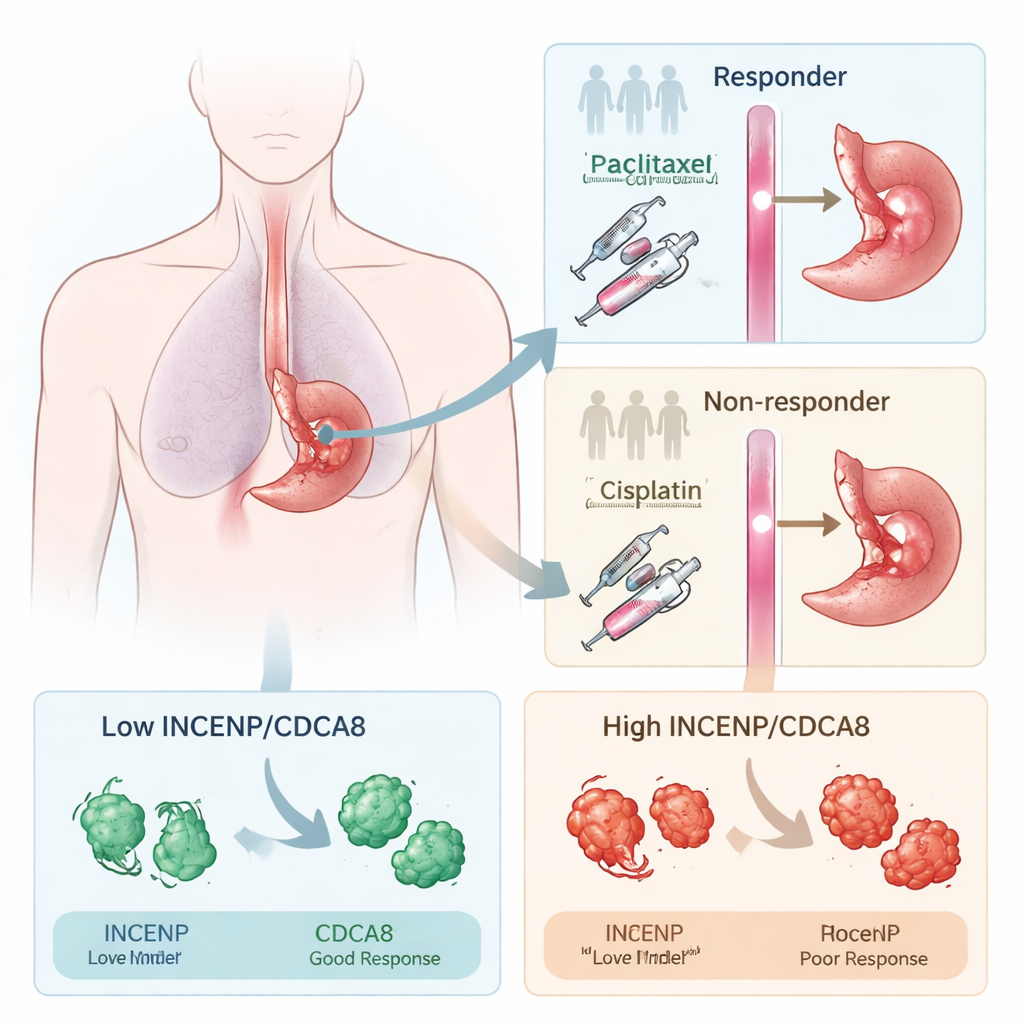
Ver quem responde ao tratamento
Os pesquisadores concentraram-se em um esquema pré-cirúrgico padrão que combina paclitaxel e cisplatina, usado amplamente em vários cânceres. Trabalhando primeiro com pacientes com carcinoma espinocelular do esôfago, eles compararam amostras tumorais de pessoas cujos cânceres encolheram fortemente após essa terapia (respondedores) com amostras daqueles cujos tumores mal mudaram (não respondedores). Ao mapear quais genes estavam ativados ou reprimidos, encontraram muitas diferenças relacionadas à forma como as células se dividem, um processo que a quimioterapia visa interromper. Duas proteínas que ajudam a controlar a separação dos cromossomos durante a divisão celular, INCENP e CDCA8, destacaram-se repetidamente por estarem muito mais altas em tumores que resistiram ao tratamento.
Duas proteínas que sinalizam provável resistência
Para testar se INCENP e CDCA8 eram apenas espectadores ou condutores ativos da resistência, a equipe alterou seus níveis em células de câncer esofágico cultivadas em laboratório. Quando reduziram qualquer uma das proteínas, as células cancerosas ficaram muito mais sensíveis ao paclitaxel e à cisplatina, formando menos colônias e apresentando doses muito menores necessárias para matá-las. Quando forçaram as células a produzir INCENP ou CDCA8 em excesso, ocorreu o oposto: os fármacos ficaram menos eficazes. Em camundongos implantados com tumores humanos de esôfago, reduzir essas proteínas fez a quimioterapia reduzir os tumores com mais intensidade. Pacientes cujos tumores continham altos níveis de INCENP e CDCA8 antes do tratamento também apresentaram maior probabilidade de progressão da doença e sobrevivência mais curta, reforçando seu valor como sinais de alerta.
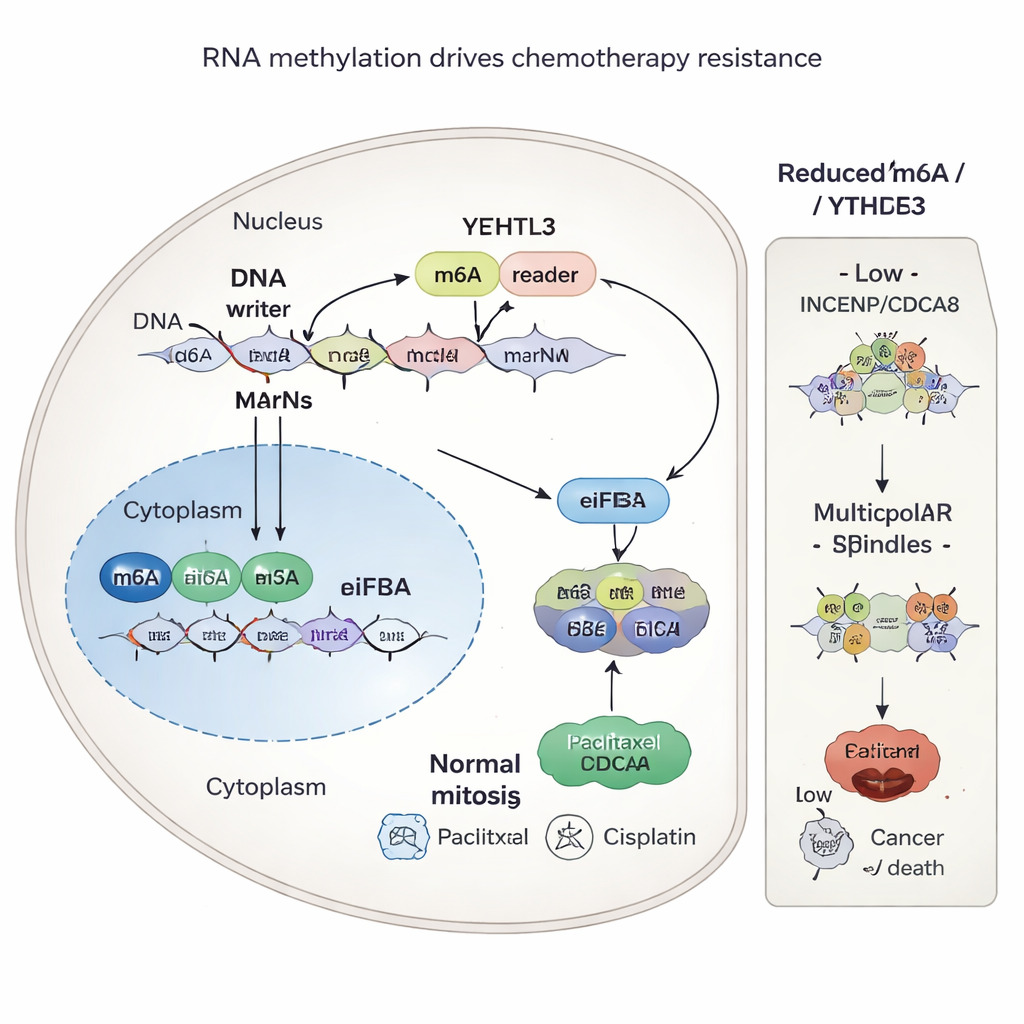
Uma marca química no RNA que alimenta a resistência
O estudo então investigou por que INCENP e CDCA8 são tão abundantes em tumores resistentes. A resposta remeteu a uma marca química sutil no RNA chamada m6A, que funciona como um botão de ajuste para a eficiência com que mensagens genéticas são traduzidas em proteína. Uma enzima chamada METTL3 adiciona essas marcas m6A em pontos específicos dos RNAs que codificam INCENP e CDCA8. Outra proteína, YTHDF3, reconhece essas marcas e ajuda a recrutar a maquinaria de síntese proteica da célula, aumentando a produção das duas proteínas. Quando os cientistas reduziram METTL3 ou YTHDF3, ou bloquearam YTHDF3 com uma pequena molécula chamada Ebselen, as marcas m6A foram perdidas ou ignoradas, os níveis proteicos de INCENP e CDCA8 caíram e as células cancerosas ficaram mais vulneráveis à quimioterapia.
Disruptando a divisão celular para ajudar a quimioterapia
INCENP e CDCA8 fazem parte de uma máquina maior chamada complexo cromossômico de passageiros, que garante que os cromossomos sejam divididos de forma equilibrada entre as células filhas. Em células resistentes, altos níveis dessas proteínas ajudam a manter fusos bipolares organizados durante a divisão celular, permitindo que o câncer sobreviva ao dano causado pelo paclitaxel e pela cisplatina. Quando INCENP e CDCA8 são suprimidos, as células frequentemente formam fusos defeituosos e multipolares. Esse caos na segregação cromossômica empurra as células cancerosas em direção à morte, ampliando o poder letal da quimioterapia. Fundamentalmente, a capacidade de INCENP e CDCA8 de proteger as células dependia desses locais m6A específicos em seus RNAs; mutar esses locais eliminou a resistência.
Além de um tipo de câncer
Como paclitaxel mais cisplatina também é usado para cânceres de pulmão e mama, a equipe examinou amostras de biópsia de pacientes com esses tumores. Nos três tipos de câncer, pessoas cujos tumores apresentavam baixos níveis de INCENP, CDCA8 e YTHDF3 antes da terapia tiveram muito mais probabilidade de responder bem ao tratamento. Análises estatísticas mostraram que combinar esses três marcadores deu um poder particularmente bom para distinguir prováveis respondedores de não respondedores, sugerindo um painel de teste prático que poderia ser usado em múltiplos cânceres.
O que isso significa para pacientes e médicos
Em termos claros, este trabalho identifica uma “impressão digital” molecular que ajuda a explicar por que alguns tumores ignoram a quimioterapia poderosa. Altos níveis de INCENP e CDCA8, impulsionados por um sistema de controle baseado em m6A envolvendo METTL3 e YTHDF3, mantêm as células cancerosas dividindo-se de forma ordenada mesmo sob ataque químico. Medir essas proteínas em uma biópsia poderia ajudar médicos a prever se paclitaxel mais cisplatina provavelmente beneficiará um paciente, poupando outros de um tratamento ineficaz. Ao mesmo tempo, fármacos que bloqueiam essa via poderiam ser combinados com a quimioterapia padrão para induzir erros fatais na divisão em tumores resistentes, potencialmente melhorando a sobrevida de pessoas com vários cânceres importantes.
Citação: Wang, X., Wang, T., Wang, K. et al. INCENP and CDCA8 predict neoadjuvant chemotherapy response and outcomes in esophageal squamous cell carcinoma. Nat Commun 17, 1672 (2026). https://doi.org/10.1038/s41467-026-68371-x
Palavras-chave: quimioterapia neoadjuvante, carcinoma espinocelular do esôfago, resistência à quimioterapia, biomarcadores INCENP e CDCA8, metilação de RNA m6A