Clear Sky Science · pt
Proteases dependentes de ubiquitina ligada a K48 cortam proteínas pós-RER
Como as células decidem quais proteínas destruir
Nossas células removem constantemente proteínas desgastadas ou danificadas, especialmente aquelas incorporadas em membranas que funcionam como portões e sensores. Este artigo revela que as células usam uma pequena etiqueta chamada ubiquitina não apenas como um rótulo genérico de “lixo”, mas como um código que informa às proteínas de membrana exatamente como elas serão degradadas. Compreender esse código ajuda a explicar como as células mantêm a saúde e pode orientar futuras terapias que destroem deliberadamente proteínas causadoras de doenças.
Um código de barras celular para o descarte de proteínas
As células decoram proteínas indesejadas com cadeias de uma pequena proteína chamada ubiquitina. Essas cadeias podem ser ligadas de maneiras diferentes, um pouco como contas enfiadas por furos distintos, e cada padrão pode sinalizar um desfecho diferente. Os autores concentraram-se em proteínas de membrana que já saíram do retículo endoplasmático (RER) e transitam por compartimentos como o Golgi e endossomos. Eles perguntaram se dois tipos comuns de cadeia, chamados de ubiquitina ligada por K48 e por K63, são realmente rótulos intercambiáveis ou se direcionam o cargo para rotas de degradação distintas.
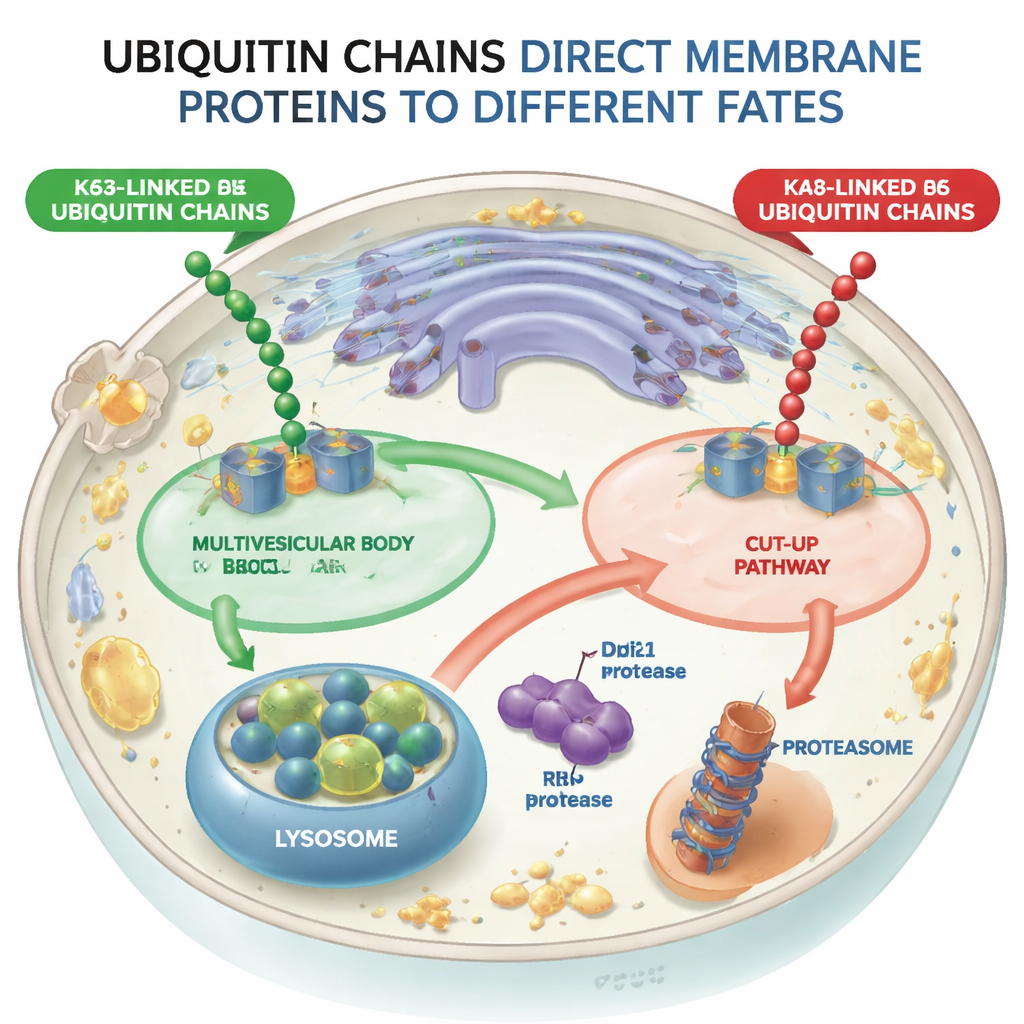
Dois caminhos divergentes para proteínas marcadas
Usando leveduras como modelo, os pesquisadores projetaram máquinas moleculares (ligases de ubiquitina) que podiam anexar tanto cadeias ligadas por K48 quanto por K63 à mesma proteína de membrana teste, um receptor de triagem chamado Vps10. Quando Vps10 recebia cadeias ligadas por K63, era enviado para vesículas internas dentro dos endossomos — estruturas conhecidas como corpos multivesiculares — que eventualmente se fundem com lisossomos, os compartimentos digestivos da célula. Em contraste, quando Vps10 carregava cadeias ligadas por K48, ele não seguia essa via multivesicular. Em vez disso, era desmembrado de uma maneira completamente diferente, mostrando que a célula distingue esses dois tipos de cadeia e que a via multivesicular efetivamente rejeita cargas marcadas por K48.
Uma via “Cut-Up” que fatiam proteínas em dois
A equipe descobriu que as cadeias ligadas por K48 desencadeiam uma via de cisalhamento proteico que chamaram CUT-UP, abreviação de Cleavage of Ubiquitinated Targets by Ubiquitin-dependent Proteases (Clivagem de Alvos Ubiquitinados por Proteases Dependentes de Ubiquitina). Em vez de puxar a proteína inteira para fora da membrana de uma só vez, o CUT-UP a corta em pedaços que são então finalizados pelos sistemas de descarte celulares existentes. Uma enzima-chave, Ddi1, flutua no citosol e corta a porção da proteína de membrana que fica voltada para o citoplasma. Esse fragmento é então digerido pelo proteassoma, o principal triturador de proteínas da célula. Ao mesmo tempo, outra enzima, Rbd2, fica inserida na própria membrana e corta a parte da proteína voltada para o interior do compartimento, liberando-a no espaço que eventualmente se conecta ao lisossomo. Bloquear Ddi1, Rbd2, o proteassoma e as enzimas lisossomais simultaneamente foi necessário para proteger completamente o Vps10 marcado por K48 da destruição, confirmando que todos esses componentes cooperam na via CUT-UP.
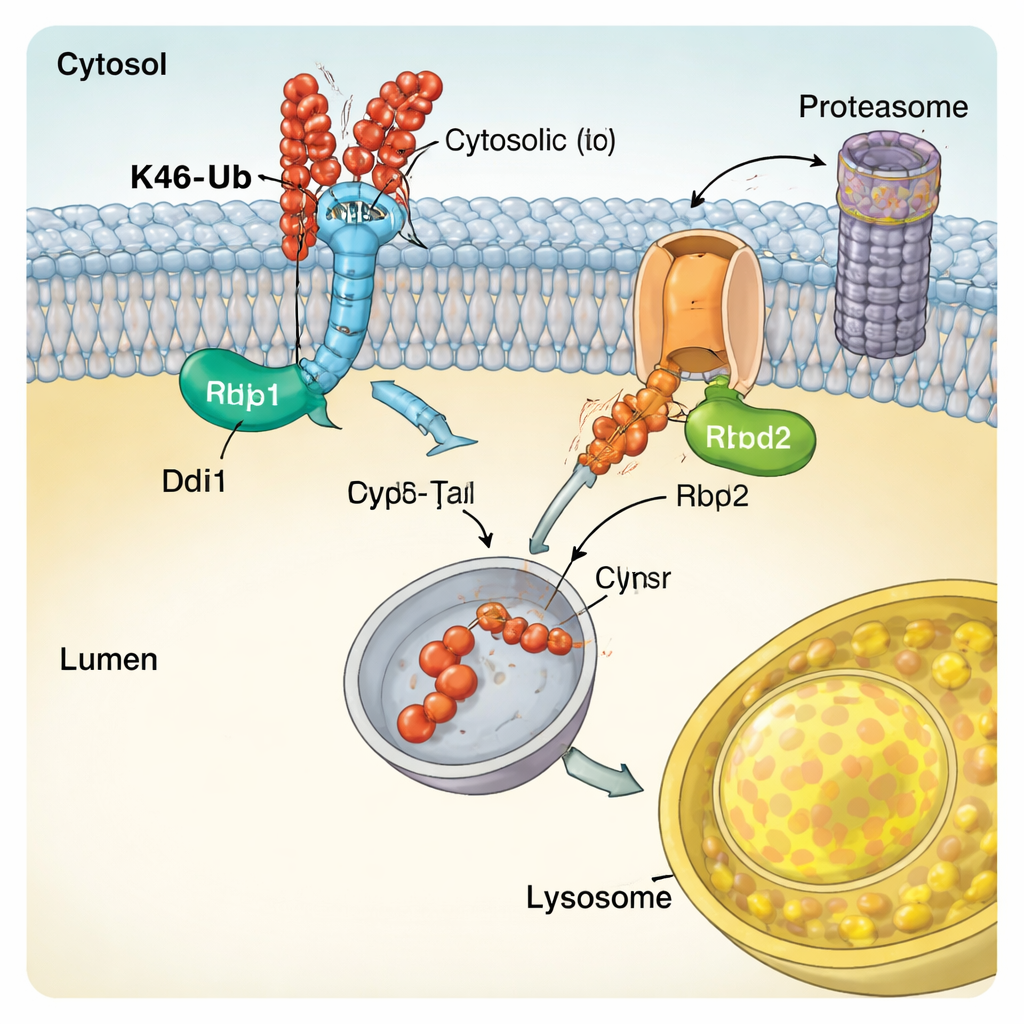
Enzimas especializadas que leem o código da ubiquitina
Para entender como o CUT-UP reconhece seus alvos, os autores examinaram as características moleculares de Ddi1. Eles mostraram que o núcleo catalítico central de Ddi1 não apenas corta proteínas, mas também pode se ligar à ubiquitina diretamente, e que sua atividade é modulada por regiões extras que se prendem às cadeias de ubiquitina. Ddi1 mostrou uma dependência particular por cadeias ligadas por K48, compatível com seu papel no CUT-UP. Rbd2, por outro lado, é uma protease romboide que atravessa a membrana. O estudo constatou que o sítio ativo de Rbd2 é essencial para cortar as porções de Vps10 voltadas para o lúmen e que a enzima transita por vários compartimentos da via secretora, permitindo que atue em múltiplas localizações celulares. Enzimas semelhantes existem em células humanas e têm sido implicadas em condições que vão da neurodegeneração ao câncer, sugerindo que mecanismos semelhantes ao CUT-UP podem ter importância ampla.
Por que isso importa para a saúde e a terapia
Ao mostrar que diferentes tipos de cadeia de ubiquitina encaminham a mesma proteína de membrana para destinos bem distintos — seja para a triagem por corpos multivesiculares ou para a fatiamento mediado pelo CUT-UP — este trabalho fornece evidências fortes de que as células usam um verdadeiro “código da ubiquitina” para ajustar finamente o descarte de proteínas. A descoberta do CUT-UP esclarece como proteínas de membrana resistentes podem ser desmontadas peça por peça e destaca Ddi1 e Rbd2 como atores-chave que leem e aplicam esse código. Para não especialistas, a lição é que as células não apenas marcam proteínas como lixo; elas especificam como esse lixo será removido. À medida que desenvolvedores de fármacos projetam ferramentas que etiquetam proteínas nocivas com ubiquitina para removê-las, entender vias como o CUT-UP será essencial para prever quais fragmentos serão produzidos e como isso pode afetar o comportamento celular.
Citação: Minard, A.Y., Winistorfer, S., Yu, L. et al. K48-ubiquitin-dependent proteases cut-up post-ER proteins. Nat Commun 17, 1669 (2026). https://doi.org/10.1038/s41467-026-68367-7
Palavras-chave: código da ubiquitina, degradação de proteínas, proteínas de membrana, proteassoma, lisossomo