Clear Sky Science · pt
Perda da sinalização por quorum Fsr promove formação de biofilme e piora os desfechos na endocardite infecciosa enterocócica
Sabotadores silenciosos nas válvulas do coração
A endocardite infecciosa é uma infecção potencialmente letal das válvulas cardíacas, e sua incidência tem aumentado no mundo todo. Este estudo foca em um culpado principal, a bactéria intestinal Enterococcus faecalis, e investiga por que algumas infecções são especialmente difíceis de tratar. Ao desvendar como essas bactérias se comunicam e constroem biofilmes protetores nas válvulas cardíacas, os pesquisadores mostram por que certas cepas causam doenças mais graves e resistem a antibióticos, e por que um sistema de comunicação bacteriana chamado Fsr se revela, surpreendentemente, um freio em vez de um acelerador do dano.
Como as bactérias constroem fortalezas no coração
As válvulas cardíacas normalmente suportam alguns dos fluxos sanguíneos mais rápidos do corpo, mas se a superfície da válvula for danificada, plaquetas e proteínas de coagulação podem formar um pequeno coágulo, ou vegetação. Esse coágulo torna‑se uma plataforma para bactérias na corrente sanguínea. Uma vez aderidas, as bactérias se multiplicam e se entrelaçam em um biofilme — uma comunidade viscosa e estruturada que as protege de células imunes e de drogas. A equipe usou dispositivos microfluídicos para imitar o fluxo sanguíneo em laboratório e um modelo em ratos para recriar a endocardite em animais vivos, permitindo observar como E. faecalis se adapta à medida que a infecção evolui de algumas células isoladas para biofilmes espessos e maduros. 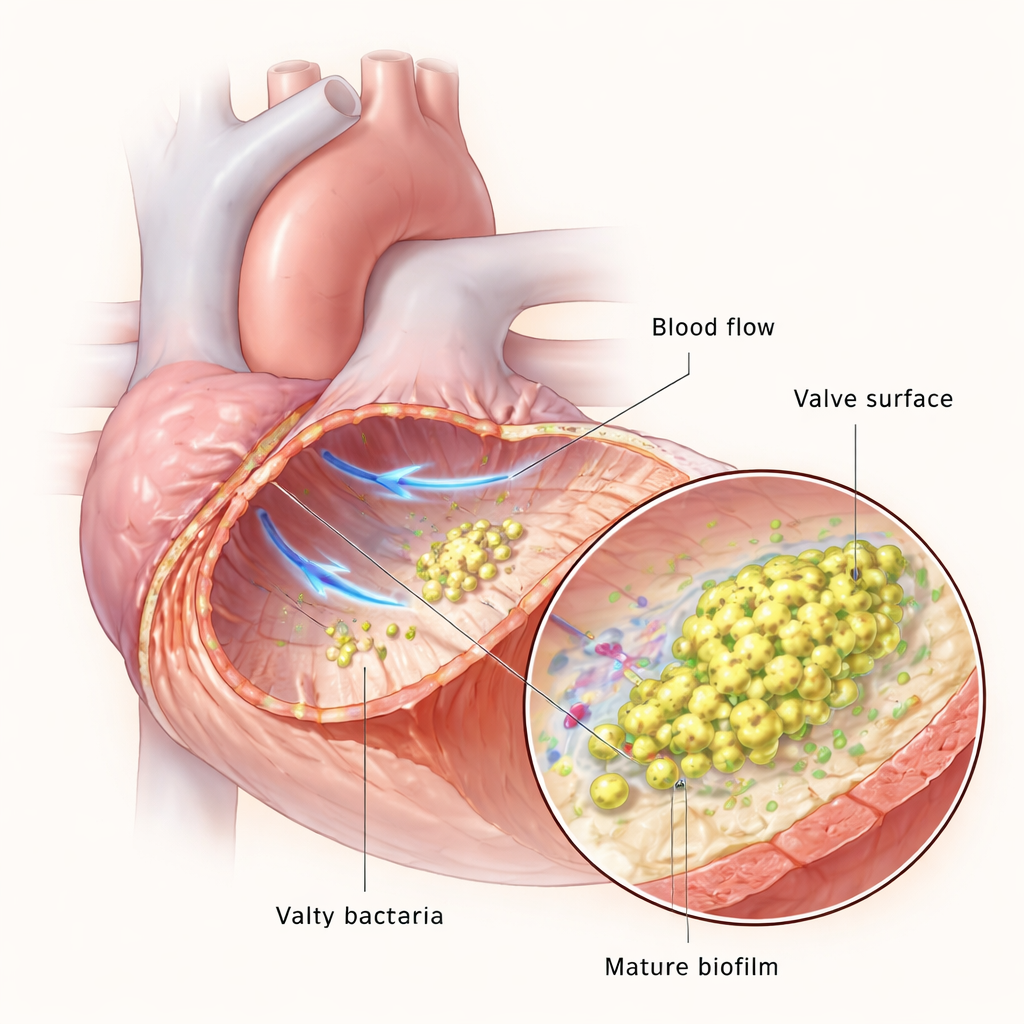
Quando o fluxo sanguíneo forte desliga o “conversa” bacteriana
As bactérias frequentemente coordenam seu comportamento por meio de quorum sensing, um sistema químico de “votação” que liga ou desliga genes quando há células suficientes. O sistema Fsr é o quorum sensing usado por E. faecalis. Surpreendentemente, os pesquisadores descobriram que um fluxo de fluido forte e em movimento realmente arrasta as moléculas sinalizadoras necessárias para ativar o Fsr. No início da infecção, quando as bactérias estão presas à superfície exposta da vegetação e sentem toda a força do fluxo sanguíneo, o Fsr fica amplamente silencioso. Só mais tarde, quando microcolônias crescem e ficam enterradas mais profundamente na vegetação — protegidas do fluxo — o Fsr se ativa. Isso significa que, no coração real, o quorum sensing é governado não apenas pelo número de bactérias presentes, mas também por onde elas se situam dentro da estrutura tridimensional.
Desligar o Fsr permite que os biofilmes cresçam demais
Para testar o que o Fsr realmente faz na infecção, a equipe comparou bactérias normais com mutantes que faltavam todo o sistema Fsr. No início, ambas as versões colonizaram as válvulas igualmente bem. Mas aos três dias, animais infectados com cepas deficientes em Fsr apresentaram vegetações maiores e muito mais bactérias nelas. Imagens detalhadas mostraram que seus biofilmes cobriam mais da superfície do coágulo e que suas microcolônias eram maiores. A perda do Fsr também desligou duas enzimas secretadas-chave, GelE e SprE, que normalmente ajudam a moldar o biofilme e podem limitar o crescimento excessivo. Animais infectados com mutantes sem apenas essas enzimas também desenvolveram biofilmes volumosos, embora não tão extremos quanto nas cepas nulas para Fsr, sugerindo que outros fatores controlados pelo Fsr também contribuem. 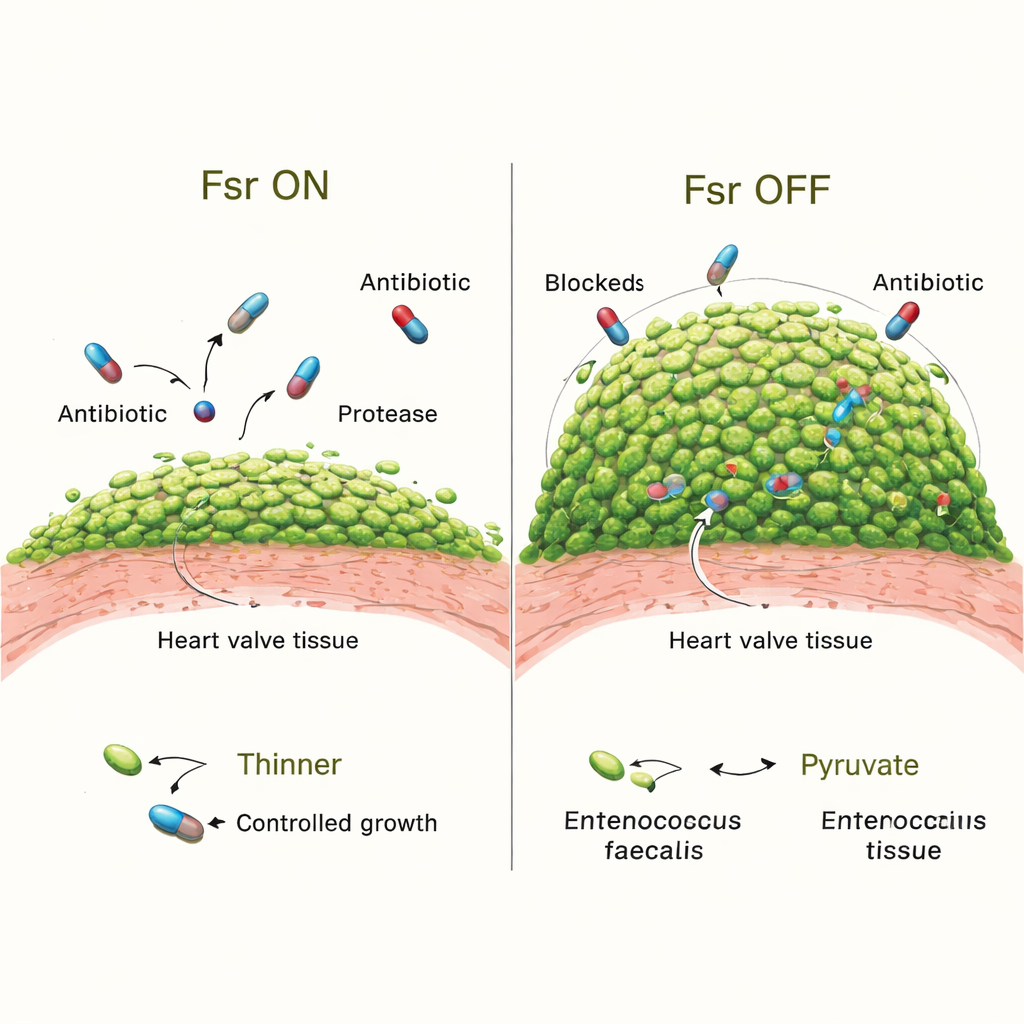
Reprogramação metabólica e maior tolerância a antibióticos
O perfil de expressão gênica das bactérias dentro de válvulas infectadas revelou que o Fsr faz mais do que controlar algumas enzimas. Sem Fsr, centenas de genes alteraram sua atividade, especialmente aqueles envolvidos na captação de açúcares e na produção de energia. Um par de genes, lrgA e lrgB, destacou‑se: foram fortemente ativados em bactérias deficientes em Fsr e ajudaram as células a explorar melhor o piruvato, uma pequena molécula rica em energia presente no sangue. Quando os pesquisadores deletaram lrgAB juntamente com Fsr, o crescimento excessivo do biofilme desapareceu, apontando para um papel-chave dessa via metabólica no impulsionamento da infecção sobressalente. Notavelmente, os biofilmes deficientes em Fsr também foram mais difíceis de tratar. Em ratos tratados com o antibiótico gentamicina, infecções por bactérias normais diminuíram e as contagens de plaquetas — um marcador de gravidade da doença — melhoraram. Em contraste, infecções sem Fsr quase não responderam, mesmo que as bactérias não apresentassem maior resistência aos fármacos em testes laboratoriais padrão.
Uma reviravolta específica em humanos na inflamação
O estudo também revelou uma possível forma como essas bactérias podem provocar inflamação em pessoas. A enzima GelE pode cortar o precursor humano do sinal imune IL‑1β em uma forma ativa que desencadeia respostas inflamatórias. Intrigantemente, GelE cortou o IL‑1β de rato de maneira diferente, degradando‑o em vez de ativá‑lo, e o corte preciso que ativa estava ausente nas proteínas de rato e camundongo. Esse efeito específico por espécie sugere que, em humanos, GelE pode ajudar a concentrar a inflamação justamente na borda do biofilme, possivelmente agravando o dano tecidual durante a endocardite.
Do banco ao leito: por que a perda de Fsr importa para pacientes
Para avaliar se essas descobertas experimentais importavam na prática clínica, os pesquisadores analisaram isolados de E. faecalis de 81 pacientes com endocardite infecciosa na Suíça e nos Estados Unidos. Quase metade das cepas naturalmente carecia do sistema Fsr. Pacientes infectados por essas cepas Fsr‑negativas tiveram bacteremia de duração mais longa — mais dias com bactérias detectáveis no sangue — e tiveram maior probabilidade de cair em uma categoria de alta gravidade que incluiu cuidados intensivos, internações prolongadas, procedimentos cardíacos maiores ou morte. Outros genes de virulência não explicaram esse padrão, apontando diretamente para a perda do Fsr como um marcador-chave de doença mais agressiva.
Por que isso importa para tratamentos futuros
Em conjunto, essas descobertas derrubam a ideia simplista de que bloquear a comunicação bacteriana sempre enfraquecerá as infecções. Na endocardite por E. faecalis, o sistema Fsr na verdade restringe a expansão do biofilme e torna as bactérias mais vulneráveis aos antibióticos. Quando o Fsr está ausente, as bactérias formam biofilmes mais densos, exploram nutrientes do sangue com mais eficiência e ajudam a conduzir infecções persistentes e difíceis de erradicar. Para os pacientes, isso significa que cepas sem Fsr podem prever doenças mais difíceis de tratar, e que terapias que bloqueiem indiscriminadamente o quorum sensing podem ter efeito contrário nesse contexto. Em vez disso, direcionar cuidadosamente vias metabólicas como o uso de piruvato, ou monitorar o status de Fsr e GelE como marcadores prognósticos, pode oferecer maneiras melhores de manejar essas perigosas infecções cardíacas.
Citação: Antypas, H., Schmidtchen, V., Staiger, W.I. et al. Loss of Fsr quorum sensing promotes biofilm formation and worsens outcomes in enterococcal infective endocarditis. Nat Commun 17, 1668 (2026). https://doi.org/10.1038/s41467-026-68366-8
Palavras-chave: endocardite infecciosa, biofilmes bacterianos, sinalização por quorum, Enterococcus faecalis, tolerância a antibióticos