Clear Sky Science · pt
VPg saRNA projetado alcança codificação cap-independent, de baixa imunogenicidade e precisa de proteínas terapêuticas in vivo
Reescrevendo as regras para medicamentos de RNA
Vacinas baseadas em RNA mensageiro (mRNA) ajudaram a mudar o curso da pandemia de COVID-19, mas usar moléculas semelhantes para substituir ou suplementar proteínas ausentes em doenças crônicas é bem mais difícil. O corpo tende a destruir RNA estranho rapidamente e a montar respostas imunes fortes, e muitos designs de RNA auto-amplificante existentes cometem erros ao se copiarem. Este estudo descreve um novo tipo de RNA auto-amplificante — construído a partir de partes do norovírus humano — que foi projetado para ser duradouro, menos inflamatório e incomumente preciso, abrindo caminho para medicamentos de RNA mais precisos e duráveis.
Um RNA auto-copiador mais inteligente
Medicamentos convencionais de mRNA carregam uma única “receita” para uma proteína e são lidos uma vez pela célula antes de serem degradados. O RNA auto-amplificante (saRNA) inclui maquinário viral extra que permite que o RNA se copie dentro das células, aumentando muito a produção a partir de uma dose pequena. Os sistemas saRNA mais estudados vêm de alfavírus, mas são volumosos, desencadeiam fortes defesas antivirais e copiam suas sequências com precisão relativamente baixa. Os autores, em vez disso, voltaram-se ao norovírus humano, uma causa comum de gastroenterite. Eles isolaram uma seção compacta do material genético do norovírus e a reconstruiu como um transportador para genes terapêuticos. No seu núcleo está o VPg, uma pequena proteína viral quimicamente ligada à extremidade frontal do RNA. O VPg substitui a estrutura de “cap” habitual encontrada nos mRNAs humanos e permite que o RNA seja traduzido por um conjunto diferente de fatores celulares que são menos sensíveis a certos sinais de estresse. 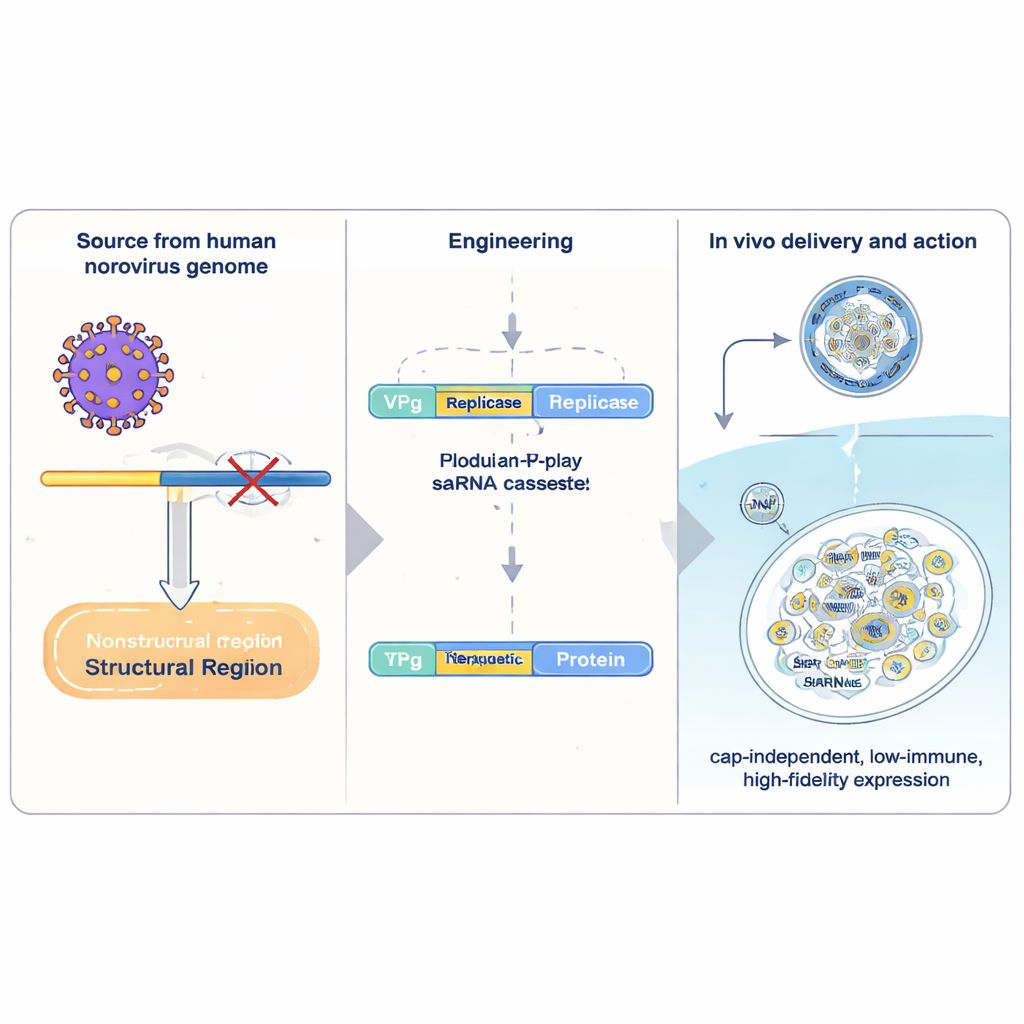
Alta precisão sem provocar a imunidade
Para terapias proteicas, a precisão importa: mesmo pequenos erros de cópia podem alterar o comportamento de um fármaco ou criar subprodutos tóxicos. A equipe mostrou que quando o VPg do norovírus se liga à enzima que copia o RNA do vírus (uma polimerase), ele reduz a velocidade com que blocos de construção incorretos são adicionados, diminuindo fortemente a taxa de erro. Eles identificaram aminoácidos específicos no VPg que contactam uma região de controle chave da polimerase e demonstraram que perturbar essa interface torna a cópia menos precisa. Ao mesmo tempo, os designs clássicos de saRNA geram grandes quantidades de RNA dupla fita, um alarme molecular que ativa defesas antivirais e interrompe a produção proteica. Ao redesenhar a polimerase para favorecer uma forma inicial ligada ao VPg e ao reorganizar o genoma para que apenas a fita terapêutica seja produzida de forma eficiente, os autores reduziram muito a formação de RNA dupla fita. Eles ainda ajustaram uma região de cauda do RNA para que o VPg se ligue no sítio correto, evitando fragmentos curtos e não intencionais que poderiam traduzir-se em peptídeos indesejados.
Funciona onde o mRNA padrão falha
O novo saRNA baseado em VPg foi então testado em cenários de doença exigentes onde o mRNA com cap comum tem problemas. Na caquexia associada ao câncer — uma síndrome de desgaste em que músculos e gordura desaparecem — fatores de tradução essenciais que reconhecem o cap padrão do mRNA são desligados, tornando mRNAs cap-dependentes ineficientes. Como o VPg usa um ponto de entrada alternativo na maquinaria de tradução celular, ele continuou a impulsionar a produção do hormônio da fome e do metabolismo, ghrelina, em um modelo murino de câncer de pâncreas. Injeções mensais de baixa dose ajudaram a preservar músculo e gordura, melhoraram a ingestão alimentar e o metabolismo, e estenderam modestamente a sobrevida, sem toxicidade óbvia ou sinais de ativação imunológica crônica.
Ataque preciso ao câncer e autoimunidade mais contida
Para testar se a cópia de alta fidelidade realmente importa, os pesquisadores carregaram o vetor VPg com um construto oncolítico complexo, GSDMDENG, projetado para abrir buracos nas mitocôndrias de células cancerosas e estimular respostas imunes específicas ao tumor. Quando o mesmo construto foi colocado em um saRNA convencional de alfavírus, mutações se acumularam após rodadas repetidas de cópia e enfraqueceram suas funções seletivas de matar câncer e de primear a imunidade. Em contraste, o sistema VPg preservou a sequência pretendida, produziu forte morte de células tumorais e desencadeou respostas duráveis de células T que retardaram ou impediram o câncer de pâncreas em modelos murinos. Finalmente, aplicaram o saRNA VPg a um desafio diferente: doença enxerto-contra-hospedeiro crônica, em que células imunes atacam os pulmões após transplante de medula óssea. Um saRNA VPg codificando proteína C ativada reduziu a formação de anticorpos nocivos, preveniu o enrijecimento pulmonar e melhorou a respiração em camundongos, enquanto um construto comparável à base de alfavírus provocou imunidade inata mais forte e piorou os desfechos.
Por que isso importa para futuros medicamentos de RNA
Em conjunto, o trabalho descreve uma plataforma de RNA compacta e “plug-and-play” que reúne três características desejáveis: ela se copia com precisão, foi projetada para minimizar alarmes imunes e contorna alguns dos gargalos que restringem a tradução do mRNA padrão. Como o gene terapêutico é simplesmente trocado em um arcabouço fixo baseado em norovírus, muitas proteínas diferentes — de hormônios a reguladores de coagulação a agentes oncolíticos — podem ser testadas no mesmo chassi. Embora muito trabalho ainda seja necessário antes do uso em humanos, essa abordagem de saRNA com VPg sugere um caminho rumo a medicamentos de RNA que atuem mais como infusões proteicas estáveis: de baixa dose, de duração mais longa e capazes de operar mesmo em tecidos doentes onde mensagens de mRNA comuns não podem ser lidas de forma confiável. 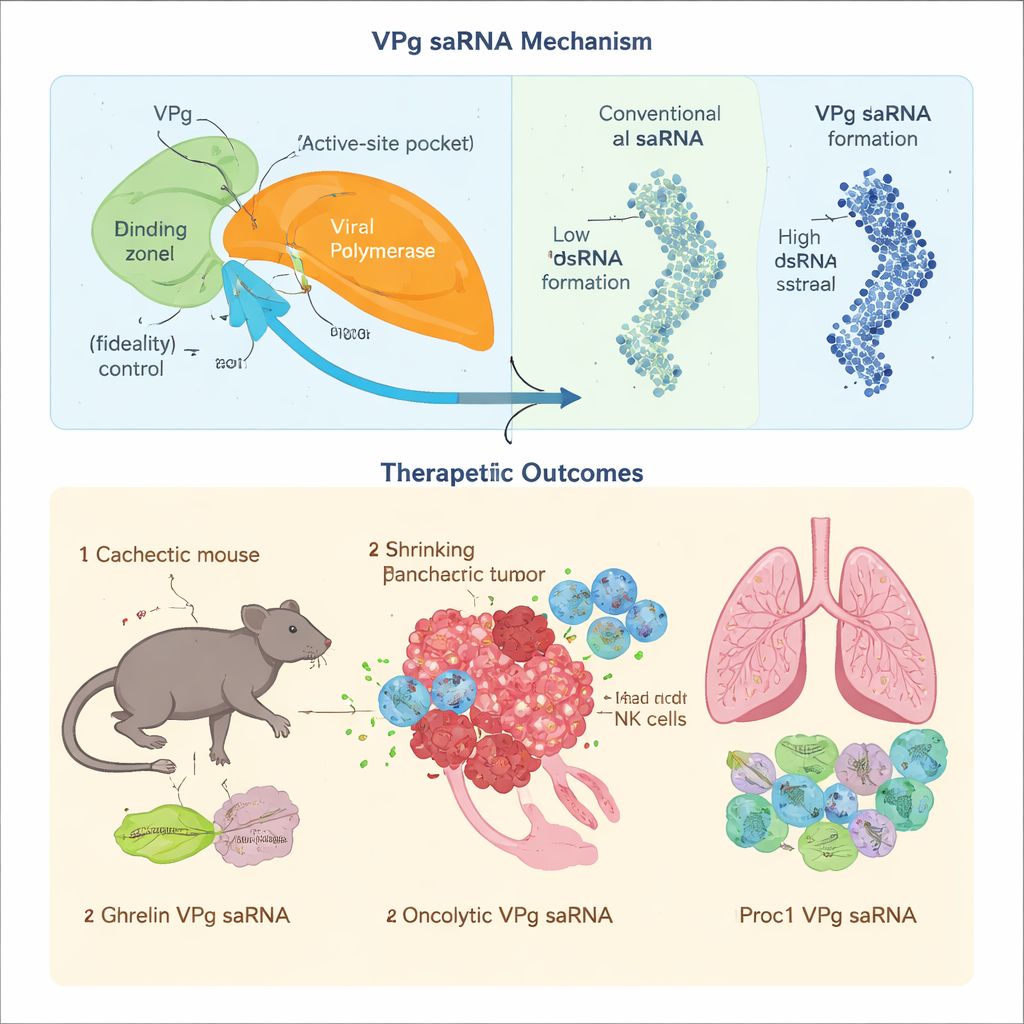
Citação: Feng, Z., Chu, L., Li, Q. et al. Engineered VPg saRNA achieves cap-independent, low-immunogenic and precise encoding of therapeutic proteins in vivo. Nat Commun 17, 1666 (2026). https://doi.org/10.1038/s41467-026-68364-w
Palavras-chave: RNA auto-amplificante, terapêuticas com mRNA, VPg do norovírus, caquexia associada ao câncer, doença enxerto-contra-hospedeiro