Clear Sky Science · pt
O papel de repetições de baixa complexidade em interações RNA–RNA e uma plataforma de deep learning para previsão de duplos
Sequências de RNA “pegajosas” que moldam o comportamento celular
Dentro de cada célula, moléculas de RNA colidem constantemente, formando parcerias efêmeras que ajudam a controlar quais genes são ativados, como proteínas são produzidas e como as células se desenvolvem. Este estudo revela que muitos desses encontros RNA–RNA não são aleatórios: são guiados por sequências curtas, simples e altamente repetitivas que atuam como velcro molecular. Os pesquisadores também desenvolveram uma ferramenta de inteligência artificial capaz de identificar onde tais pares de RNA provavelmente se formam, abrindo novas formas de explorar como as células funcionam em saúde e doença.
Repetições simples com efeitos poderosos
O RNA costuma ser descrito como uma mensageiro que carrega informação genética do DNA para as proteínas, mas ele também atua como andaime, regulador e guia. Grande parte dessa atividade depende da união de duas cadeias de RNA. Ao combinar dados de vários levantamentos experimentais abrangentes em células humanas e de camundongo, os autores mostram que as regiões de RNA que realmente participam desse emparelhamento são fortemente enriquecidas em repetições de baixa complexidade. São trechos construídos a partir de motivos curtos — como séries de bases G e C — repetidos várias vezes. Em vez de serem “lixo” genômico, esses pedaços repetitivos se mostram locais preferenciais onde um RNA pode se ligar a muitos outros, formando centros densos de interação através do transcriptoma. 
Hubs de RNA para desenvolvimento e regulação
Ao examinar quais genes carregam esses sítios de contato ricos em repetições, surgiu um padrão marcante: muitos codificam proteínas que controlam o desenvolvimento e a identidade celular, como fatores de transcrição. Mesmo em linhagens celulares cancerosas que não estão ativamente se diferenciando, RNAs ligados a programas de desenvolvimento participaram intensamente de contatos baseados em repetições. Os autores também analisaram com detalhe certos RNAs longos não codificantes (lncRNAs), que não codificam proteínas, mas frequentemente as regulam. Por exemplo, alvos do lncRNA TINCR e de outro lncRNA importante para a formação de neurônios motores, Lhx1os, exibiram excesso de repetições complementares. Nesses casos, repetições simples no lncRNA são pareadas por repetições complementares nos RNAs parceiros, permitindo emparelhamentos estáveis que podem ajudar a ajustar os níveis ou a tradução de genes de desenvolvimento-chave.
Onde proteínas e enzimas de edição entram
Esses contatos mediados por repetições raramente atuam sozinhos. Os autores sobrepuseram mapas de ligação de proteínas aos seus dados de interação e descobriram que muitos sítios de contato portadores de repetições também são reconhecidos por proteínas de ligação ao RNA envolvidas no controle da tradução, na degradação de RNA e na formação de grânulos citoplasmáticos, como P-bodies e grânulos de estresse. Uma proteína em particular, STAU1, que pode desencadear a destruição de seus alvos de RNA, liga-se com frequência aos duplos formados por repetições de baixa complexidade. A redução de STAU1 levou a níveis mais altos de RNAs envolvidos nesses duplos, especialmente daqueles que carregam repetições, sugerindo que o emparelhamento mediado por repetições pode sinalizar transcritos para degradação controlada. As mesmas regiões ricas em repetições também atraem enzimas de edição de RNA como ADAR1, que modificam quimicamente bases específicas dentro de RNA de fita dupla, indicando que repetições de baixa complexidade ajudam a posicionar sítios de edição que afinam o comportamento do RNA.
Ensinando uma rede neural a ler contatos de RNA
Programas convencionais tentam prever a ligação RNA–RNA com base principalmente na estabilidade termodinâmica — quanta energia seria necessária para formar ou quebrar um duplo. Embora úteis, esses modelos muitas vezes deixam de captar interações reais observadas em células, especialmente entre RNAs longos. Para ir além das regras energéticas simples, os autores treinaram um modelo de deep learning chamado RIME que usa embeddings no estilo de “modelos de linguagem”: representações numéricas de sequências de RNA que codificam padrões aprendidos a partir de grandes coleções de dados de ácidos nucleicos. O RIME é apresentado a pares de segmentos de RNA e aprende a classificar se eles interagem, usando muitos emparelhamentos reais de experimentos de crosslinking com psoraleno como exemplos positivos e pares não interagentes cuidadosamente construídos como negativos. 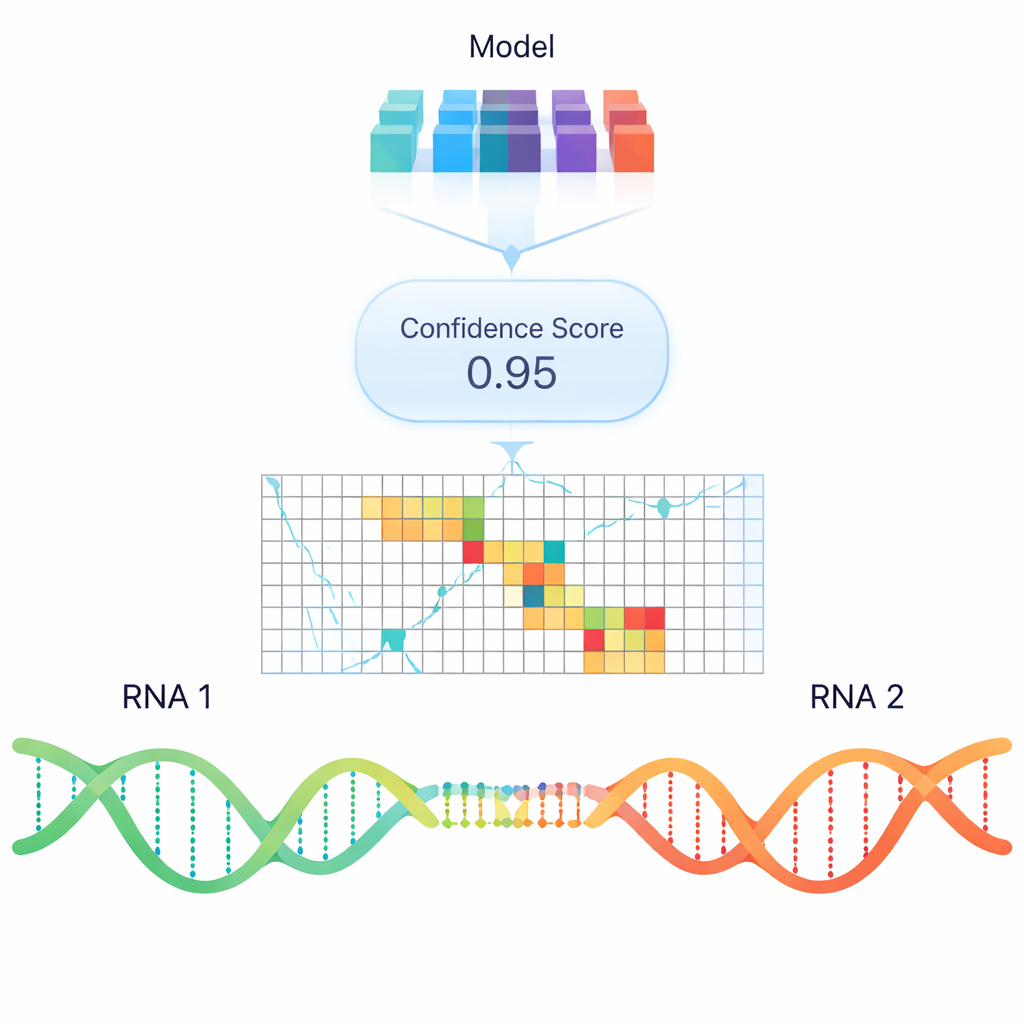
Previsões mais inteligentes e novas pistas biológicas
Quando comparado a ferramentas líderes baseadas em termodinâmica e a outro método por rede neural, o RIME apresenta desempenho consistentemente melhor na distinção entre contatos reais de RNA–RNA e falsos, especialmente para interações experimentais de alta confiança. Ele não apenas prevê se dois RNAs irão parear, como também tende a destacar as regiões exatas envolvidas, e aprende naturalmente que repetições de baixa complexidade são fortes preditoras de contato. Notavelmente, o mesmo modelo, treinado apenas em interações entre RNAs distintos, também funciona bem para prever o pareamento interno de bases dentro de uma única molécula de RNA, alinhando-se com experimentos estruturais e com algoritmos clássicos de dobramento. Para reguladores não codificantes como TINCR, NORAD e SMaRT, o RIME redescobre com sucesso sítios de interação funcionais conhecidos e sugere regiões candidatas adicionais.
Por que isso importa
Para um leitor leigo, a mensagem-chave é que trechos curtos e repetitivos no RNA — antes fáceis de desprezar como ruído inútil — atuam como pontos centrais de conexão no diagrama de fiação de RNA da célula. Eles ajudam a aproximar RNAs, atraem proteínas reguladoras e enzimas de edição, e são amplamente usados em vias que controlam como as células se desenvolvem e respondem ao estresse. O novo modelo RIME fornece aos pesquisadores uma ferramenta poderosa para vasculhar genomas em busca dessas parcerias RNA–RNA, incluindo aquelas que podem falhar em doenças neurológicas e outras ligadas à expansão de repetições. Em essência, este trabalho mostra que entender — e prever — como repetições simples de RNA se unem pode revelar camadas ocultas de regulação gênica.
Citação: Setti, A., Bini, G., Pellegrini, F. et al. The role of low-complexity repeats in RNA–RNA interactions and a deep learning framework for duplex prediction. Nat Commun 17, 1637 (2026). https://doi.org/10.1038/s41467-026-68356-w
Palavras-chave: Interações RNA–RNA, repetições de baixa complexidade, RNA longo não codificante, deep learning, regulação gênica