Clear Sky Science · pt
Depleção guiada por assinatura transcriptômica de células epiteliais alveolares intermediárias melhora a fibrose pulmonar em camundongos
Por que pulmões cicatrizados importam
A fibrose pulmonar é uma doença grave dos pulmões em que os delicados alvéolos gradualmente se transformam em tecido cicatricial rígido, tornando cada respiração um esforço. Os médicos sabem que essa cicatrização começa quando os processos normais de reparo saem do controle, mas não estava claro quais células específicas são as responsáveis e como removê‑las sem prejudicar o tecido pulmonar saudável. Este estudo explora uma nova maneira de “ler” as mensagens moleculares dentro das células pulmonares, usar essa informação para identificar células transitórias prejudiciais e eliminá‑las seletivamente para reduzir a cicatrização em camundongos.
Células flagradas no ato de um reparo defeituoso
Após uma lesão pulmonar, células especiais que produzem surfactante chamadas células do tipo II normalmente se multiplicam e depois amadurecem em células do tipo I, finas, que revestem os alvéolos e permitem a passagem de oxigênio para o sangue. Na fibrose, muitas dessas células ficam presas em um estado intermediário ou transitório, em vez de completar essa transformação. Estudos anteriores de sequenciamento de RNA de célula única haviam identificado essas células intermediárias em camundongos e humanos, mas não estava claro se eram meros espectadores ou agentes-chave da doença. Os autores concentraram‑se em um tipo transitório de camundongo chamado Krt8+ intermediários de diferenciação alveolar, e em seus equivalentes humanos conhecidos como células basaloides aberrantes, que aparecem em grande número em pulmões cicatrizados.
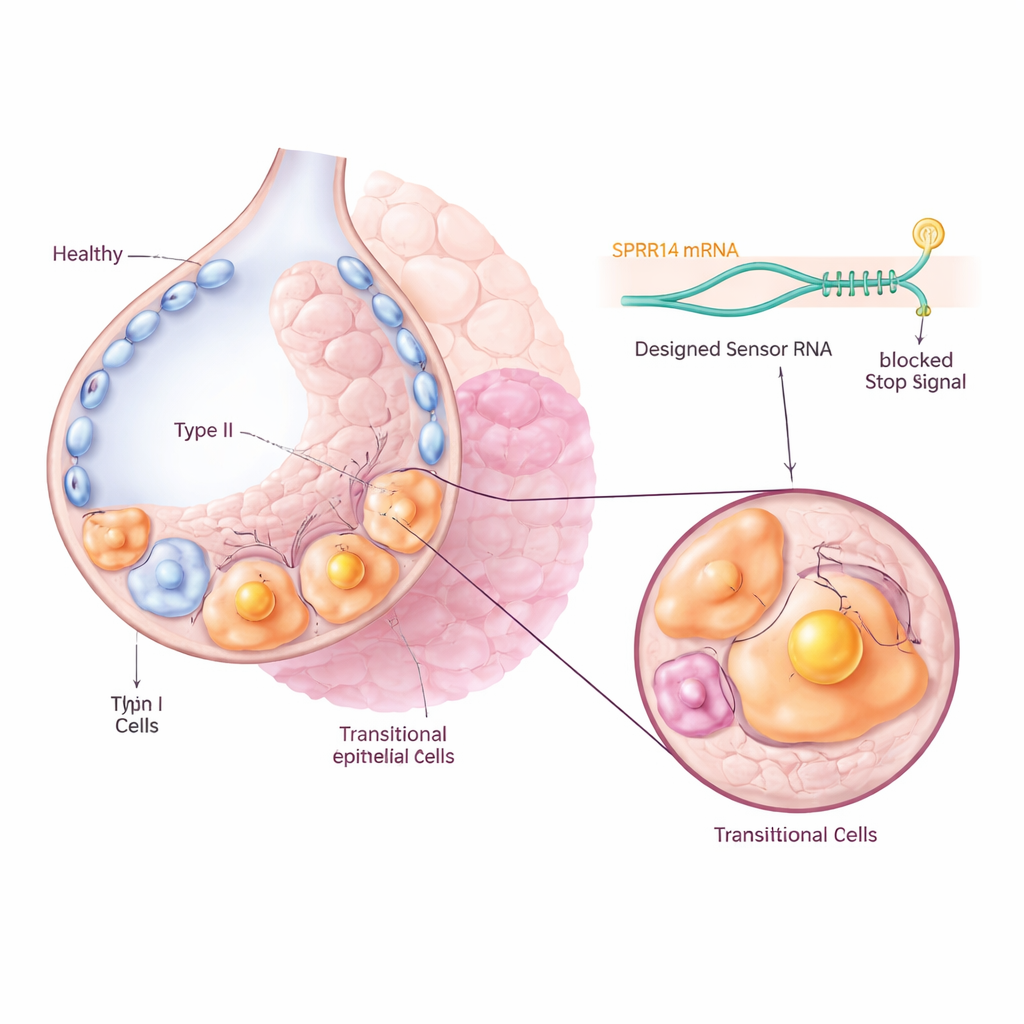
Encontrando uma etiqueta molecular única
Para direcionar essas células problemáticas sem atingir suas vizinhas saudáveis, a equipe primeiro procurou em grandes conjuntos de dados de expressão gênica um marcador que fosse fortemente e especificamente ativado na população transitória. Eles identificaram uma molécula chamada SPRR1A como uma “etiqueta” distintiva: estava altamente enriquecida em células intermediárias Krt8+ em pulmões fibróticos de camundongos e em células basaloides aberrantes KRT5-/KRT17+ de pacientes com fibrose pulmonar idiopática, mas praticamente ausente em células pulmonares normais. A microscopia de tecido pulmonar de camundongos e humanos confirmou que SPRR1A aparecia principalmente em regiões lesionadas e remodeladas e não nos alvéolos saudáveis, sugerindo que poderia servir como um identificador preciso para as células culpadas.
Programando células com um sensor de RNA
Os pesquisadores então usaram uma tecnologia recentemente desenvolvida chamada CellREADR, que funciona como um sensor molecular interno. Eles desenharam sequências curtas de RNA que podem parear com o RNA de SPRR1A dentro de uma célula. Quando o sensor detecta SPRR1A, ele dispara a produção de uma proteína “efetora” acoplada, como uma etiqueta fluorescente ou um receptor que torna a célula sensível a um medicamento. Em camundongos, vírus foram usados para entregar esses construtos sensor‑efetor às células pulmonares. Apenas as células que produziam ativamente SPRR1A ligaram o sinal fluorescente, permitindo à equipe rastrear e isolar as células transitórias diretamente de pulmões fibróticos. O sequenciamento de célula única mostrou que as células marcadas correspondiam de perto à assinatura gênica conhecida das transitórias, confirmando que o sensor de RNA estava atingindo com precisão a população pretendida.
Desativando intermediárias prejudiciais
Em seguida, o efetor foi trocado de uma proteína fluorescente inofensiva para o receptor da toxina diftérica, de modo que células positivas para SPRR1A pudessem ser seletivamente eliminadas pela administração de toxina diftérica. Ao cronometrar o tratamento para coincidir com o pico de abundância das células transitórias após lesão química no pulmão, os autores conseguiram remover cerca de um terço dessa população. Essa depleção direcionada resultou em bem menos cicatrização pulmonar: houve menor acúmulo de colágeno, níveis reduzidos de proteínas fibróticas e estruturas alveolares com aparência mais normal. Análises detalhadas mostraram que a maioria das células positivas para SPRR1A exibiam sinais de um estado estressado e semelhante ao envelhecimento, com um pequeno subconjunto capaz de alta proliferação, sugerindo que essas intermediárias tanto falham em reparar propriamente o tecido quanto ajudam a sustentar o processo fibrótico.
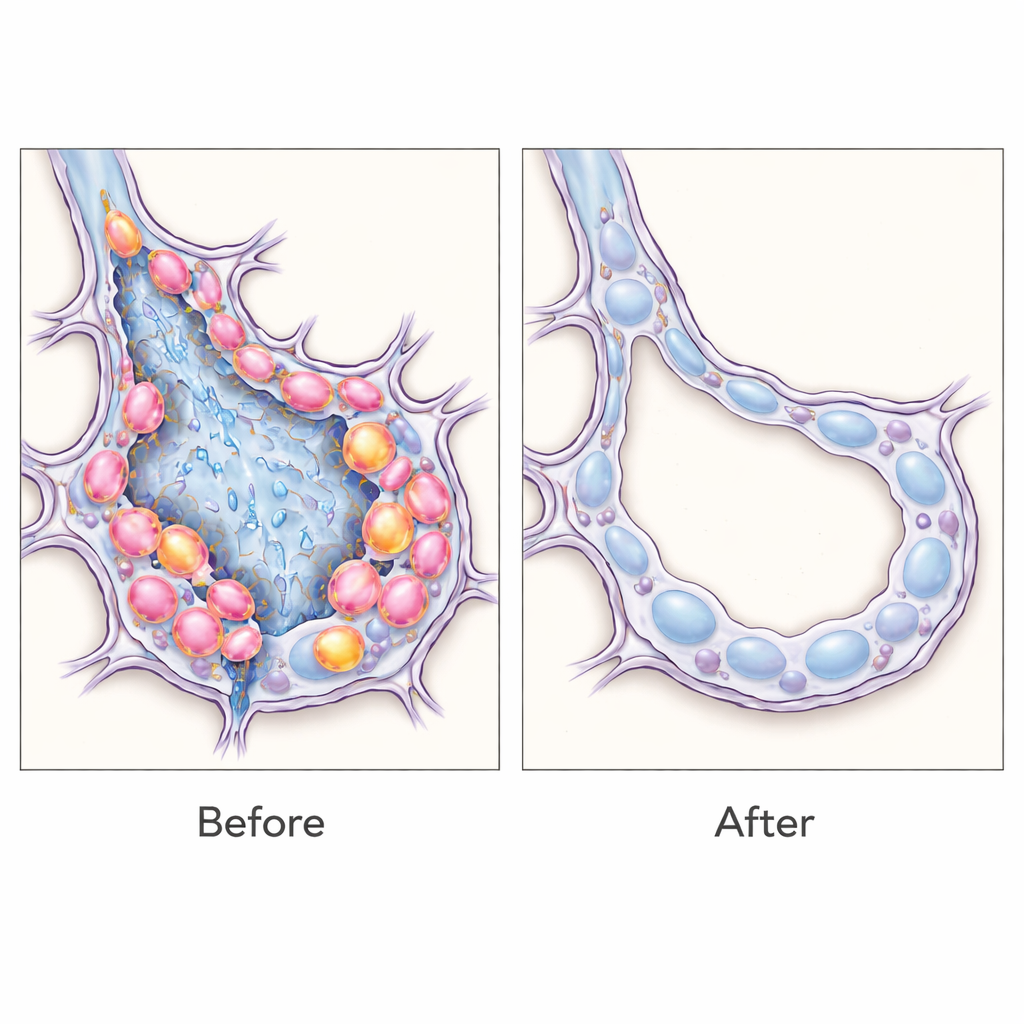
O que isso significa para tratamentos futuros
Esses achados indicam que as células epiteliais transitórias não são apenas marcadores, mas motoras ativas da fibrose pulmonar, e que removê‑las seletivamente pode inclinar a balança de volta para uma arquitetura pulmonar mais saudável em camundongos. De forma mais ampla, o trabalho demonstra uma estratégia flexível: ao “ler” assinaturas de RNA específicas de células, os pesquisadores podem rotular, estudar e até eliminar populações celulares estreitamente definidas em tecido vivo sem criar linhagens animais personalizadas a cada vez. Embora ainda reste muito trabalho antes que tais ferramentas de detecção de RNA possam ser adaptadas com segurança para humanos, essa abordagem abre um caminho para terapias de precisão que visem os tipos celulares exatos que atrapalham a cicatrização em fibrose pulmonar crônica e, potencialmente, em outras doenças fibróticas.
Citação: Peng, F., Jiang, Cs., Zheng, Z. et al. Transcriptomic signature-guided depletion of intermediate alveolar epithelial cells ameliorates pulmonary fibrosis in mice. Nat Commun 17, 1636 (2026). https://doi.org/10.1038/s41467-026-68354-y
Palavras-chave: fibrose pulmonar, células epiteliais alveolares, sequenciamento de RNA de célula única, tecnologia de detecção de RNA, senescência celular